Le diabète de type 2 est une maladie chronique qui se déclare généralement après l’âge de 40 ans et qui se caractérise par une élévation du taux de glucose dans le sang (hyperglycémie). Cette pathologie résulte d’une résistance à l’insuline souvent associée à une production insuffisante de cette hormone. De plus en plus fréquent, le diabète de type 2 est principalement lié à des facteurs comme l’obésité, la sédentarité et des prédispositions génétiques. Ses complications incluent des troubles cardiovasculaires, ophtalmologiques, rénaux et nerveux. Une prise en charge adaptée combine alimentation, activité physique et traitements médicamenteux.
Le diabète de type 2 (anciennement appelé diabète gras) est l’affection métabolique la plus répandue dans le monde et touchait environ 510 millions de personnes en 2021. Sa prévalence s’accroît de manière exponentielle et les projections indiquent qu’en 2050, plus de 1,27 milliard de personnes devraient vivre avec un diabète de type 2 1.
Cette maladie, qui se déclare le plus souvent après l’âge de 40 ans, résulte de l’interaction de différents facteurs environnementaux et génétiques qui aboutissent au développement d’une résistance à l’insuline engendrant une hyperglycémie. Le traitement de première intention n’est généralement pas l’insuline, qui est correctement sécrétée au début de la maladie. Cette forme de diabète est donc également appelée diabète non-insulinodépendant.
Le traitement repose dans un premier temps sur des modifications de l’hygiène de vie (rééquilibrage alimentaire et pratique d’une activité physique), puis éventuellement sur des traitements médicamenteux. La gravité de cette maladie tient aux complications qu’elle peut engendrer sur les reins, les yeux, le cœur, les vaisseaux sanguins ainsi que les nerfs.
La régulation de la glycémie
Chez le sujet sain, malgré des variations liées aux apports alimentaires, la glycémie est maintenue entre 0,7 et 1,1 g/L notamment grâce à l’insuline, hormone hypoglycémiante sécrétée par les cellules β des îlots de Langerhans du pancréas. L’hormone se lie aux récepteurs membranaires des cellules cibles (foie, tissu adipeux et muscles squelettiques) permettant l’entrée de glucose dans ces cellules. Au sein des cellules hépatiques et musculaires, le glucose est mis en réserve sous forme de glycogène (glycogénogenèse) tandis qu’au sein du tissu adipeux, il est converti en acides gras et stocké sous forme de triglycérides. À distance des repas, le foie libère du glucose à partir du glycogène (glycogénolyse) puis, si la période de jeûne se prolonge (quelques heures), le foie met en route la néoglucogenèse permettant de fabriquer du glucose à partir de précurseurs non glucidiques (tels que le pyruvate, le lactate, le glycérol et les acides aminés). L’insuline sécrétée au moment du repas inhibe la glycogénolyse ainsi que la néoglucogenèse.
Les mécanismes cellulaires et moléculaires du diabète de type 2
Les personnes vivant avec le diabète de type 2 présentent une résistance plus ou moins sévère à l’action de l’insuline. Cette résistance, qui s’exerce au niveau des trois principaux tissus cibles de l’hormone (foie, tissu adipeux et muscles squelettiques), serait liée à des dysfonctionnements des récepteurs de l’insuline ou des voies de signalisation de celle-ci.
L’insensibilité des cellules cibles à l’insuline conduit les cellules β à en produire de plus en plus jusqu’à s’épuiser. Leur épuisement entraîne alors la diminution de la production d’insuline et l’accumulation de glucose dans le sang à l’origine de l’hyperglycémie chronique. Le glucose ne pouvant plus pénétrer dans les tissus, les cellules cibles se comportent comme dans une situation de jeûne prolongé. Ainsi, le foie se met à produire plus de glucose (principalement à partir de la néoglucogenèse) tandis qu’une lipolyse exagérée au niveau du tissu adipeux provoque une élévation du taux d’acides gras libres plasmatiques.
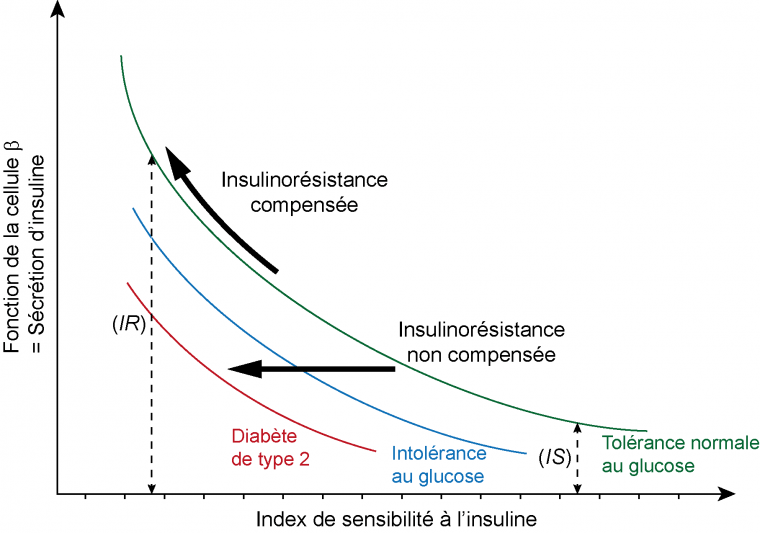
Chez l’individu prédiabétique, l’augmentation de la glycémie conduit vers un état de diabète suite à une modification de la tolérance au glucose. Chez un individu sain, la tolérance au glucose désigne la capacité à éliminer l’excès de glucose du sang, principalement grâce à l’action de l’insuline. De nombreuses études ont montré que l’évolution d’une tolérance normale au glucose vers un diabète passe par un stade d’intolérance au glucose au cours duquel la glycémie augmente mais sans atteindre la valeur d’un individu diabétique (Figure 1). À ce stade, la production d’insuline, bien que plus élevée, devient insuffisante pour empêcher l’augmentation de la glycémie 1.
Le diabète de type 2 apparaît au moment où la sécrétion d’insuline n’est plus capable de compenser la résistance à l’hormone 2. Une fois installé, ce diabète a tendance à s’aggraver au cours du temps, de manière plus ou moins rapide selon les individus.
L’index de sensibilité à l’insuline mesure la capacité des cellules à répondre à l’action de l’insuline, et donc à faire baisser la glycémie. Une amélioration ou une détérioration de l’action de l’insuline sur ses cellules cibles (foie, tissu adipeux, muscles squelettiques) est compensée par une réduction ou une augmentation de la sécrétion par les cellules β des îlots de Langerhans du pancréas. On parle d’insulinorésistance compensée lorsque le pancréas répond à l’insulinorésistance en produisant davantage d’insuline, ce qui permet de maintenir une glycémie normale. L’insulinorésistance est dite non compensée lorsque le pancréas ne parvient plus à produire suffisamment d’insuline pour compenser l’insulinorésistance. Par conséquent, la glycémie augmente, menant à une intolérance au glucose puis à un diabète de type 2.
IR : situation d’insulinorésistance, les cellules cibles sont peu sensibles à l’insuline ; IS : situation d’insulinosensibilité, les cellules cibles sont sensibles à l’insuline.
Le diagnostic de la maladie
Une des méthodes de détection de la maladie à un stade précoce est la mesure de la glycémie à jeun. Si elle se situe entre 1,10 et 1,26 g/L, le patient est considéré comme prédiabétique, et le diabète est déclaré si elle dépasse 1,27 g/L lors de deux dosages successifs. Le diagnostic peut également être posé en cas de glycémie supérieure à 2 g/L à n’importe quel moment de la journée, associée à la présence de symptômes de la maladie : polyurie (production importante d’urine) et polydipsie (soif intense) notamment 1.
D’autres critères tels que la mesure de la glycémie post-prandiale, de la glycémie provoquée ou du taux d’hémoglobine glyquée (hémoglobine sur laquelle s’est fixé du glucose) peuvent venir confirmer ou préciser le diagnostic. Les patients prédiabétiques ou même diabétiques ne présentant en général aucun signe clinique avant plusieurs années, la détection est souvent fortuite, à la suite d’un bilan sanguin ou par la découverte des complications engendrées. La détection tardive du diabète de type 2 (65 ans en France) permet à l’hyperglycémie chronique de causer des dommages importants aux organes.
Les conséquences sur la santé
L’hyperglycémie chronique abîme les vaisseaux sanguins suite à divers mécanismes physiopathologiques impliquant notamment des espèces réactives de l’oxygène, la glycation de certaines protéines ou encore l’activation de voies d’inflammation. La taille des vaisseaux atteints permet de distinguer deux grands types de complications : les microangiopathies et les macroangiopathies. Les microangiopathies concernent les capillaires et les petites artérioles, notamment au niveau des reins (protéinurie pouvant conduire à une insuffisance rénale chronique), des yeux (vision floue pouvant aller jusqu’à la cécité en l’absence de traitement) et des nerfs périphériques, au niveau des pieds principalement (douleurs, perte de sensibilité et ulcères du pied avec risque d’amputation). Les macroangiopathies touchent les artères de gros et moyen calibre, avec des atteintes au niveau du cœur (angor, infarctus du myocarde), du cerveau (risque d’accident vasculaire cérébral) et des membres inférieurs (claudication, gangrène).
Par ailleurs, une hyperglycémie maintenue pendant trop longtemps entraîne un stress oxydatif des cellules β et l’activation de mécanismes inflammatoires et de mort cellulaire programmée altérant encore davantage la capacité du pancréas à sécréter de l’insuline.
Origine multifactorielle
Une influence importante de l’environnement
L’obésité
La consommation d’une alimentation riche en sucres et en graisses, couplée à la sédentarité chronique, majore le risque de développer une obésité ou un diabète de type 2 au long terme chez les personnes ayant un terrain génétique à risque.
Ainsi, le diabète de type 2 touche environ 50 % des individus atteints d’obésité morbide, c'est-à-dire ayant un indice de masse corporelle (IMC) supérieur à 40 kg/m². Cela s’explique par l’impact de l’excès de tissu adipeux sur la sensibilité des cellules à l’insuline. En effet, l’obésité contribue à l’installation d’une insulinorésistance. Afin de compenser cette baisse d’efficacité, le pancréas augmente sa production d’insuline de façon chronique ce qui, à long terme, peut conduire à l’épuisement des cellules β et à la perte du contrôle glycémique.
Cependant, toutes les personnes obèses ne sont pas touchées par ce phénomène de perte de contrôle glycémique. En effet, certains individus peuvent présenter une adaptation pancréatique au degré d’insulinorésistance. Ainsi le pancréas est capable de répondre à cette demande accrue d’insuline par expansion de la masse des cellules β et par augmentation de l’expression d’enzymes impliquées dans la sécrétion de l’insuline 2.
Le rôle du microbiote
Le rôle du microbiote intestinal dans le développement du diabète de type 2 a été largement étudié. Les bactéries de l’intestin jouent un rôle important dans la régulation du métabolisme et de l’inflammation. Une perturbation de cet équilibre, appelée dysbiose, a été associée à des troubles métaboliques.
L’une des bactéries les plus abondantes du microbiote intestinal humain, Akkermansia muciniphila, est notamment reconnue pour ses effets bénéfiques sur la barrière intestinale et la régulation métabolique. Chez la souris, l’administration d’A. muciniphila diminue le développement de l’obésité et du diabète de type 2. Chez l’être humain, plusieurs études observationnelles ont montré que l’abondance d’A. muciniphila est souvent diminuée chez les personnes en surpoids, obèses, prédiabétiques ou diabétiques de type 2, ainsi que chez celles souffrant de maladies inflammatoires de l’intestin. Cependant, la nature exacte du lien reste à préciser : il n’est pas encore clairement établi si la dysbiose contribue au développement de ces pathologies, ou si ce sont ces dernières qui induisent la dysbiose.
Autres facteurs environnementaux
D’autres facteurs peuvent également entraîner l’apparition d’un diabète de type 2. Ainsi, certains patients sont persuadés que c’est un choc émotionnel qui a déclenché leur diabète. En réalité, les effets de ce choc émotionnel seraient plutôt indirects, en induisant de mauvaises habitudes alimentaires et une importante sédentarité qui, ensuite, engendreraient l’insulinorésistance et déclencheraient le diabète proprement dit.
L’observation de certaines familles, plus touchées par le diabète de type 2 que d’autres, plaide en faveur de causes génétiques et non uniquement environnementales pour cette maladie.
Une influence génétique
Une recherche de gènes complexe
Le taux de concordance élevé chez les jumeaux monozygotes (de 60 à 90 %) et l’agrégation familiale du diabète de type 2 suggèrent une contribution génétique importante au développement de la maladie. Le risque pour un individu de développer la maladie est d’environ 30 % si l’un de ses parents est diabétique et approche les 70 % si les deux parents le sont.
De plus, l’hétérogénéité phénotypique de la maladie et sa prévalence élevée dans la population générale suggèrent l’existence d’un très grand nombre de gènes de susceptibilité ou de prédisposition. Ces gènes n’entraînent pas directement la maladie, mais augmentent le risque de la développer, en interaction avec des facteurs environnementaux tels que l’alimentation, la sédentarité et l’obésité. Cette complexité rend délicate l’identification des gènes de susceptibilité au diabète de type 2 1.
Afin d’identifier un maximum de ces gènes, la France a mis en place une banque d’ADN de familles diabétiques. Une équipe de recherche située à l’Institut Pasteur de Lille vient de publier des résultats issus de l’analyse des génomes d’un panel de plus de 74 000 individus issus d’études françaises, anglaises et américaines afin d’identifier les mutations associées au diabète de type 2. Parmi les gènes associés à cette maladie, certains participent à la régulation de la sécrétion de l’insuline ou à son action. Cependant, il s’est avéré que l’association entre un locus donné et la susceptibilité à la maladie varie d’un groupe ethnique à l’autre et d’un individu à un autre, hormis pour le gène de la calpaïne 10, une protéase qui semble significativement associée au diabète dans plusieurs populations.
Quelques gènes de susceptibilité
Les protéines de la famille des calpaïnes sont des protéases à cystéines. L’un des membres de cette famille multigénique, le gène codant la calpaïne 10 (CAPN10), a été le premier gène de susceptibilité associé au diabète de type 2 2.
Le gène CAPN10 est un gène complexe, formé de 12 exons, porté par le bras long du chromosome 2. Ce gène peut produire, par épissage alternatif, huit protéines différentes (calpaïne 10a, b, c, d, e, f, g, et h). La calpaïne 10 présente une expression ubiquitaire et est en particulier exprimée par les cellules β pancréatiques, le foie et le muscle squelettique.
De nombreuses études ont montré qu’une combinaison d’allèles comprenant l’association de trois polymorphismes introniques du gène CAPN10 (UCSNP-43, -19 et -63) est associée à un risque accru de diabète de type 2 chez certaines populations mais n’a pas d’impact sur d’autres (risque plus important que si un seul des polymorphismes est présent). Ceci plaide en faveur d’une origine multifactorielle du diabète de type 2, dont le développement met en jeu l’intervention d’autres gènes ainsi que de facteurs environnementaux. La fonction exacte de la calpaïne 10 reste à déterminer, mais elle a été impliquée à la fois dans la translocation du transporteur de glucose de type 4 (GLUT4) vers la membrane cellulaire, dans la régulation de la sécrétion d’insuline et dans l’apoptose des cellules β du pancréas 34. GLUT4 est une protéine transmembranaire principalement exprimée dans les tissus sensibles à l’insuline, tels que les muscles squelettiques et le tissu adipeux. Son rôle principal est de faciliter l’entrée du glucose dans les cellules.
Lorsque la glycémie augmente au-delà de la valeur de 1 g/L, les cellules β pancréatiques libèrent de l’insuline. L’hormone se lie aux récepteurs présents à la surface des cellules des tissus sensibles à l’insuline et cela déclenche une cascade de signalisation intracellulaire. Sous l’influence de cette cascade de signalisation, des vésicules contenant les transporteurs GLUT4 sont acheminées vers la membrane plasmique, facilitant la pénétration de glucose dans les cellules, et par conséquent la baisse de la glycémie. Le transport de ces vésicules implique l’actine sous-membranaire, qui est reconfigurée par la calpaïne 10.
Des travaux ont montré que la diminution ou la suppression de l’expression de CAPN10 empêchait l’absorption de glucose dans le tissu adipeux et le muscle squelettique. Cette diminution s’explique par l’inhibition de la reconfiguration de l’actine induite par la calpaïne 10 qui entrave l’acheminement de GLUT4 vers la membrane plasmique et donc l’absorption du glucose 567.
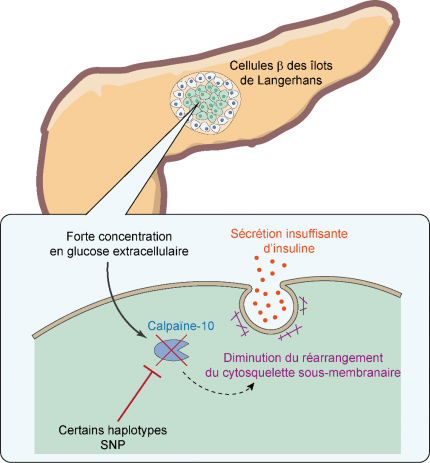
La calpaïne 10 joue un rôle majeur dans la sécrétion d’insuline par les cellules β pancréatiques. Cette fonction est altérée pour divers polymorphismes mononucléotidiques (SNP) du gène CAPN10, dont le SNP-43.
Par ailleurs, divers travaux ont montré que la calpaïne 10 contribuait à la libération d’insuline dans les cellules β pancréatiques. Pour divers polymorphismes mononucléotidiques (SNP), notamment le SNP-43, cette fonction est altérée. Cela s’explique par une inhibition d’un réarrangement du cytosquelette (Figure 2) 1.
Les calpaïnes, y compris la calpaïne 10, sont activées par des augmentations du calcium intracellulaire. Or, dans un contexte de stress oxydatif ou d’inflammation tel qu’observé dans le diabète de type 2, les niveaux élevés de calcium intracellulaire au niveau les cellules β du pancréas peuvent déclencher l’activation excessive de la calpaïne 10. Ceci active des cascades de signalisation pro-apoptotiques conduisant à la mort des cellules β entraînant une diminution de la capacité du pancréas à produire de l’insuline et contribuant ainsi à la progression du diabète de type 2 23.
Traitements
Modification de l’hygiène de vie
En cas de diabète de type 2, le traitement prioritaire et de référence consiste en la modification de l’hygiène de vie du patient, incluant une alimentation équilibrée et la pratique d’une activité physique régulière couplées à une perte de poids, si nécessaire.
Ces mesures peuvent être suffisantes pour réguler la glycémie. Dans le cas contraire, des traitements médicamenteux peuvent être employés.
Traitements médicamenteux
Il existe différents médicaments antidiabétiques, qui peuvent être administrés seuls ou en association. Le premier médicament employé est la metformine, dont la principale cible est l’AMPK (protéine kinase activée par l’AMP), une enzyme clé dans la régulation du métabolisme énergétique. L’AMPK diminue la production hépatique de glucose, en inhibant les enzymes impliqués dans la néoglucogenèse. La diminution de la glycémie qui en résulte entraîne l’augmentation de la sensibilité à l’insuline.
En deuxième intention, d’autres options thérapeutiques sont envisageables :
- stimuler la production d’insuline au niveau du pancréas (sulfamides hypoglycémiants et glinides) ;
- retarder l’absorption des glucides après les repas (inhibiteurs des alpha-glucosidases) ;
- ralentir la vidange gastrique, limiter l’appétit et stimuler la sécrétion d’insuline, mais uniquement en cas d’élévation de la glycémie (agonistes du récepteur du glucagon-like peptide-1, GLP-1) ;
- bloquer la réabsorption du glucose au niveau du rein (inhibiteurs de SGTL2).
Malgré la mise en place des différents traitements, la glycémie de certains patients reste parfois difficile à équilibrer. Cela peut s’expliquer par une alimentation insuffisamment équilibrée, par l’épuisement progressif de la capacité des cellules pancréatiques à sécréter de l’insuline ou encore par l’impossibilité d’intégrer une activité physique, même légère (marcher un peu plus chaque jour peut avoir un impact positif sur le contrôle du diabète).
Les traitements du diabète de type 2 visent à faire baisser la glycémie et à réduire le risque de complications à long terme, notamment cardiovasculaires. Certains médicaments autrefois largement utilisés, comme les sulfamides hypoglycémiants, le sont beaucoup moins aujourd’hui car ils provoquent davantage d’hypoglycémies et n’ont pas montré de bénéfice cardiovasculaire. À l’inverse, les agonistes du GLP-1 entraînent peu d’hypoglycémies, favorisent la satiété et apportent une protection cardiovasculaire. Les inhibiteurs du cotransporteur sodium-glucose de type 2 (SGLT2), ne majorent pas non plus le risque d’hypoglycémie, améliorent le pronostic en cas d’insuffisance cardiaque et protègent la fonction rénale.
Lorsque ces traitements ne suffisent plus, une insulinothérapie peut être nécessaire. Elle consiste à s’injecter de l’insuline, comme dans le diabète de type 1. Il existe aujourd’hui plusieurs types d’insulines, à action plus ou moins rapide ou prolongée, ce qui permet d’adapter le traitement à chaque patient. Étant donné le caractère évolutif de la maladie, un suivi régulier est indispensable pour ajuster la prise en charge au fil du temps 1.
Les enjeux de la recherche
La recherche sur le diabète de type 2 se poursuit avec des études visant à comprendre l’étiologie et la physiopathologie de la maladie : mécanismes de la résistance à l’insuline, origine des troubles métaboliques, impact du microbiote, rôles de variations génétiques…
D’autres recherches portent sur les moyens de prévention mais également sur la mise au point de traitements pharmacologiques (élaboration de nouveaux médicaments et thérapies combinées) ainsi qu’à la gestion des complications (étude des relations entre le diabète de type 2 et les maladies cardiovasculaires, recherche sur la néphropathie diabétique et les approches pour retarder son apparition).
Enfin, une dernière approche se concentre sur l’aspect psychosocial et sociétal du diabète de type 2 : elle s’intéresse à l’impact psychologique de la maladie sur les patients, aux moyens d’améliorer leur qualité de vie et aux programmes éducatifs pour mieux gérer la maladie, tout en prenant en compte le rôle du mode de vie et des politiques de santé publique dans la prévention de cette affection.