Des médicaments populaires et efficaces pour le traitement de l’obésité et des diabètes.
Au cours de l’année écoulée, des médicaments amaigrissants comme Ozempic, Wegovy, Mounjaro et d’autres ont fait la une des médias et sont devenus des noms familiers aux États-Unis. Si l’intérêt pour ces médicaments est récent, la recherche dans ce domaine ne l’est pas. Ils appartiennent tous à une classe de molécules, de nature peptidique, appelées agonistes du récepteur du GLP-1 (pour glucagon-like peptide-1 en anglais), qui font l’objet d’études depuis plus de deux décennies. Ces médicaments imitent un peptide naturel produit par l’organisme appelé GLP-1, une molécule qui joue un rôle clé dans la régulation de l’appétit et du métabolisme, mais qui est dégradée en quelques minutes dans l’organisme par certaines enzymes.
Améliorer une toxine de lézard
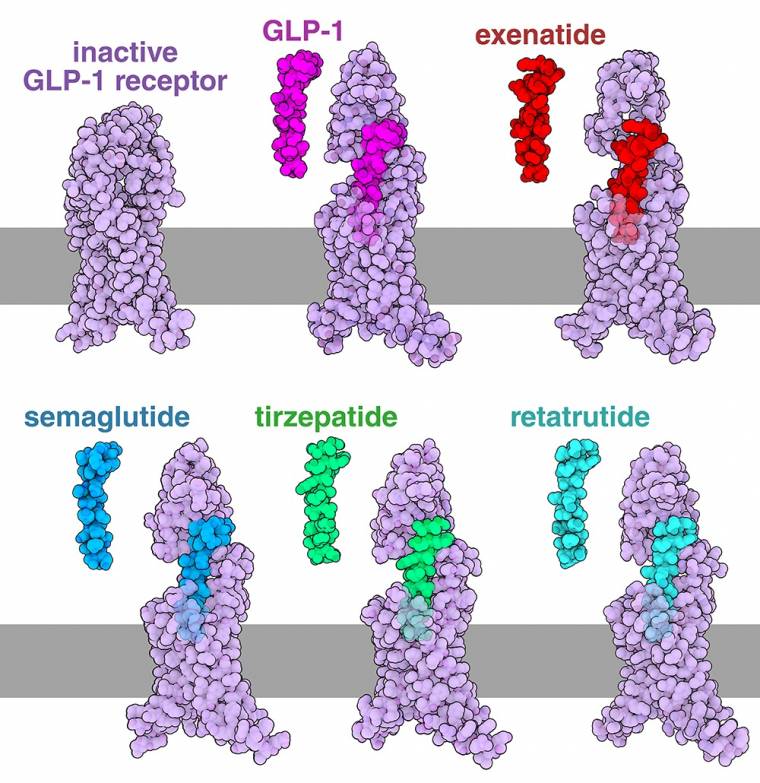
Les agonistes du récepteur du GLP-1 ont vu le jour dans un endroit improbable : la bouche d’un lézard. Un peptide découvert dans la salive du monstre de Gila, appelé exendine-4, imite l’action du GLP-1 et a servi de base à la synthèse d’un médicament pour le traitement du diabète de type 2, l’exénatide (commercialisé sous le nom de Byetta). L’exénatide (représenté en rouge sur la figure 1, entrée de la banque de données des protéines (PDB) 7LLL), a été le premier agoniste du récepteur GLP-1 approuvé par l’Agence américaine des produits alimentaires et médicamenteux (FDA, Food and Drug Administration en anglais). Il partage seulement un peu plus de 50 % d’identité de séquence avec GLP-1, mais possède une structure tridimensionnelle similaire et il est capable d’activer le récepteur GLP-1, tout en évitant une dégradation protéolytique rapide 1.
Le récepteur du GLP-1 est représenté en violet. GLP-1 est représenté en rose, tandis que les agonistes comme l’exénatide, le sémaglutide, le tirzépatide ou le rétatrutide sont représentés respectivement en rouge, bleu, vert et turquoise. La membrane plasmique est représentée en gris.
Le récepteur GLP-1, qui fait partie d’une grande classe de récepteurs couplés aux protéines G, subit une série de changements conformationnels lorsqu’il est activé. En l’absence d’agoniste, le domaine extracellulaire du récepteur est fermé et interagit avec le domaine transmembranaire (entrée PDB 6LN2). Du côté intracellulaire, la structure est compacte, stabilisée par des interactions entre les acides aminés de différentes hélices alpha 1. Lors de la liaison du GLP-1 (représenté sur la figure 1 en rose, entrée PDB 6X18), le domaine extracellulaire se déplace vers le haut et accueille le ligand, ce qui provoque également une ouverture du côté intracellulaire du récepteur 2. Cela permet la liaison et l’activation d’une protéine G (non représentée), qui à son tour pousse l’une des hélices transmembranaires du récepteur vers l’extérieur. Il en résulte une perturbation des contacts stabilisateurs au sein du récepteur et le déclenchement d’une signalisation en aval qui influence l’appétit et le métabolisme.
Après le succès de l’exénatide, les scientifiques ont travaillé à l’amélioration des agonistes du récepteur GLP-1 afin de les rendre plus stables, plus efficaces et plus faciles à administrer. L’un des produits les plus réussis grâce à ces travaux est le sémaglutide (entrée PDB 7KI0), mieux connu sous ses noms de marque Ozempic, Rybelsus et Wegovy. Le sémaglutide possède des substitutions et des modifications qui le rendent plus résistant au clivage protéolytique et qui ralentissent son élimination par l’organisme, ce qui permet une administration hebdomadaire (en comparaison, la formulation originale de l’exénatide nécessitait deux injections quotidiennes) 3.
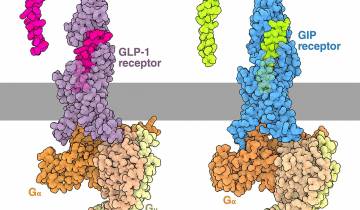
Une autre avancée majeure a été réalisée avec le tirzépatide (entrée PDB 7FIM), commercialisé sous les noms Mounjaro et Zepbound. Le tirzépatide est un agoniste double qui active à la fois le récepteur du GLP-1 et le récepteur du peptide insulinotrope dépendant du glucose (GIP), étendant ainsi ses effets au-delà de ceux des médicaments précédents 4. Il a été conçu en combinant les caractéristiques du GLP-1 et du GIP, et il produit, dans le récepteur GLP-1 activé, des réarrangements structuraux très similaires à ceux du ligand naturel.
Le rétatrutide (entrée PDB 8YW3) est un peptide pouvant servir de médicament qui n’est pas encore approuvé par la FDA. Il s’agit d’un agoniste triple ciblant à la fois le récepteur GLP-1, le récepteur GIP et le récepteur du glucagon 5. En incluant l’activité du récepteur du glucagon, le rétatrutide supprime non seulement l’appétit, mais possède également d’autres effets sur le métabolisme. Les essais cliniques suggèrent que ce mécanisme combiné entraîne une perte de poids plus importante que celle obtenue avec le sémaglutide ou le tirzépatide. Des études structurales montrent que le rétatrutide est capable de ce triple agonisme car il interagit avec des acides aminés communs dans les trois récepteurs.
De petites molécules mimétiques
Malgré le succès des agonistes du récepteur GLP-1 à base de peptides, ceux-ci présentent des inconvénients importants. Les peptides étant dégradés dans le tube digestif, la plupart de ces médicaments doivent être injectés. Une formulation orale du sémaglutide, commercialisée sous le nom de Rybelsus, peut être utilisée pour le traitement du diabète de type 2, mais elle présente une biodisponibilité très faible, des effets limités sur la perte de poids et elle est associée à des effets secondaires importants comme des nausées. Les médicaments à base de peptides doivent également être conservés au réfrigérateur pour éviter leur dégradation et leur fabrication est plus coûteuse que celle des médicaments à base de petites molécules. Ces défis ont stimulé les efforts visant à créer des agonistes non peptidiques du récepteur GLP-1, pouvant être pris par voie orale. Cependant, la découverte de telles molécules est difficile, car elles doivent reproduire les effets des grands peptides qui stabilisent le récepteur actif grâce à de nombreuses interactions dispersées. Malgré tout, des candidats prometteurs ont fait leur apparition.
L’orforglipron (jaune) et le danuglipron (orange) sont de petites molécules capables de se fixer au récepteur du GLP-1 (violet). La membrane plasmique est représentée en gris.
L’orforglipron (entrée PDB 6XOX) en est un exemple. Il s’agit d’une petite molécule qui se lie au récepteur GLP-1 à un emplacement unique, en hauteur dans le faisceau d’hélices α du récepteur. Par rapport aux agonistes peptidiques, ce médicament interagit avec un ensemble différent de résidus du récepteur, tout en parvenant à activer ce dernier 1. Des études ont montré que les signaux en aval résultant de la liaison entre l’orforglipron ou le GLP-1 d’une part et le récepteur au GLP-1 d’autre part sont similaires mais distincts. L’orforglipron fait actuellement l’objet d’essais cliniques de phase 3 en tant que traitement oral à prise unique quotidienne contre l’obésité, le diabète de type 2, l’apnée obstructive du sommeil et l’hypertension.
Un autre candidat, le danuglipron (PDB 6X1A), a été conçu pour occuper le cœur du récepteur, chevauchant la position normalement occupée par une extrémité du GLP-1 2. La liaison du danuglipron stabilise le récepteur dans une conformation unique, différente de celles observées lors de la liaison du GLP-1 ou de l’orforglipron. Bien que les premières études aient été encourageantes, Pfizer a interrompu le programme en 2025 après l’apparition de cas de lésions hépatiques induites par le médicament au cours des essais cliniques.
La liaison au récepteur GLP-1 de médicaments à base de peptides ou de petites molécules
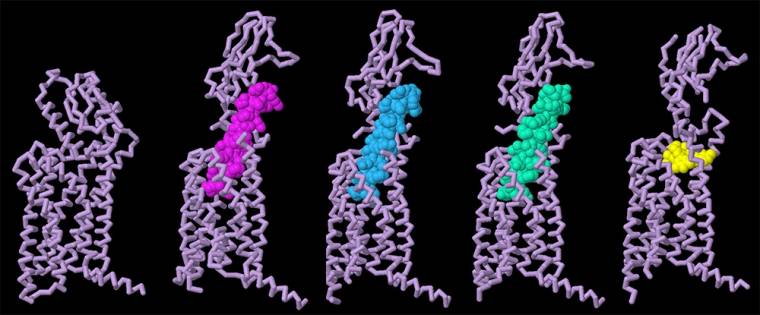
Alors que les agonistes peptidiques du récepteur GLP-1 se lient tous au récepteur GLP-1 de manière similaire, l’orforglipron est beaucoup plus petite et présente beaucoup moins d’interactions 1. Vous pouvez examiner de plus près comment le GLP-1 (entrée PDB 6X18), le sémaglutide (entrée PDB 7KI0), le tirzépatide (entrée PDB 7FIM) et l’orforglipron (entrée PDB 6XOX) sont capables de stabiliser la forme active du récepteur GLP-1, et ainsi comparer ces structures à celle du récepteur GLP-1 inactif (PDB 6LN2) en vous rendant sur la page de l’article d’origine (en anglais), et en cliquant sur l’onglet JSmol de la section Exploring the structure.
Le récepteur du GLP-1 (violet) est représenté sous sa forme libre (à gauche) ou fixée à différentes molécules : le GLP-1 (en rose), la sémaglutide (en bleu), la tirzépatide (en turquoise) et l’orforglipron (en jaune).
Pour aller plus loin
-
Explorez le rôle du GLP-1 et du GIP, des molécules connues sous le nom d’incrétines en lisant l’article de la molécule du mois sur les incrétines disponible sur le site Planet-Vie.
-
Découvrez comment la glycémie est régulée par l’insuline et le récepteur de l’insuline, et comment fonctionnent les insulines de synthèse en lisant ces trois anciens articles de la molécule du mois : Insulin, Insulin Receptor et Designer Insulins. Vous trouverez aussi sur le site Planet-Vie : le diabète de type 1.
-
Vous pouvez en apprendre davantage sur les protéines G et les récepteurs couplés aux protéines G en relisant d’anciens articles de la molécule du mois et de la base de données sur les protéines. Vous pouvez aussi apprendre à modéliser un récepteur couplé aux protéines G avec du papier.
Ce texte correspond à la traduction par Cédric Bordi de l’article Molecule of the Month : GLP-1 Receptor Agonists 1 écrit par Janet Iwasa en novembre 2025 sur le site PDB-101, le portail éducatif de la base de données sur les protéines (PDB).