Pourquoi Saccharomyces cerevisiae est la levure fermentaire ? Comment obtient-on du (bon) vin à partir du raisin ? Qu’apporte le houblon à la bière ? La mise en parallèle de notions de biologie et de biochimie avec les pratiques de vinification et de brassage permet de mieux comprendre l’enjeu de chacune des étapes de fabrication de ces boissons, tout en explorant des domaines scientifiques variés tels que la microbiologie, la biologie végétale ou la biochimie.
Microbiologie et métabolisme dans la production de boissons alcoolisées
La production de vin et de bière repose sur la transformation d’ingrédients de base différents : jus de raisin dans le premier cas, orge malté mélangé à de l’eau dans le second. Cependant, leurs mécanismes de transformation présentent des points communs car ils sont assurés par des micro-organismes en partie identiques, dont la levure de bière Saccharomyces cerevisiae.
De nombreux autres produits alcoolisés (rhum, saké, tequila…) ont également des fabrications très proches de celle du vin et de la bière mais diffèrent par la nature et le traitement des matières premières mises à fermenter, comme nous le verrons en conclusion.
Caractéristiques des levures brassicoles et vinicoles
Les levures sont des unicellulaires eucaryotes appartenant au règne des Fungi et à la division des Ascomycota. Celles utilisées pour la fermentation alcoolique sont du genre Saccharomyces : la « levure de bière » (également appelée « levure de boulangerie ») Saccharomyces cerevisiae en immense majorité, et certains de ses hybrides domestiqués tels que S. pastorianus (= S. carlsbergensis, issue d’une hybridation avec la levure cryotolérante S. eubayanus) utilisée dans les bières de type lager, et S. bayanus (hybride de S. cerevisiae, S. eubayanus et S. uvarum) pour la fabrication du cidre [1, 2].
Ces levures peuvent floculer, c’est-à-dire former des amas, soit spontanément, soit suite à l’ajout de divers composés (présentés plus loin). Ces amas sédimentent et permettent la clarification du liquide [3].
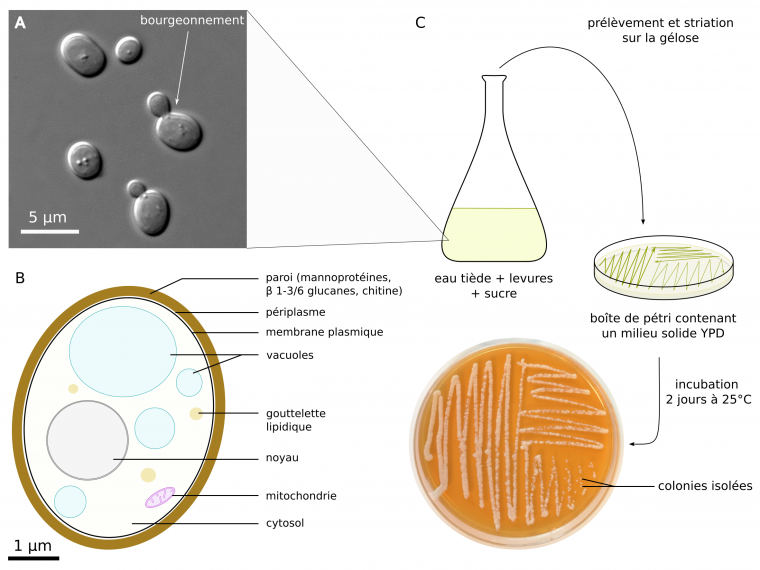
Les levures sont facilement cultivables et observables au microscope (Figure 1). Leur reproduction est principalement asexuée, par mitose et bourgeonnement d’une cellule fille à partir d’une cellule mère ce qui leur vaut également le nom de « levures bourgeonnantes ».
A : photographie d’une suspension de levures observée au microscope à contraste de phase. B : schéma d’une cellule de S. cerevisiae. C : méthodes de culture en milieu liquide et isolement de colonies sur milieu solide. Composition du milieu YPD solide (en % massique) : 1,5 % d'agar, 1 % d'extrait de levures, 2 % de peptone, 2 % de glucose. Un protocole de culture de levures est disponible sur le site de l'APBG (association des professeurs de biologie géologie).
Crédits : A : Masur, domaine public, Wikimedia ; B et C : Mathias Penot, CC BY-SA.
La fermentation des levures dans la production de boissons alcoolisées
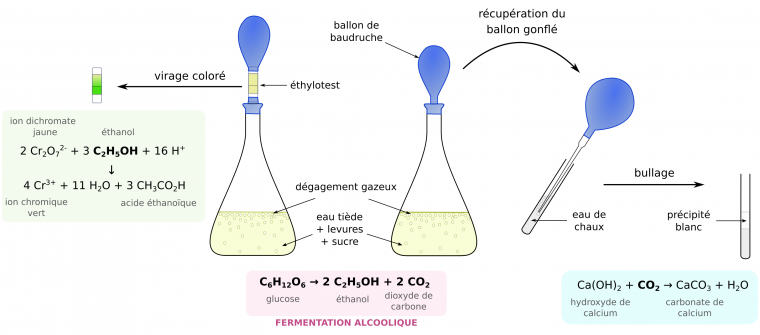
Le métabolisme fermentaire de Saccharomyces cerevisiae et la nature de ses produits, éthanol et dioxyde de carbone, peuvent facilement être mis en évidence (Figure 2).
Des levures Saccharomyces cerevisiae sont mises en suspension dans de l’eau tiède et sucrée. Après quelques dizaines de minutes, on observe un virage coloré de l’éthylotest placé à la sortie de l’erlenmeyer. Par ailleurs, le gaz contenu dans le ballon trouble l’eau de chaux. La réalisation d’expériences témoins (sans sucre ou sans levures) permet de déduire que les levures consomment des sucres et produisent de l’éthanol et du dioxyde de carbone, avec pour équation-bilan : C6H12O6 → 2 C2H5OH + 2 CO2
Des exemples de protocoles de mise en évidence de la production d'éthanol sont disponibles sur le site Bio-tremplins.
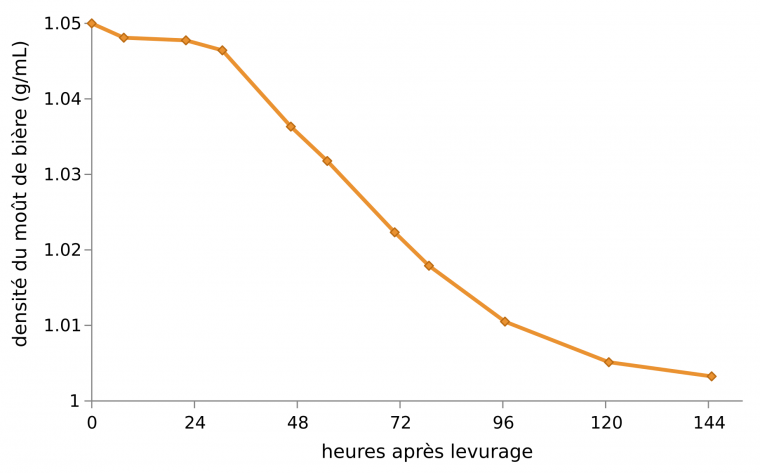
En vinification et en brasserie, le suivi de cette fermentation alcoolique se fait par mesure de la densité du moût1, qui est directement liée à sa concentration en sucres. Elle est déterminée à l’aide d’un densimètre gradué (densité fixe) qui flotte dans le liquide (densité à mesurer) : plus la fermentation est avancée, moins le moût est sucré, moins il est dense et plus le densimètre coule (Figure 3).
Il est possible de calculer le taux d’alcool de la bière produite en utilisant la formule : $$\dfrac{\textrm{densité initiale} - \textrm{densité finale}}{\textrm{densité initiale}} \times 1,33 \times 100$$Ici la bière produite est à 6,2 °, donc 100 mL de bière contiennent 6,2 mL d’éthanol pur.
L’atténuation représente la proportion des sucres du moût consommés par la fermentation, exprimée en %. Sa formule est : $$\dfrac{\textrm{densité initiale} - \textrm{densité finale}}{\textrm{densité initiale} - 1} \times 100$$Elle vaut ici 93,5 % à la dernière mesure. L’atténuation maximale procurée par les souches vendues par les levuristes est une caractéristique essentielle à connaître pour pouvoir prévoir la quantité finale en sucres et en éthanol de la boisson.
Les produits fermentaires rendent le milieu peu propice au développement d’autres micro-organismes que les levures : le CO2 participe à son acidification (le pH des vins et des bières est généralement compris entre 3 et 6 ; cette acidité est également due à la présence d’acides organiques), et l’éthanol est un biocide à large spectre. Or les levures sont acidophiles et résistantes à plus de 10° d’éthanol [1], leur métabolisme représente donc une véritable arme de colonisation. Néanmoins, cette résistance n’est pas illimitée ; la fermentation s’arrête donc au-delà d’un certain seuil de concentration en éthanol, variable selon la souche employée, et ce même s’il reste des sucres fermentescibles dans le milieu (voir les parties 2.3 et 3.4).
Certains micro-organismes indésirables peuvent toutefois se développer dans les milieux de fermentation et conduire à une diminution de leur qualité, par la production d’arômes indésirables ou de toxines. Par exemple, la levure Brettanomyces bruxellensis est responsable d’odeurs de cuir et de gouache dans le vin ; la mère du vinaigre (biofilms d’Acetobacter et de Gluconobacter) s’y développe en surface et produit de l’acide acétique ; des lactobactéries contaminantes donnent un goût aigre à la bière, etc [4]. Ces contaminations sont évitées par divers traitements, comme l’ajout de dioxyde de soufre SO2 en vinification (sulfitage) ou à l’aide de procédures de désinfection et de stérilisation, essentielles en brasserie.
Exploration des voies métaboliques en jeu
La fermentation alcoolique
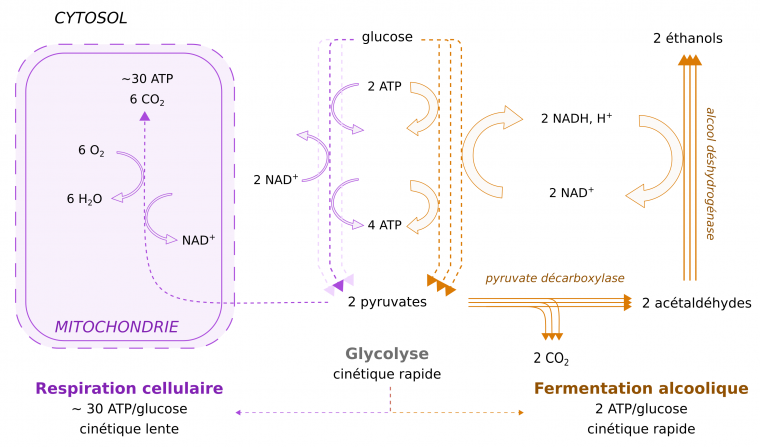
Le glucose présent dans le moût subit la glycolyse dans le cytosol des levures. Cette réaction aboutit à la production d’ATP, de coenzymes réduits NADH,H+, ainsi que de pyruvate. La fermentation alcoolique correspond à la décarboxylation du pyruvate, qui libère du CO2, et à la réduction de l’acétaldéhyde ainsi produit en éthanol, couplée à la réoxydation des coenzymes en NAD+. C’est par cette voie que les levures produisent préférentiellement leur ATP, même en conditions aérobies, lorsque le glucose est présent en quantité importante. Pourtant le rendement de la fermentation alcoolique, qui ne produit que deux molécules d’ATP par molécule de glucose est bien inférieur à celui de la respiration cellulaire (Figure 4) [5]. Ce désavantage apparent est contrebalancé par le fait que la vitesse de production d’ATP par fermentation est environ 100 fois plus rapide que par la voie respiratoire, en particulier du fait de la concentration importante des enzymes glycolytiques et fermentaires dans le cytosol. Ainsi, même si le rendement énergétique de la fermentation est environ 15 fois plus faible que celui de la respiration, cette voie métabolique permet de produire plus d’ATP [5].
Le nombre de flèches schématise la vitesse des réactions, la largeur des flèches pleines schématise la quantité de produits créés par unité de temps ; traits pointillés : succession de réactions enzymatiques d’une voie métabolique ; traits pleins : réaction enzymatique simple avec le nom de l’enzyme en italique. L’oxydation du NADH,H+ maintient un ratio [NAD+]/[NADH,H+] stable, ce qui permet la conservation de conditions rédox compatibles avec le bon fonctionnement de la cellule [5].
Il est important de noter que le glycérol joue un rôle important dans la balance rédox durant le métabolisme fermentaire de S. cerevisiae [29]. La fermentation alcoolique a un bilan neutre en terme rédox puisque la production d’éthanol consomme le NADH produit par la glycolyse (Figure 4). Or, d’autres réactions métaboliques produisent du NADH qui, en conditions anaérobies, ne peut être consommé par la chaîne respiratoire mitochondriale. L’excès de NADH est alors utilisédans le cytosol pour réduire le dihydroxyacétone-phosphate dérivé de la glycolyse, produisant ainsi du glycérol (Figure 8). Cette molécule contribue également à la protection osmotique des levures, en augmentant la pression osmotique du cytosol face aux fortes concentrations en sucres du moût qui rendent ce milieu hypertonique. De plus, le glycérol est un agent important pour la texture du vin (Figure 8).
Les fermentations
Le terme de « fermentation » désigne toutes les voies productrices d’ATP conduisant à l’oxydation incomplète d’un substrat carboné. Le NADH,H+ produit est alors utilisé pour réduire le pyruvate ou l’un de ses dérivés, sans utilisation d’O2 ou d’une chaîne de transporteurs d’électrons.
Il existe une grande diversité de voies fermentaires (majoritairement bactériennes), dont certaines produisent de l’éthanol et du CO2. C’est le cas de la fermentation alcoolique, abordée ici, mais également de la fermentation dite « hétérolactique », qui produit en quantités équimolaires du lactate, de l’éthanol et du CO2 [6].
Les préférences métaboliques de S. cerevisiae
Saccharomyces cerevisiae est une levure de type aéro-anaérobie facultative : elle peut se développer en l’absence de dioxygène, mais la présence de ce gaz permet un meilleur développement. En effet, chez S. cerevisiae le dioxygène est impliqué dans la synthèse des stérols membranaires et de coenzymes lorsque ces composés sont absents du milieu [7]. C’est la raison pour laquelle des phases d’oxygénation modérées (quelques mg/L d'O2 dissout au maximum) sont utilisées en vinification et en brassage. Ces stérols membranaires, dont l’ergostérol, confèrent notamment aux levures une meilleure résistance à l’éthanol et donc une meilleure viabilité en fin de fermentation [30].
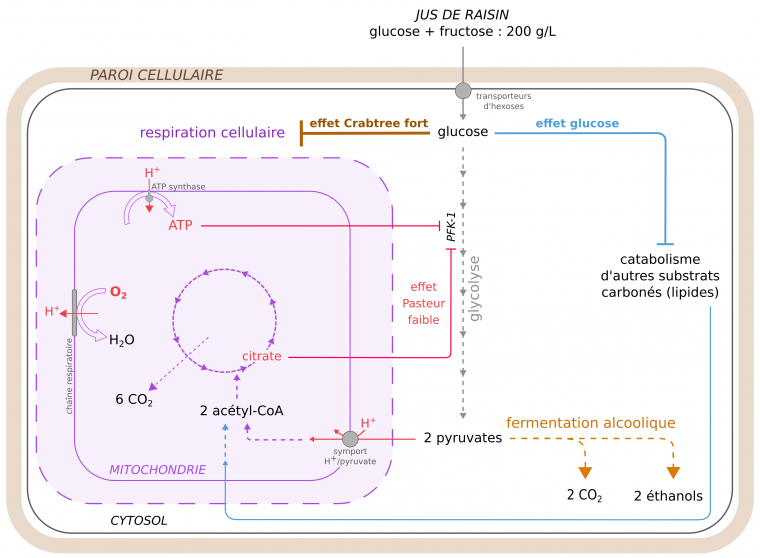
La fermentation alcoolique est la voie préférentielle de production d’ATP chez S. cerevisiae. Elle a lieu lorsque la levure est en anaérobiose ou lorsqu’elle est en aérobiose mais en présence d’une forte concentration de glucose, ce qui est le cas dans le moût de raisin et de bière. La respiration cellulaire n’est active qu’à faible concentration en glucose et à forte concentration en O2. Trois phénomènes contrôlent l’engagement métabolique vers la respiration ou vers la fermentation : les effets Pasteur, Crabtree et glucose (Figure 5).
L’effet Pasteur (faible chez S. cerevisiae) est le mécanisme par lequel l’O2 favorise la respiration mitochondriale aux dépens de la fermentation [1, 5]. Cet effet s’explique par deux mécanismes. D’une part, certains intermédiaires et produits de la respiration freinent la glycolyse. En particulier, l’ATP et le citrate inhibent l’activité de l’enzyme glycolytique PFK-1 (phosphofructokinase 1), aboutissant à une réduction du flux glycolytique, et donc à une plus faible production de pyruvate. D’autre part, la force proton-motrice générée par le fonctionnement de la chaîne respiratoire permet l’import du pyruvate depuis le cytosol vers la mitochondrie, ce qui prive la pyruvate décarboxylase de son substrat et limite de fait la fermentation [5]. Ainsi, plus la respiration augmente, moins la glycolyse produit de pyruvate, et plus ce rare pyruvate est mobilisé pour la respiration mitochondriale. Un faible effet Pasteur permet à S. cerevisiae d’utiliser le dioxygène présent dans le moût pour son anabolisme (dont la synthèse de stérols membranaires) et se multiplier, notamment au début de l’étape de fermentation.
L’effet Crabtree (fort chez S. cerevisiae), correspond quant à lui au fait qu’une forte concentration de glucose inhibe la respiration mitochondriale [1]. Ses mécanismes sont encore discutés mais pourraient notamment impliquer l’inhibition des complexes III et IV de la chaîne respiratoire par le fructose-1,6-bisphosphate produit en grande quantité par la glycolyse lorsque le glucose est abondant [28]. Les levures colonisent ainsi rapidement les milieux riches en sucres grâce à la grande quantité d’ATP produite par fermentation, et les « stérilisent » grâce à leurs produits fermentaires.
Enfin l’effet glucose est l’effet par lequel une forte concentration de glucose inhibe l’utilisation d’autres substrats énergétiques (acides gras notamment), ce qui limite l’alimentation de la respiration mitochondriale par l’acétyl-CoA [8].
Durant la vinification et le brassage, les conditions permettant la respiration (présence de dioxygène et faible concentration en glucose) ne sont généralement pas réunies, ce qui favorise une forte activité fermentaire des levures au sein des moûts. Les caractéristiques métaboliques de S. cerevisiae (faible effet Pasteur, fort effet Crabtree) ont probablement été accentuées au cours de sa domestication.
En rouge : quelques acteurs de l’effet Pasteur ; flèches pointillées : voies métaboliques ; PFK-1 = enzyme phosphofructokinase 1.
La « fermentation » malolactique des bactéries du vin
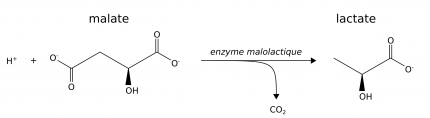
L’arôme de pomme non mûre du malate disparaît au profit de celui plus doux de petit-lait du lactate. Cette réaction contribue également à l’augmentation pH du vin.
En parallèle de la fermentation alcoolique réalisée par les levures, la production de vins rouges et de certains blancs met en jeu la « fermentation » malolactique. Elle correspond simplement à la décarboxylation du malate du raisin en lactate. Il ne s’agit donc pas d’une fermentation stricto sensu et l’expression « conversion malolactique » devrait être préférée (Figure 6) [5].
La bactérie Oenococcus oeni est principalement responsable de cette réaction, mais dans de rares cas Lactobacillus plantarum est utilisée en inoculation exogène pour la vinification [4]. La croissance de ces bactéries se produit dès la fin de la fermentation alcoolique, lorsque la population de levures commence à décliner : une véritable succession écologique se produit durant la vinification.
Le suivi de la fermentation malolactique se fait facilement par chromatographie sur couche mince.
Les métabolites secondaires et la production d’arômes
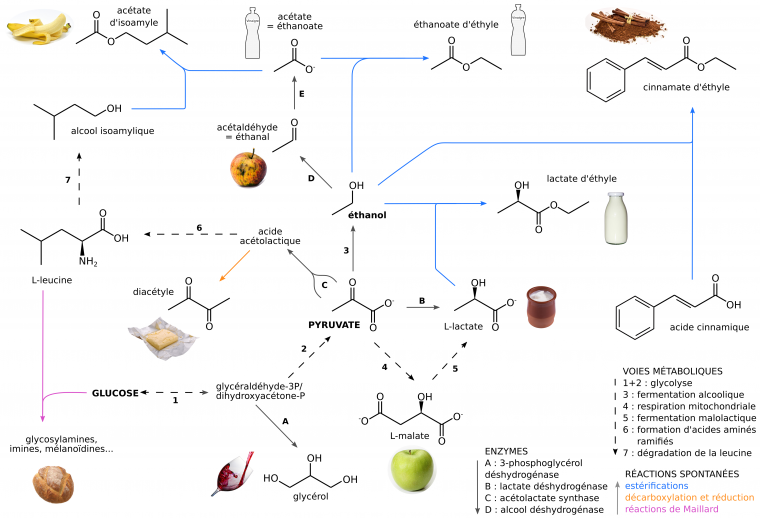
Le pyruvate occupe une place centrale dans les réseaux métaboliques, et certains de ses dérivés présentent des propriétés organoleptiques (Figure 8). La plupart de ces métabolites sont produits par les levures au cours de la fermentation puis durant son achèvement, qui correspond aux étapes d’élevage du vin (voir partie 2.2) ou de la « fermentation secondaire » de la bière (voir partie 3.4). Ils varient en quantité et en diversité en fonction des souches employées et des conditions de fermentation (température, oxygénation, nutriments disponibles…). Ces arômes sont les produits du métabolisme carboné et azoté des levures, mais peuvent également être issus de la simple hydrolyse de composés présents dans le milieu.
Ces composés sont volatils (car faiblement solubles) et provoquent des sensations gustatives, dépendantes de leur concentration et du contexte de dégustation [4]. Leur oxydation tend à créer des arômes de noix, de miel et de pruneau souvent indésirables dans les vins et les bières, d’où l’utilisation de bouteilles colorées et hermétiques permettant de réduire le processus de photo-oxydation [4].
Acétaldéhyde : pomme trop mûre (métabolite toxique); acétate d’isoamyle : banane ; cinnamate d’éthyle : cannelle ; diacétyle : arômes beurrés ; éthanoate et éthanoate d’éthyle : vinaigre ; glycérol : sensation de « gras » du vin ; lactate : petit lait, yaourt ; lactate d’éthyle : arômes crémeux ; malate : pomme peu mûre ; composés issus des réactions de Maillard : arômes et colorations de croûte de pain, miel, caramel, goûts lourds et épais.
Les réactions de Maillard sont des réactions chimiques complexes, qui débutent par la condensation d’un sucre réducteur (par son groupement carbonyle) et d’une amine (généralement un acide aminé ou une protéine), et se poursuivent par des réarrangements intramoléculaires, des déshydratations ou d’autres réactions intermoléculaires.
Les enzymes et les voies métaboliques ont été recherchées en utilisant la base de données Metacyc, les vignettes proviennent de Pixabay.
Biologie de la vigne et du vin
Caractéristiques du raisin et de la vigne
Ces molécules sont présentes en quantité différentes en fonction du cépage, du stade de maturité du fruit, et du terroir. Les principaux acides organiques sont les acides citrique, malique et tartrique, présents à des concentrations de quelques g/L. Les tanins sont des polyphénols aux propriétés antioxydantes, antimicrobiennes, pigmentaires et gustatives (goût herbacé, amertume et astringence) [9, 10].
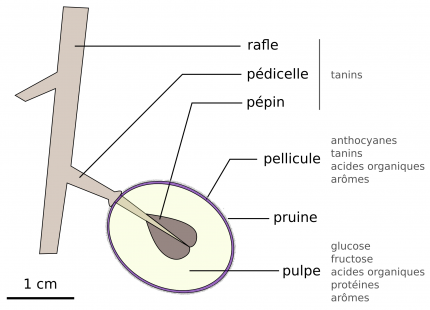
Le raisin est le fruit de la vigne Vitis vinifera (Figure 9). Les baies sont organisées en grappes, et sont récoltées durant les vendanges qui se déroulent d’août à octobre dans l’hémisphère nord. La période de récolte dépend des propriétés gustatives recherchées par le vigneron (atteinte de la maturité en sucres et/ou en tanins) et varie d’une année sur l’autre [4].
La pruine qui couvre la pellicule est une couche cireuse sur laquelle se développent des bactéries et des levures sauvages, dont peu de Saccharomyces. Cette flore microbienne n’est pas adaptée aux conditions de vinification et disparaîtra au profit des S. cerevisiae domestiques présentes dans les caves, en laissant toutefois une empreinte aromatique au vin [4].
Les variétés de vigne sont nommées cépages, dont la diversité de goûts est renforcée par les caractéristiques pédologiques et climatiques du terrain. Un stress hydrique modéré (climat sec, terrain drainé, en pente) et un fort ensoleillement (coteaux sud-ouest) permettent de favoriser la fructification et d’augmenter la quantité de sucres des baies [4].
Le terroir viticole représente donc la confluence entre la géologie, le climat, la biologie de la vigne et les pratiques de culture, et confère son originalité à chaque parcelle. [voir les articles Planet-Terre Éclogites et vignobles : exemples de la Vallée d'Aoste (Italie) et du Pays Nantais, Les vignobles de Lanzarote (Canaries) et de Pico (Açores) : deux exemples de vignes sur des volcans actifs, Champs de fractures et vin en Alsace)]
Les vignes sont artificiellement reproduites par greffage : le porte-greffe est choisi en fonction de son adaptation au terrain, et les sarments greffés sont sélectionnés pour leurs caractéristiques agronomiques (résistance aux maladies, rendement, qualité…) [4].
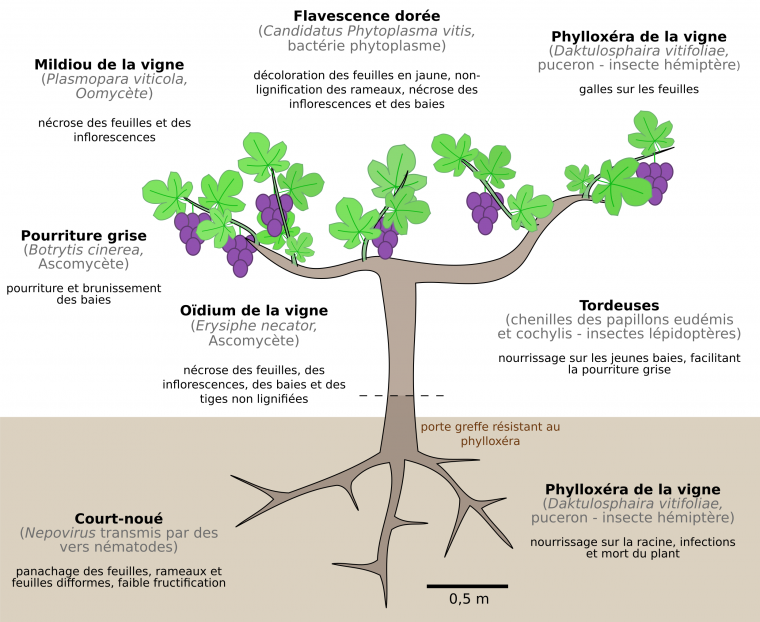
Le greffage est également une réponse à l’invasion d’un puceron d’origine américaine, le phylloxéra de la vigne (Daktulosphaira vitifoliae), qui ravagea les vignes européennes à la fin du XIXe. L’utilisation de porte-greffes d’espèces américaines résistantes (V. riparia, V. rupestris et V. berlandieri) donne des plants hybrides dont les rameaux sont des clones de cépages européens traditionnels. Cependant, d’autres maladies atteignent encore les vignes françaises (Figure 10) [4].
Le nom de la maladie est indiqué en noir. L’espèce et son appartenance phylogénétique sont données entre parenthèses. En-dessous sont précisés les principaux symptômes.
Quelques molécules importantes du raisin
...pour la fermentation
Les raisins matures contiennent peu de saccharose ou d’amidon, mais jusqu’à 25 % massique de fructose et glucose, facilement mis en évidence par un test à la liqueur de Fehling sur du jus de raisin blanc. Le vigneron utilise un réfractomètre pour mesurer la concentration en sucres présents dans le jus des baies, et décider de débuter les vendanges. Ce paramètre est essentiel, car la concentration en sucres du moût détermine directement la teneur en alcool du vin produit (Figure 3).
...pour la couleur
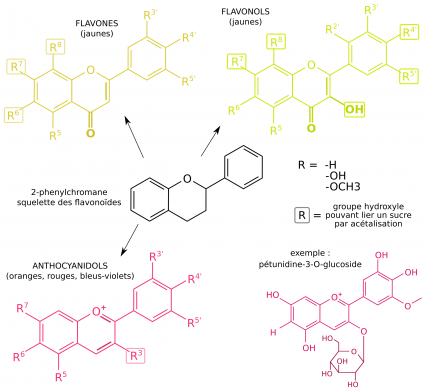
Ces molécules sont présentes sous formes d’hétérosides (molécule liée à un ou plusieurs sucres) dans le raisin, ce qui permet leur stabilisation et leur solubilisation [10, 27]. Les anthocyanes sont formées par un noyau anthocyanidol relié à un mono, di ou triholoside. L’exemple donné est celui de la pétunidine-3-O-glucoside présente dans le raisin noir.
La couleur de ces pigments peut varier avec le pH, la complexation avec des ions métalliques (Al2+, Fe2+, Fe3+), leur degré d’oxydation, leurs liaisons faibles avec d’autres molécules (phénomène de copigmentation), ou leur liaison conjuguée avec d’autres molécules (les tanins notamment) [11, 27]. Ces phénomènes sont responsables de l’évolution de la couleur du vin au cours de sa vie [10].
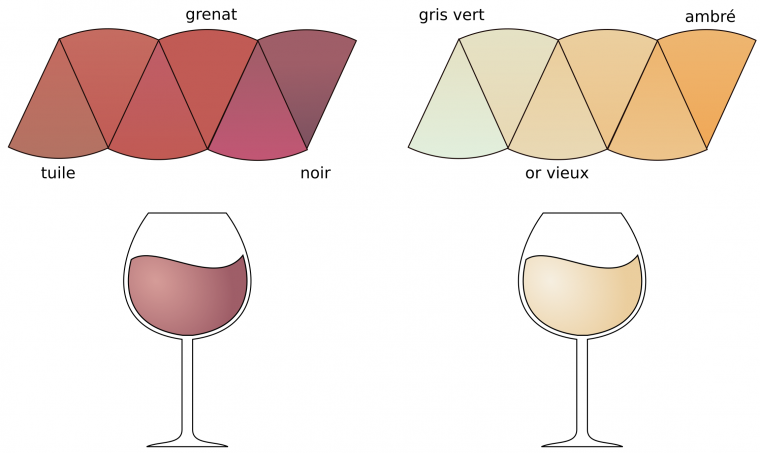
La couleur des raisins noirs est due aux anthocyanes, des pigments de la famille des flavonoïdes contenus dans la vacuole des cellules de la pellicule. Dépourvus de ces pigments, les cépages blancs doivent leur couleur à d’autres composés phénoliques (flavones, flavonols et tanins) présents dans la pulpe (Figure 11) [9, 10]. Toutes ces molécules sont responsables de la couleur des vins (Figure 12), et participent dans une moindre mesure à leur goût.
Les grandes lignes de la vinification
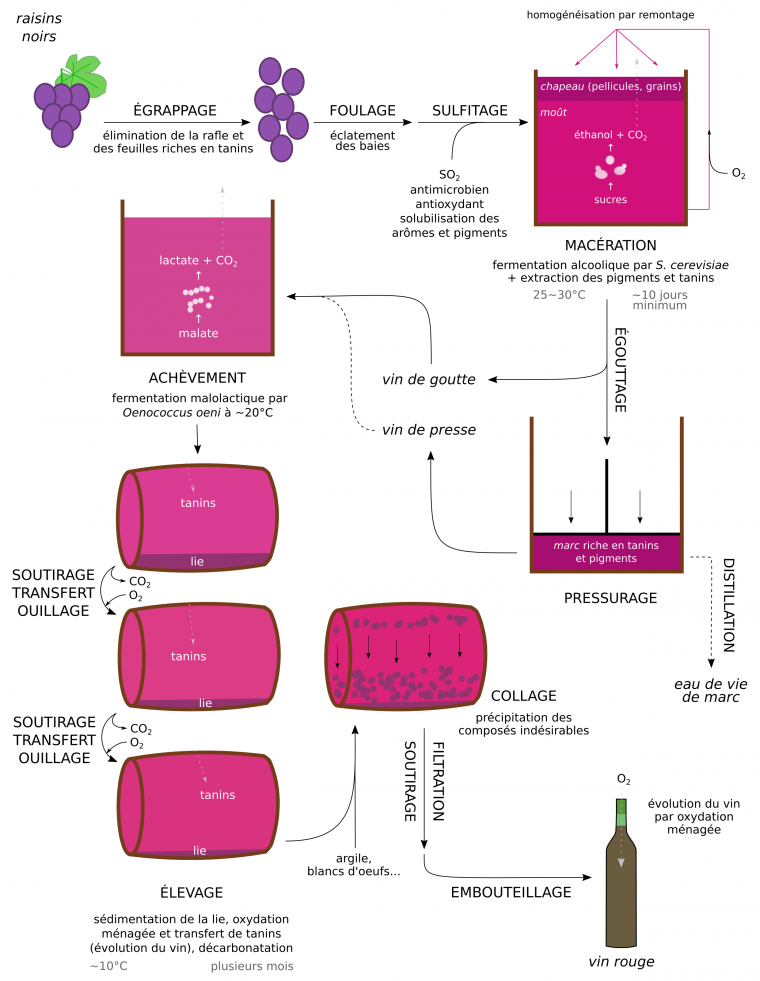
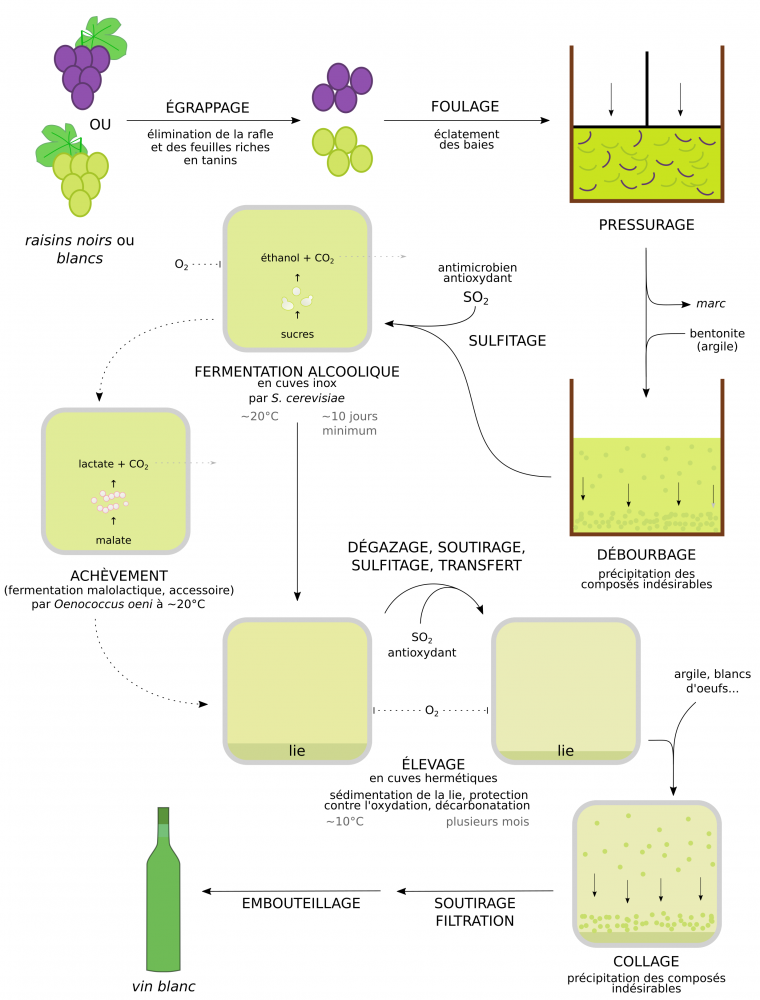
La vinification en rouge ou en blanc correspondent à deux méthodes de fabrication du vin qui possèdent la même trame, mais aussi quelques spécificités importantes (Figures 13 et 14). La vinification en rouge utilise l’intégralité de la baie des raisins noirs, tandis que le vin blanc est produit à partir du seul jus non coloré de cépages noirs ou blancs, la pellicule étant éliminée [4, 12, 13].
Les vins rouges
La première étape de la fabrication d’un vin rouge est l’égrappage, qui permet la récupération des baies et l’élimination des feuilles, de leur pédoncule et de la rafle. Les tanins amers, herbacés et astringents présents dans les feuilles et le pédoncule sont ainsi mis à l’écart. Vient ensuite le foulage durant lequel l’éclatement des baies conduit à l’obtention du moût, qui correspond donc à un mélange de pellicule et de jus issu de la pulpe.
Ce moût subit alors un sulfitage, qui consiste en l’ajout de dioxyde de soufre SO2 (les enjeux de cette étape sont développés en 2.4). En solution, au pH du vin (compris entre 3 et 4), la forme majoritaire de cet acide est l’ion hydrogénosulfite (ou bisulfite) HSO3−.
Si le moût est pauvre en azote (NH4+, acides aminés…), un apport est réalisé pour favoriser la multiplication et l’activité métabolique des levures durant la fermentation. Cet apport peut-être réalisé avant la fermentation, ou durant le premier tiers de celle-ci.
Durant l’étape de macération qui suit, deux événements importants se produisent : l’extraction des composés de la pellicule, qui donnent la coloration et une partie des arômes du vin, et la fermentation alcoolique. L’augmentation de la température et de la concentration en alcool qui se produit au cours de la fermentation facilite d’ailleurs l’extraction des pigments et tanins.
L’homogénéisation du moût empêche la formation d’un « chapeau » de débris solides en surface qui, sinon, limiterait l’extraction et favoriserait le développement de bactéries acétiques. Cette homogénéisation est réalisée par remontages (arrosage du chapeau par le vin) et pigeages (immersion du chapeau) qui permettent également d’oxygéner le moût, facilitant la croissance et la viabilité des levures ainsi que l’oxydation ménagée du vin.
La fermentation alcoolique démarre naturellement grâce à la microflore présente dans l’environnement de la cave, ou suite à un levurage (ajout de souches commerciales dans le moût). Elle dure de 5-6 jours à parfois plus d’un mois. La température du moût augmente, puis est maintenue entre 25 et 30 °C1. Cette régulation de la température évite une fermentation trop rapide, la mort des levures, la production d’arômes indésirables et, à l’inverse, la dégradation des arômes d’intérêt. À l’issue de la fermentation, la concentration en levures atteint plus de 10⁸ cellules/mL, générant, avec d’autres débris solides, un trouble dans le liquide.
La densité du moût est régulièrement contrôlée. Dans un vin sec, la fermentation est totale, tandis que dans un vin sucré une partie des sucres n’a pas été consommée (voir 1.2 et Figure 3). La concentration finale en sucres détermine l’appellation du vin : sec ≤ 20 g/L (mais généralement moins de 5 g/L) ; demi-sec ≈ 20 g/L ; moelleux ≈ 30 g/L ; liquoreux ≥ 40 g/L.
Une fois la macération terminée, l’égouttage permet de séparer par écoulement ou soutirage la partie liquide, le vin de goutte, d’un résidu solide, le marc. Le pressurage consiste alors à extraire le vin de presse par pressage du marc. Ce vin de presse est plus riche en tanins, pigments et sucres, et peut être ajouté au vin de goutte en fonction des qualités finales recherchées.
Vient ensuite l’étape d’achèvement durant laquelle se déroule la fermentation malolactique du vin (voir 1.3.3) à environ 20 °C, après un démarrage spontané ou par ensemencement. La densité en Oenococcus oeni atteint plus de 10⁷ cellules/mL. Le vin s’« assouplit » gustativement par la conversion du malate en lactate. Ce processus peut facilement être suivi par chromatographie (voir 1.3.3) .
Le vin subit alors l’élevage, étape qui permet sa maturation. Il se déroule en fûts ou en cuve en inox entreposés dans les chais à environ 10 °C et peut durer de plusieurs mois à plusieurs années. L’élevage consiste en :
- un transfert de cuve régulier par soutirage pour se débarrasser des particules ayant sédimentées, qui forment la lie.
- une aération du vin pour éliminer le CO2 et les composés volatils réduits et indésirables. Par ailleurs, une oxydation ménagée du vin par l’O2 stabilise sa couleur, développe son bouquet (palette aromatique) et exprime son terroir (caractéristiques gustatives propres au vignoble).
- une évolution aromatique par diffusion des tanins du bois, liés au terroir du fût (espèce, forêt, méthode de fabrication…). Si les cuves utilisées sont en inox et non en bois, des copeaux et des galles de chêne sont ajoutés comme source de tanins.
- l’ouillage, qui correspond au maintien des fûts toujours pleins par ajout de vin qui remplace la « part des anges » (vin évaporé à travers le bois).
L’alternance entre des conditions réductrices (ouillage) et oxydantes (soutirage et transfert) permet aux vins rouges de développer leur bouquet, grâce à des successions d’oxydations ménagées et de réactions entre les composés du raisin, ceux produits par les micro-organismes et ceux provenant du bois. Les vins « primeurs » (par exemple les Beaujolais) ne subissent pas d’élevage, contrairement aux vins « de garde », et ont de fait des goûts considérablement différents.
L’étape de collage permet finalement la sédimentation des derniers composés indésirables du vin (levures non floculées, tanins ou protéines) par précipitation à l’aide d’argile, de caséine, de gélatine, de blancs d’œufs, etc.
Enfin, la mise en bouteille a lieu et consiste en une filtration du vin suivie de son embouteillage. Les bouchons de liège sont produits à partir du suber du chêne-liège (Quercus suber), et leur perméabilité au dioxygène permet une lente maturation en bouteille. D’autres types de bouchons moins coûteux sont également utilisés : matières plastiques, liège aggloméré, ou capsule d’aluminium à visser (par ordre de perméabilité aux gaz décroissante).
Les vins blancs
Lors de la vinification en rouge, l’étape de fermentation alcoolique se déroule alors que le jus et les pellicules du raisin sont en contact, permettant ainsi le transfert de composés aromatiques et colorés des pellicules vers le jus. À l’inverse, lors de la fabrication d’un vin blanc, le jus est rapidement séparé des pellicules lors de l’étape de pressurage. Le moût produit est peu coloré, et sa faible teneur en tanins le rend particulièrement sensible à l’oxydation. Après le pressurage, le jus subit une étape de débourbage afin de le débarrasser de ses composés indésirables : particules en suspension et protéines du moût, en particulier les phénoloxydases qui provoqueraient sinon un brunissement du liquide. Le débourbage est réalisé grâce à l’action d’une argile, la bentonite, qui adsorbe ces composés. C’est seulement après le pressurage et le débourbage, suivis du sulfitage, que démarre la fermentation alcoolique. Celle-ci se produit à une température d’environ 20 °C, plus faible que celle des rouges. À l’issue de cette fermentation alcoolique certains vins blancs passent, comme les vins rouges, par une étape de fermentation malolactique (achèvement). Enfin, durant l’élevage, un seul soutirage avec sulfitage est réalisé, et les cuves utilisées durant cette phase sont majoritairement en inox étanche car l’oxydation est nuisible à la couleur et aux arômes des vins blancs. Cependant certains vins subissent un élevage en fût comparable à ceux des vins rouges, et développent ainsi des arômes et des teintes plus oxydés : c’est le cas des vins jaunes du Jura.
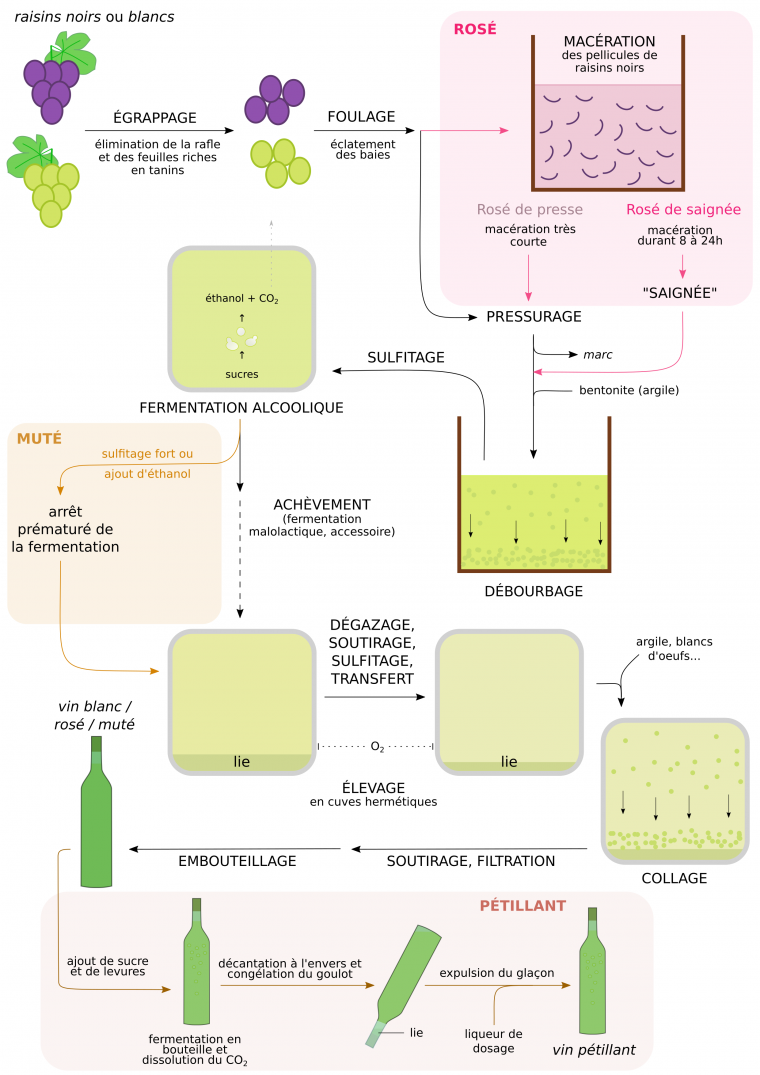
Les vins rosés
Les vins rosés ne résultent pas du mélange de vins blancs et rouges (sauf pour le champagne rosé), mais sont obtenus à partir de cépages noirs. Ceux-ci subissent une macération courte, permettant l’extraction partielle de certains des composés aromatiques et colorés de la pellicule vers le moût, puis une vinification en blanc.
Les vins pétillants
L’effervescence des vins pétillants s’obtient par ajout de sucre et de levures au vin, après l’élevage. Cette seconde fermentation en cuve pressurisée ou en bouteille permet le maintien du CO2 produit à l’état dissous. C’est de cette façon que sont obtenus, entre autres, les champagnes et les crémants.
Les vins mutés
Les vins mutés sont réalisés à partir de raisins riches en sucres. La fermentation est arrêtée précocement par un sulfitage fort, ou par ajout dans le moût d’alcool neutre ou d’eau-de-vie de vin. Le vin produit est donc sucré, et son taux d’alcool est contrôlé par la quantité d’éthanol ajoutée. Le muscat et le pineau des Charentes constituent des exemples de vins mutés1.
La saignée sépare le moût coloré des pellicules par simple écoulement. Les vins mutés peuvent être des vins rouges ou blancs, et sont souvent élevés en fûts de manière à développer leurs palettes aromatiques. La seconde fermentation des vins pétillants se déroule soit en cuves résistantes à la pression, soit en bouteille (schéma). Dans ce dernier cas, la liqueur de dosage (vin mélangé à du sucre) permet de compenser le volume perdu durant le débouchage, et est ajoutée rapidement avant le rebouchage. La concentration finale en sucres détermine l’appellation du vin : extra brut, brut, sec, demi-sec, doux (concentration en sucres croissante).
Le rôle du SO2 en vinification
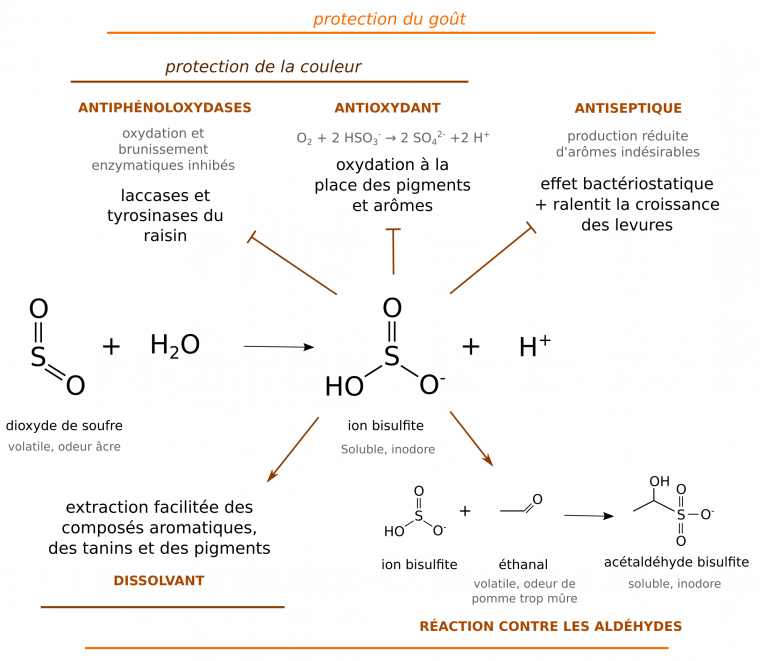
Quasiment indispensable en vinification, le dioxyde de soufre exerce un rôle antioxydant [4, 14] :
- Il joue un rôle de tampon en évitant l’oxydation des tanins, des pigments et des arômes par le dioxygène. En effet le SO2 est oxydé, à la place de ces molécules, en ions sulfates SO42−.
- Il inhibe les phénoloxydases du raisin responsables du brunissement du moût.
De plus, l’effet bactériostatique du dioxyde de soufre empêche la croissance de bactéries contaminantes. Il prévient également l’apparition d’odeurs « d’évent » causées par les aldéhydes volatils tels que l’éthanal (voir 1.3.4). En effet, le dioxyde de soufre se combine aux fonctions carbonyles de ces molécules, ce qui les solubilise et neutralise leurs propriétés organoleptiques indésirées [14]. Enfin, c’est un agent favorisant la dissolution des tanins et des arômes [4, 14].
SO2 = dioxyde de soufre ; HSO3− = ion bisulfite ; SO32− = ion sulfite ; SO42− = ion sulfate.
Biologie de la bière
De l’orge au malt
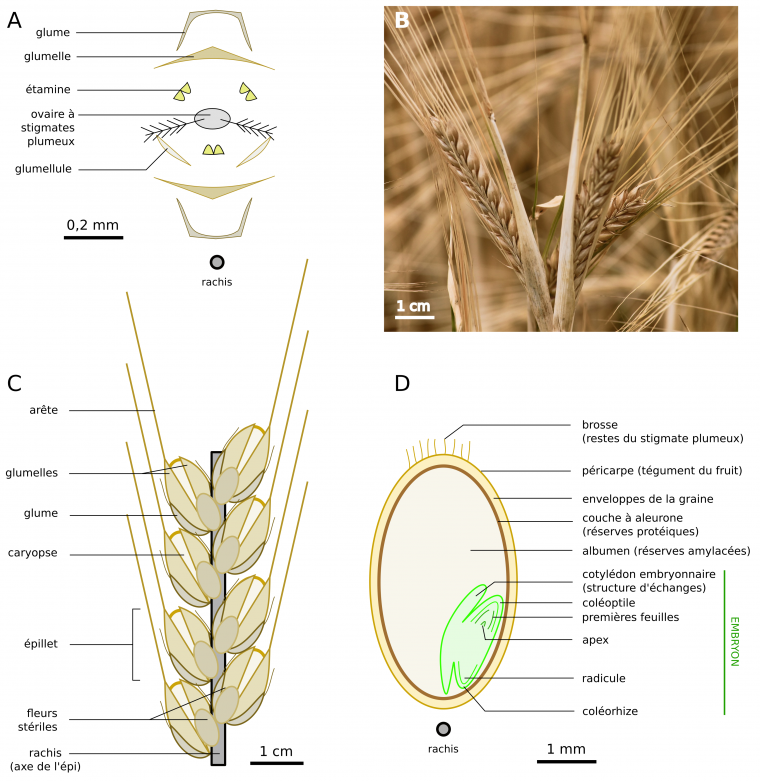
L’orge (Hordeum vulgare, famille des Poacées) est une céréale utilisée comme plante fourragère (pour la sous-espèce H. vulgare hexastichum, l’orge à six rangs) ou comme ingrédient principal de la bière (pour la sous-espèce H. vulgare distichum, l’orge à deux rangs) [15, 16]. Ses fruits sont des caryopses riches en amidon et contiennent chacun un embryon (Figure 17).
A : diagramme floral d’un épillet à une fleur ; B : photographie d’épis ; C : schéma d’un épi d’épillets ; D : schéma en coupe longitudinale d’un grain (= caryopse).
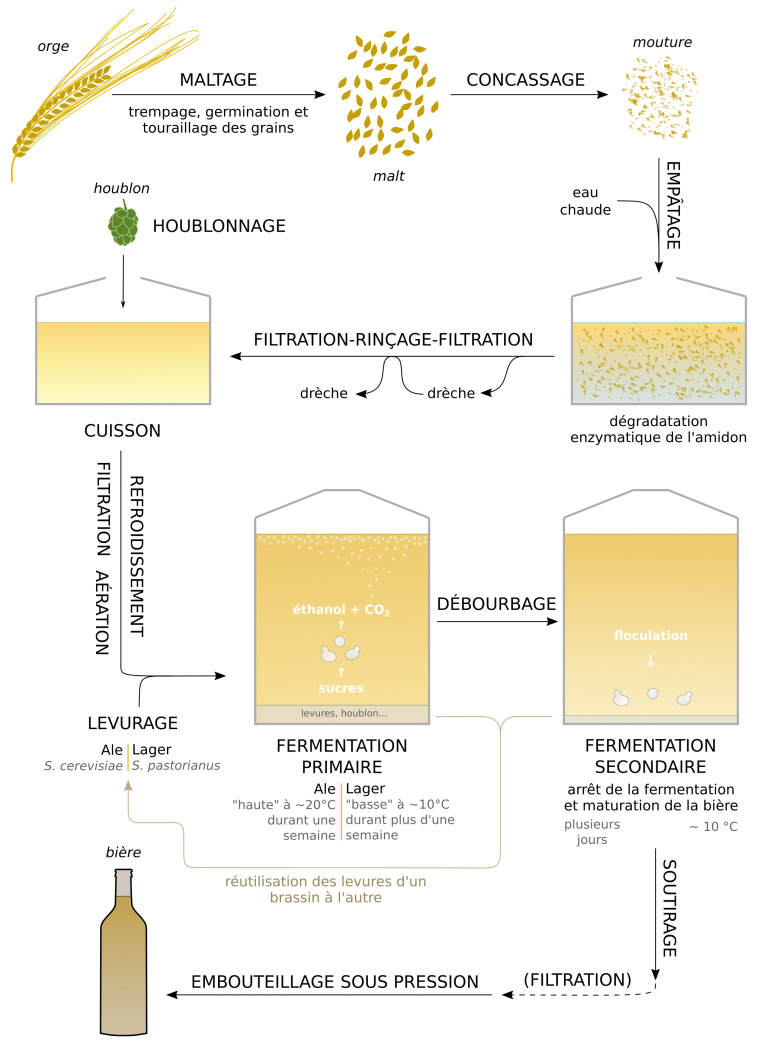
La première étape dans la fabrication de la bière correspond à la transformation des grains en malt, une opération nommée maltage. Ce processus comprend plusieurs étapes [17].
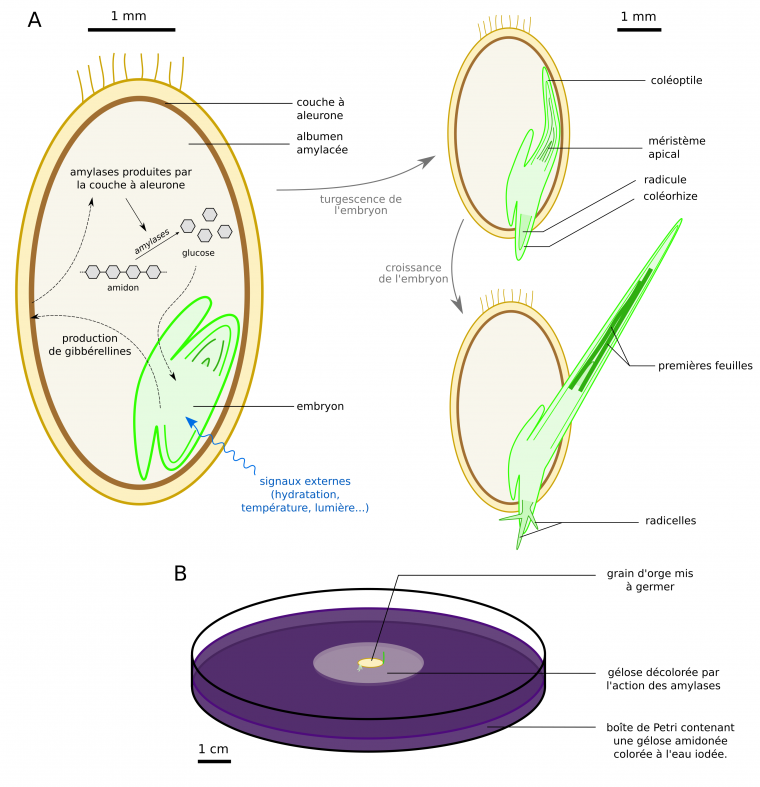
Lors de l’étape de trempage les grains d’orge subissent une alternance entre des bains d’une douzaine d’heures et des phases d’aération, ce qui permet leur sortie de dormance. Vient alors une étape de germination durant laquelle les grains sont mis à germer durant une dizaine de jours à environ 12 °C dans des conditions d’humidité élevée (Figure 18). Le « malt vert » obtenu est riche en enzymes, et ses radicelles sont visibles.
A : étapes et mécanismes de germination du grain. Des signaux externes conduisent à la sortie de dormance de l’embryon, dont la production de gibbérellines (hormones végétales) déclenche la mobilisation des réserves de l’albumen [9, 11]. La réhydratation de l’embryon permet sa turgescence et la sortie du coléorhize puis du coléoptile. Le fonctionnement des méristèmes apicaux conduit ensuite à la croissance de la plantule.
B : mise en évidence de la production d’amylases par le grain au cours de sa germination.
Voir aussi Les plantules modèles : pois, blé, maïs et soja (2/2).
Le touraillage vise ensuite à lentement déshydrater le malt vert, par ventilation et chauffage dans un four durant environ 30 h à des températures allant de 45 jusqu’à 85 °C, puis à température constante durant quelques heures. Les grains développent une coloration et des arômes typiques (réactions de Maillard, voir 1.3.4) à l’origine de différents types de malt qui détermineront la couleur et le goût de la bière obtenue [17-19] (Figure 23) :
- blonde : grains légèrement torréfiés à environ 85 °C, couleur dorée, goût léger de miel.
- ambrée : grains torréfiés à environ 110 °C, couleur et goût de biscuit/croûte de pain, ou de caramel s’il n’y a pas eu de séchage préalable.
- brune : grains brûlés à environ 220 °C, couleur noire et goût profond, café, chocolat.
- blanche : malt de blé, non ou très légèrement torréfié.
La totalité des enzymes des malts touraillés à haute température sont inactivées : ils n’apportent pas d’activité amylolytique et ont ainsi un intérêt purement aromatique et colorant. Au contraire le malt « blond », peu colorant, peu aromatique mais possédant toujours une activité enzymatique malgré la torréfaction, sert de base à toutes les recettes de bière [18, 19].
Le malt est finalement obtenu après dégermage mécanique des grains et élimination des grains non germés.
La digestion enzymatique du malt lors du brassage
Le brassage désigne le processus par lequel est obtenu le moût, à partir d’eau, de malt et de houblon. Il comprend plusieurs étapes [20].
Le concassage consiste à assembler les différents malts choisis pour la recette puis à les broyer en une mouture grossière.
Cette mouture est ensuite mélangée à de l’eau de manière à obtenir la « maische », qui est ensuite brassée (mélangée) et chauffée de manière à provoquer la digestion enzymatique de l’amidon contenu dans le malt (Figure 18). Ces étapes d’empâtage, permettent de produire un moût sucré. Un chauffage en plusieurs étapes est généralement utilisé :
- un palier de 15 min autour de 50 °C réactive et solubilise les enzymes produites durant la germination des grains.
- un palier de 40 min autour de 60 °C permet l’hydratation de l’amidon et l’action des β-amylases.
- un palier de 30 à 60 min autour de 70 °C permet l’action des α-amylases et l’extraction des arômes et pigments du malt.
- un palier de 10 min autour de 80 °C inactive les enzymes, et solubilise les composés restants.
En parallèle, les protéines du malt sont dégradées par des protéases également produites durant la germination. Le moût s’enrichit en acides aminés utilisables par les levures pour leur multiplication et leur croissance.
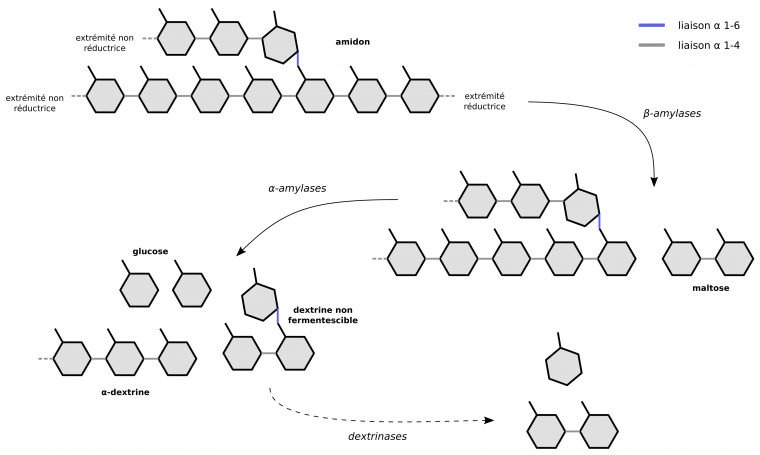
Les β-amylases hydrolysent l’amidon à partir de ses extrémités réductrices (activité exolytique) et produisent du maltose ; les α-amylases hydrolysent les liaisons α 1-4 au sein l’amidon (activité endolytique) et produisent des oligomères α 1-4, dont des dextrines non-fermentescibles qui ajoutent de la texture à la bière [9, 11].
Flèche pointillée : les dextrinases hydrolysent les liaisons osidiques α 1-6, mais sont inactivées dès 45 °C. Cette réaction ne se déroule donc pas durant l’empâtage [20].
Une filtration permet ensuite de séparer le moût sucré de la drèche (partie solide composée des enveloppes et de particules de malt). La drêche subit une nouvelle extraction à l’eau chaude et est filtrée à nouveau pour en extraire tout le moût sucré. Celui-ci subit alors une cuisson. Il est porté à ébullition et est brassé pendant 1 à 2 h, au cours desquelles est ajouté le houblon. Les enzymes du moût coagulent, provoquant une clarification du liquide, tandis que sa couleur et son goût se prononcent (réactions de Maillard, voir 1.3.4). C’est également une étape de stérilisation qui réduit les contaminations. La concentration en sucres du moût est contrôlée à l’aide d’un réfractomètre, et déterminera la teneur en alcool de la future bière (Figure 3).
L’importance du houblon en brasserie
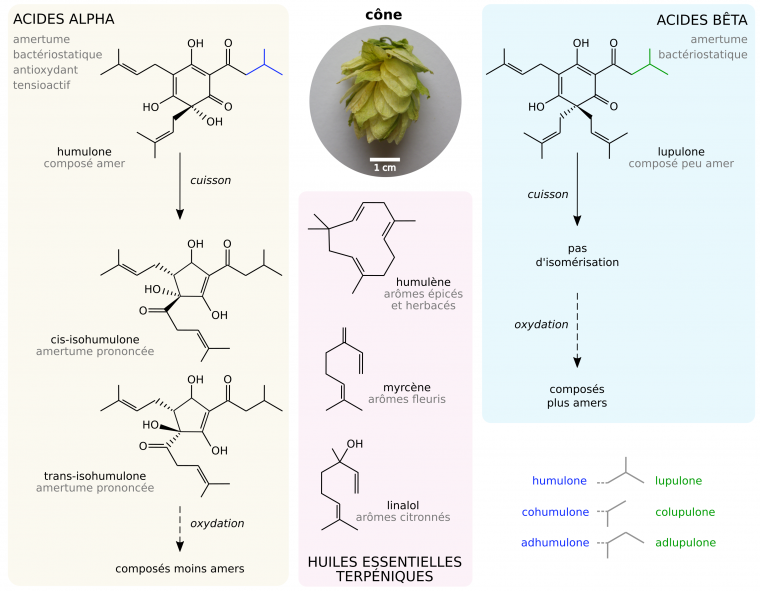
Le houblon (Humulus lupulus) est une liane herbacée dioïque de la famille des Cannabacées dont les fruits, appelés cônes, produisent la lupuline, une résine à l’odeur caractéristique [21]. Cette résine contient de nombreux composés d’intérêts pour le brassage [22, 23] :
- Des huiles essentielles, principalement des terpènes, qui ont un intérêt aromatique.
- Des acides alpha (isohumulones), qui confèrent l’amertume à la bière. Ils ont également des propriétés bactériostatiques sur les bactéries Gram +, antioxydantes, et favorisent la tenue de la mousse (propriétés tensioactives). Leur isomérisation durant la cuisson augmente l’amertume de la bière, mais leur oxydation au cours de la vie de la bière la diminue.
- Des acides bêta (isolupulones) qui ont une amertume dix fois plus faible que les acides alpha, et qui ont également des propriétés bactériostatiques et antioxydantes. Leur oxydation augmente l’amertume de la bière.
- Des tanins et polyphénols qui favorisent la coagulation des protéines du moût.
La composition des houblons diffère selon les variétés cultivées, de par leur diversité et leur richesse en huiles essentielles et en acides alpha et bêta.
Seuls les acides alpha s’isomérisent durant la cuisson. Leur oxydation diminue leur amertume, tandis que celle des acides bêta l’augmente. Un rapport alpha:bêta de 2:1 permet en pratique de conserver un degré d’amertume stable tout au long de la maturation (et donc de l’oxydation potentielle) de la bière [22, 23].
Les formules de ces molécules sont disponibles sur PubChem.
Le houblonnage a lieu durant la cuisson : les houblons sont ajoutés dans le moût sucré en ébullition en une ou plusieurs fois, sous la forme de granulés (cônes broyés et comprimés).
Les huiles étant rapides à extraire, un houblonnage tardif apportera beaucoup d’arômes. En revanche les acides sont extraits plus lentement, et les alpha s’isomérisent sur la durée : un houblonnage précoce donnera de l’amertume à la bière [20].
Le profil aromatique de la bière repose sur les variétés de houblon choisies, leur quantité et leur temps d’infusion (Figure 23). D’autres éléments aromatisants peuvent être utilisés, comme des épices ou des fruits [19, 20, 24].
Il est également possible d’ajouter des houblons ou des épices en fin de fermentation (houblonnage « à cru »), ce qui permet d’extraire principalement les huiles essentielles et ainsi d’apporter des arômes mais peu d’amertume.
La transformation du moût en bière
Les levures choisies par le brasseur métabolisent les composants du moût sucré houblonné, et le transforment en bière [25].
À la fin de la cuisson, un soutirage permet la séparation du moût des résidus solides ayant sédimenté (houblon, protéines coagulées) dans la cuve. Il est alors filtré, refroidi et aéré, puis transféré dans une cuve de fermentation aseptisée. Cette étape permet notamment de réoxygéner le moût dégazé par la cuisson, ce qui favorise la multiplication des levures en début de fermentation (voir 1.3).
Afin de démarrer la fermentation le brasseur procède au levurage : le moût est ensemencé avec des levures sèches ou réutilisées à partir de brassins (moûts en cours de fermentation) précédents. Plusieurs souches de levures existent, chacune ayant des caractéristiques différentes d’atténuation (capacité à consommer les sucres présents dans le moût), de température de fermentation et de production d’esters aromatiques.
Deux types de bières sont obtenues en fonction de l’espèce de levure utilisée [1, 26]. Pour les bières de type « Ale », c’est S. cerevisiae qui est inoculée dans le moût. La fermentation est dite « haute » car les levures fermentent au sommet de la cuve et à 20 °C environ. C’est la fermentation artisanale par excellence, car elle se déroule en une semaine environ, à température ambiante, et permet de produire des bières aux goûts complexes et avec un taux d’alcool supérieur à 5°.
Pour les bières de type « Lager » la fermentation est réalisée par S. pastorianus et est dite « basse » car ces levures fermentent au bas de la cuve. Elle se déroule dans des cuves refroidies à 10 °C environ, sur une durée plus longue que pour les ales. Elles nécessitent donc des installations plus conséquentes. Les lagers ont un goût léger, peu complexe et elles sont moins alcoolisées. La majorité des bières produites à l’échelle industrielle sont des lagers.
La fermentation spontanée (bières de type lambics) ou à partir de souches de levures non conventionnelles sont des variantes explorées par les brasseurs. Enfin, dans les bières de type « sour » des bactéries du genre Lactobacillus sont inoculées et réalisent une fermentation lactique [26].
À la suite du levurage, les levures se multiplient et entament une fermentation rapide des sucres, en une semaine environ pour les ales : c’est la fermentation « primaire » (ou tumultueuse). La cuve résistante à la pression permet la dissolution du CO2. La densité du moût est régulièrement mesurée jusqu’au ralentissement de la fermentation et l’atteinte de l’atténuation désirée (Figure 3).
La bière est alors refroidie et maintenue à faible température durant plusieurs semaines. La fermentation s’arrête sous l’effet de la température et de la baisse de nutriments disponibles. Le métabolisme des levures ralentit, les cellules floculent et la bière acquiert sa maturité aromatique grâce à la production de métabolites secondaires par les levures et aux réactions entre les différents composés dissous (voir 1.3.4). Cette étape de fermentation « secondaire » (ou calme) n’est donc pas une étape de fermentation à proprement parler, mais une étape comparable à l’élevage du vin.
Certaines bières sont embouteillées plates et refermentées en bouteilles par adjonction de sucre et de levures durant l’embouteillage. Cependant l’appellation de bières « doubles », « triples » ou « quadruples » ne fait pas référence au nombre réel de fermentations qu’elles ont subies, mais à une teneur en éthanol croissante, allant de 7 à 12° (et donc à une plus grande quantité de malt utilisée pour l’empâtage) [19].
À droite : bière bien conservée ; à gauche : bière oxydée.
La bière est finalement soutirée de la cuve de manière à la séparer des bourbes (levures et particules solides sédimentées). Après une éventuelle filtration, elle est encapsulée dans une bouteille de verre teintée, sous pression et sous atmosphère inerte pour limiter l’oxydation délétère de ses arômes et de sa couleur (Figure 22).
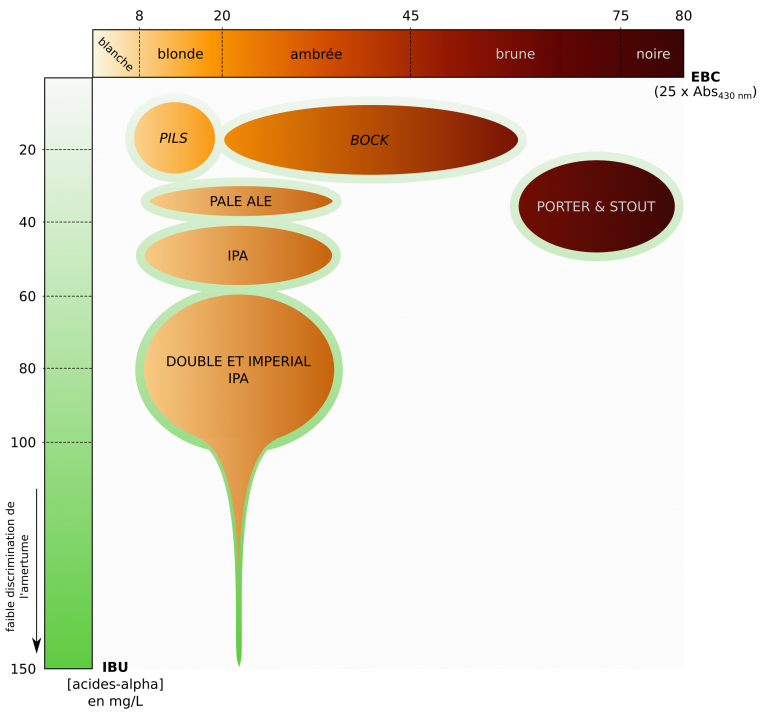
Il existe de nombreux « styles » de bières, dont la nomenclature est basée sur les méthodes de brassage, la fermentation (ale, lager, sour…), la couleur (malts), l’amertume (houblons), le degré d’alcool (élevé pour les imperial), la quantité de sucres résiduels (faibles dans les dry), les arômes, etc. (Figure 23) [19].
Les bières en italiques sont des lagers, les autres sont des ales. IPA : India Pale Ale.
La couleur de la bière se mesure sur l’échelle de couleur EBC (European Brewery Convention), allant de 0 (clair) à 80 (foncé), qui est liée à l’absorbance de la bière limpide à 430 nm. Cette valeur dépend des malts utilisés [19].
Le degré d’amertume de la bière est quantifiée de 1 à 150 sur une l’échelle IBU (International Bitterness Unit) et correspond à la concentration d’acides alpha dans la bière, en mg/L.Cette valeur dépend des quantités et des variétés de houblons utilisés, et du houblonnage effectué [19].
Conclusion
Le vin et la bière sont produits grâce à l’action du métabolisme fermentaire de levures domestiquées du genre Saccharomyces sur des produits végétaux, plus ou moins transformés : jus de raisin, éventuellement mélangé aux pellicules pour les vins, orge ou blé malté pour les bières. Alors que le jus de raisin contient déjà des sucres fermentescibles (glucose et fructose), l’orge et le blé contiennent essentiellement de l’amidon, non assimilable par les levures. C’est ce qui explique l’étape préalable de maltage réalisée dans la fabrication de la bière. Pour les deux types de boisson, la fermentation alcoolique du moût se produit à une température allant de 10 à 30 °C compatible avec la physiologie des levures employées. Alors que l’éthanol reste en solution, le dioxyde de carbone tend à s’échapper dans l’atmosphère mais peut cependant être partiellement conservé à l’état dissous dans la bière ou les vins pétillants, suite à une fermentation en cuve pressurisée ou par refermentation en bouteille. En plus de leur rôle dans la conversion des sucres en éthanol et CO2, les levures sont également impliquées dans la production de certains arômes via leur métabolisme carboné et azoté (arômes fermentaires) ou par hydrolyse de molécules présentes sous forme de précurseurs d’arômes dans le moût (arômes variétaux). Les levures contribuent également à dégrader certaines molécules aromatiques. Les souches de levures inoculées dans le moût sont d’ailleurs rigoureusement choisies par les brasseurs, tandis qu’en vinification traditionnelle l’inoculation se fait naturellement à partir de l’environnement de la cave, ce qui participe au terroir du produit1. Dans le cas du vin, le contact avec les pellicules de raisin et des fûts en bois est également à l’origine de transferts de composés aromatiques et colorés. Pour la bière, le goût varie en fonction du type de maltage pratiqué, des caractéristiques du houblonnage réalisé, et de l’éventuel ajout d’épices ou de fruits.
La transformation du raisin en vin, comme celle de l’orge ou du blé en bière, nécessite de contrôler finement les micro-organismes présents aux différentes étapes de fermentation. Les faibles températures employées en vinification comme en brasserie permettent de réduire le développement des micro-organismes thermophiles. Par ailleurs, l’éthanol produit par les levures exerce une action bactériostatique, de même que les sulfites ajoutés en vinification et que les tanins libérés par le houblon dans le cas de la bière ou par les pellicules de raisin et le bois dans le cas du vin. En brasserie, l’étape de cuisson permet de stériliser le liquide obtenu à l’issue du houblonnage.
Les exemples du vin et de la bière sont représentatifs des méthodes de production de toutes les boissons alcoolisées. Le jus de pomme ou de canne à sucre sont utilisés pour produire le cidre, le calvados et le rhum, tandis qu’une digestion de l’amidon contenu dans les malts de différentes céréales, l’agave ou le riz cuit est nécessaire pour la production du whisky, de la tequila ou du saké. Les étapes de fermentation sont similaires, puis la maturation en fûts de la plupart de ces boissons permet de complexifier leur saveur. Avant cette étape de maturation, l’intervention d’un procédé physique, la distillation, permet de produire des boissons avec des teneurs beaucoup plus élevées en alcool que le degré biologiquement atteignable à l’aide de levures.
Pour aller plus loin
- La vinification des vins rouges, Bureau interprofessionnel des vins de Bourgogne, YouTube, vidéo mise en ligne le 11 mai 2012
- La vinification des vins blancs, Bureau interprofessionnel des vins de Bourgogne, YouTube, vidéo mise en ligne le 11 mai 2012
- Vin sur vin, C'est par sorcier, YouTube, vidéo mise en ligne le 4 décembre 2015
Références
- Henché, S. Utilisation alimentaire des levures. (Université Henri Poincaré - Nancy I, 2000).
- Sampaio, J. P. Microbe Profile: Saccharomyces eubayanus, the missing link to lager beer yeasts. Microbiology (Reading)164, 1069–1071 (2018).
- Verstrepen, K. J., Derdelinckx, G. & Delvaux, F. R. Yeast flocculation : what brewers should know. Appl Microbiol Biotechnol 197–205 (2003) doi:10.1007/s00253-002-1200-8.
- Université de Bourgogne. MOOC #OpenWineUniversity. Catalogue de MOOC de l’Université de Bourgogne https://mediaserveur.u-bourgogne.fr/channels/#moocs (2020).
- Voet, D. & Voet, J. G. Biochemistry, 4th Edition. (W. Ross MacDonald School Resource Services Library, 2010).
- Willey, J. M., Sherwood, L. & Woolverton, C. J. Prescott’s microbiology. (McGraw-Hill, 2014).
- Salmon, J.-M. Interactions between yeast, oxygen and polyphenols during alcoholic fermentations: Practical implications. LWT - Food Sci. Technol.39, 959–965 (2006).
- Kayikci, Ö. & Nielsen, J. Glucose repression in Saccharomyces cerevisiae. FEMS Yeast Res.15, fov068 (2015).
- Taiz, L. & Zeiger, E. Plant physiology. 3rd edn. vol. 91 (2003).
- Sélosse, M.-A. Les goûts et les couleurs du monde : une histoire naturelle des tannins, de l’écologie à la santé. (Actes Sud, 2019).
- Buchanan, B., Gruissem, W. & Jones, R. Biochemistry & Molecular Biology of Plants. (2015).
- Coulombe, N. Chimie du vin - Cahier d’apprentissage. (2006).
- Comité National des Interprofessions des Vins à appellation d’origine et à indication géographique (CNIV). Production de vin. Intervin https://www.intervin.fr/de-la-vigne-au-vin/production-de-vin.
- Blouin, J. Pratique raisonnée du SO2 en œnologie. http://sn1.chez-alice.fr/vin/article/index.htm.
- Hordeum vulgare - Orge cultivé. Botarela http://botarela.fr/Poaceae/Taxons/Hordeum-vulgare.html.
- Orge commune. Wikipédia (2020).
- Production du malt. Univers-Bières.net http://univers-biere.net/malterie.php.
- Tout savoir sur les malts, céréales et sucres de la bière. Happy Beer Time https://www.happybeertime.com/blog/2016/05/03/tout-savoir-sur-les-malts-cereales-et-sucres-de-la-bi… (2016).
- Law, D. & Grimes, B. The homebrew handbook : 75 recipes for the aspiring backyard brewer. (CICO Books, 2012).
- Étapes de brassage. Univers-Bières.net http://univers-biere.net/brasserie.php.
- Prat, R. & Rubinstein, J.-P. Houblon (Humulus lupulus Cannabacées). Sorbonne Université – UFR des Sciences de la Viehttp://www.snv.jussieu.fr/bmedia/arbres/houblon.htm (2016).
- BtoBeer. Le Choix du Houblon pour la bière : de la chimie aux flaveurs. BtoBeer https://www.btobeer.com/themes-conseils-techniques-bieres-brasseries/conseils-houblons-bieres/le-ch….
- Bocquet, L. Les composés phénoliques du houblon, Humulus lupulus L. : Lutte contre la résistance microbienne et perspectives industrielles. (Université de Lille, 2018).
- Houblonnage. Wikipédia (2020).
- Fermentation de la bière. Univers-Bières.net http://univers-biere.net/bio_fermentation.php.
- Beer | alcoholic beverage. Encyclopedia Britannica https://www.britannica.com/topic/beer.
- Anthocyane. Wikipédia (2020).
- Diaz-Ruiz, R., Rigoulet, M. & Devin, A. The Warburg and Crabtree effects: On the origin of cancer cell energy metabolism and of yeast glucose repression. Biochim. Biophys. Acta BBA - Bioenerg.1807, 568–576 (2011).
- Dequin, S. Glycérol et vinification. Lallemand œnologie (2014), https://www.lallemandwine.com/wp-content/uploads/2014/09/WE-1-FRANCE-anonym%C3%83%C2%A9-final.pdf.
- Alexandre, H., Rousseaux, I. & Charpentier, C. Relationship between ethanol tolerance, lipid composition and plasma membrane fluidity in Saccharomyces cerevisiae and Kloeckera apiculata. FEMS Microbiology Letters124, 17–22 (1994).