Cet article présente quelques traits caractéristiques du chromosome Y de l'homme, à la lumière de la génétique, de la phylogénétique et du séquençage. Il aborde, en conclusion, le possible devenir de ce petit chromosome spécifiquement mâle.
Introduction
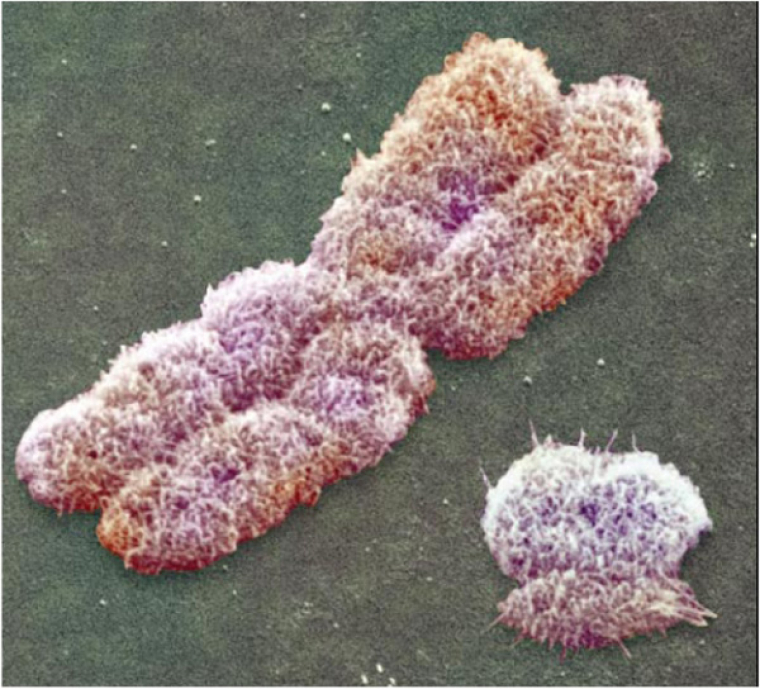
Contrairement aux autres chromosomes, dits autosomes, dont chaque paire est formée de chromosomes homologues et de même taille, les chromosomes sexuels sont souvent de taille différente. On trouve par exemple un grand X et un petit compagnon Y, chez l’Homme, comme chez beaucoup de Mammifères.
Un grand chromosome X et un petit chromosome Y
Vue prise au microscope électronique à balayage.
Le portrait du chromosome Y humain s’est largement précisé à la lumière de la génétique, de la phylogénétique et du séquençage (voir références 1, 2 et 3).
Le chromosome Y humain à la lumière de la génétique
Le chromosome Y humain mesure le tiers de la taille du chromosome X et contient environ dix fois moins de gènes.
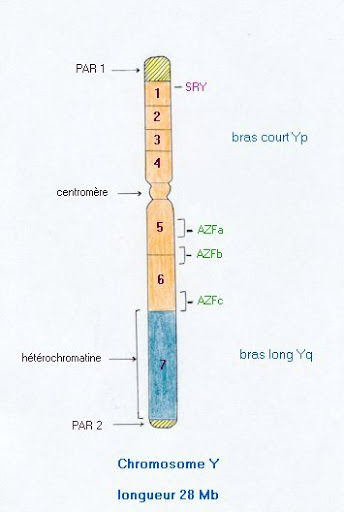
Il peut être divisé en deux types de régions, selon leur homologie, ou non, avec le chromosome X :
Les régions pseudo-autosomales (PAR)
Situées aux deux extrémités du chromosome Y, elles couvrent 5 % de sa longueur. Représentées également sur les deux extrémités du chromosome X, elles permettent l’appariement de ces deux partenaires, lors de la première phase de la méiose. La formation de ces bivalents, lors de la prophase I, permet par la suite le processus de recombinaison homologue, gage de brassages génétiques et de réparation de l’ADN.
Dans ces deux régions pseudo-autosomales, le chromosome Y et le chromosome X ne divergent pas, les mêmes 29 gènes codant des chaînes polypeptidiques y sont représentés.
La zone située entre les deux régions pseudo-autosomales
La zone située entre les deux PAR représente 95 % de la longueur du chromosome Y, dont, sur le grand bras, une large région d’hétérochromatine compacte, très riche en séquences répétées, et considérée jusqu’ici comme inerte. Pour le reste, elle contient 78 gènes codant des chaînes polypeptidiques.
Parmi ces gènes, certains codent des chaînes polypeptidiques que l’on trouve exprimées également chez les femmes, preuve qu’il existe d’autres zones d’homologie entre les chromosomes X et Y que les régions pseudo-autosomales.
A l’inverse, d’autres gènes sont spécifiques au chromosome Y : il s'agit de ceux impliquées dans la spermatogenèse et de SRY.
Les gènes impliqués dans la spermatogénèse
Le chromosome Y est fortement impliqué dans la spermatogenèse . Depuis les années 60, certaines délétions de ce chromosome ont été observées chez des patients infertiles. En 1976, une région proximale du bras long a été impliquée dans des azoospermies et dénommée AZF (pour AZoospermia Factor). Par la suite la biologie moléculaire a subdivisé le chromosome Y en 7 régions.
Le bras long du chromosome Y comporte une quinzaine de famille de gènes impliquées dans la spermatogenèse .
Citons la famille du gène DAZ, située en AZFc. Le gène DAZ est un homologue d’un gène murin (chromosome 17) et c’est le plus fréquemment muté dans les infertilités masculines dues à une microdélétion du chromosome Y.
Citons encore la famille du gène RBM, en AZFb, dont le gène RBM1 présente une expression spécifique du testicule.
Voir la carte détaillée du chromosome Y
Cependant certains gènes impliqués dans la spermatogenèse sont portés par d’autres chromosomes (comme le gène du récepteur aux androgènes, porté par le bras long du chromosome X).
Le gène SRY (sex determining region Y)
Le chromosome Y est la clé du déterminisme du sexe chez les mammifères. Avec l’équipement chrosomosique XX l’individu sera femelle, et avec XY, il s’agira d’un mâle : telle est la règle habituelle.
Mais la situation peut passablement se compliquer en cas d’anomalies chromosomiques sur ces gonosomes.
Dans l’espèce humaine, l’anomalie chromosomique XXY donne un phénotype mâle. C’est l’une des anomalies génétiques les plus fréquentes avec une fréquence moyenne de une sur 500 à 1000 naissances d’enfants de sexe masculin). Mais il est également possible de présenter un phénotype mâle en étant XX ou un phénotype femelle en étant XY.
Les porteurs de telles anomalies chromosomiques présentent des intersexuations correspondant à des désordres plus ou moins importants. Ainsi, la majorité des porteurs de XXY développent le syndrome de Klinefelter se traduisant, entre autres, par une stérilité, une faible production de testostérone, une faible pilosité et le développement de seins vers 50 ans. Les femmes XY, à cause de la présence d’un « Y non virilisant », n’ont pas d’anomalie visible, mais des ovaires incomplètement développés. D’autres cas de femmes XY sont dus à l’absence de récepteur à la testostérone (syndrome d’insensibilité complète aux androgènes ou SICA ), ces femmes présentent des testicules intra-abdominaux. Les hommes XX développent le syndrome de De La Chapelle , avec une petite taille, des testicules réduits et une infertilité, mais pas de difficulté d’apprentissage.
C’est en étudiant des patients présentant une inversion sexuelle de type « femme XY » ou « homme XX » que l’on a localisé le facteur déterminant le sexe mâle (ou Testis determinating factor, TDF) en 1990. En effet, seule une petite partie du chromosome Y, un fragment d’ADN de 35 Kilobases situé à l’extrémité du bras court (Yp), à proximité de PAR1, entraînait, selon qu’il était perdu ou transloqué, une inadéquation entre sexe chromosomique et gonadique. Les « femmes XY » l’avait perdu (délétion sur le chromosome Y) et les « hommes XX » l’avait gagné par translocation sur le chromosome X lors du crossing-over entre X et Y chez leur père. Ce facteur est un gène nommé SRY, qui pour effet de masculiniser en testicules les gonades jusque là indifférenciées du jeune embryon. La protéine SRY présente une expression très limitée dans le temps et déclenche (en association avec une autre protéine, SF1) l’activation du gène SOX9.
Le gène SOX9 (porté par le chromosome 17) est très conservé dans l’évolution. Il est responsable de la différenciation de certaines cellules du testicule primitif en cellules de Sertoli. Ce sont ensuite ces cellules de Sertoli qui, par leurs sécrétions paracrines, entraînent le développement de l’architecture complète du testicule (formation des tubes séminifères, vascularisation spécifique et différenciation des cellules de Leydig, dont les productions hormonales seront responsables des caractères sexuels secondaires).
Le sexe femelle n’est pas le résultat d’un programme « par défaut ». En particulier, l’inactivation de SOX9 est nécessaire pour obtenir un phénotype femelle. Certains gènes sont connus pour réaliser cette inhibition.
C’est notamment le cas de DAX1 (porté par le chromosome X) dont la duplication entraîne une réversion de mâle vers femelle chez les individus 46, XY qui la portent. Le gène DAX1 inhibe le gène SF1 chez la femelle et module donc l’action de SRY sur SOX9.
C’est également de cas de FOXL2 (bien étudié chez la chèvre et la souris), dont l’absence, dans une gonade XX, conduit à l’expression de SOX9 et à une différenciation des gonades en testicules, même en absence de SRY. Il a été montré queFOXL2 est capable de se fixer sur l’élément régulateur de SOX9 (TESCO situé en amont de SOX9 sur le chromosome 17).
En fait, et d’une façon générale, le déterminisme sexuel chez les êtres vivants est varié :
-
contrairement aux animaux, les plantes à fleurs sont pour la plupart hermaphrodites ;
-
chez la drosophile, les femelles sont également XX et les mâles XY, mais le sexe mâle provient de l’absence d’un autre X et non de la présence d’un Y ;
-
chez les serpents, les oiseaux, les papillons, la situation est inversée (ZW chez les femelles, ZZ chez les mâles) sans que l’on sache si c’est la présence du W qui détermine le sexe femelle ou la duplication du Z qui produit le sexe mâle ;
-
quant aux tortues, aux crocodiles, ils ne possèdent pas de chromosomes sexuels, et c’est la température à laquelle se développent leurs œufs qui oriente l’embryon vers le sexe mâle ou femelle…
Le chromosome Y humain à la lumière de la phylogénèse
Le gène SRY est présent chez les Thériens (Mammifères placentaires et marsupiaux) mais pas chez les Monotrèmes. L'ornithorynque possède un système de détermination sexuelle complexe, avec 10 chromosomes sexuels et des gènes impliqués dans le déterminisme du sexe plus proches des oiseaux que des Mammifères).
La comparaison de la séquence de quelques gènes homologues présents sur les chromosomes X et Y de différentes espèces actuelles a permis, à la lumière des connaissances relatives à la phylogénie de ces espèces, de proposer un ordonnancement des différents accidents dont leurs chromosomes sexuels ont été l’objet.
Une origine autosomique
Les chromosomes sexuels furent d’abord une paire d’autosomes tout à fait ordinaires, porteurs d’un millier de gènes, quand, il y a environ 300 millions d’années (Ma), une mutation dans le gène SOX3 produisit le gène SRY.
Le proto-Y naissait alors, tandis que son partenaire, toujours porteur de SOX3, devenait le proto-X.
Des inversions, des transpositions
Ces chromosomes ont ensuite été le siège d’une succession d’accidents :
-
des inversions se sont concentrées sur le chromosome Y, en dehors des extrémités (qui deviendront des PAR), empêchant dans ces régions les chromosomes X et Y de s’apparier, de se recombiner et donc de se réparer. Si la pression de sélection a conduit à la conservation de SRY (qui n’est pas sur les PAR), à l’inverse, beaucoup de gènes sont devenus ainsi non fonctionnels (pseudogènes) ou se sont même perdus.
-
des transpositions de fragments d’autosomes se sont produites, il y a 130 Ma, à la fois sur le X et sur le Y, elles ont rallongé ces chromosomes, leur permettant à nouveau de se réparer partiellement
-
elles ont été suivies d’inversions sur le Y, le rognant derechef
-
enfin, il y a 30 Ma, une expansion autosomale sur le seul Y lui a apporté le gène DAZ, gène dont la délétion provoque l’azoospermie (voir plus haut).
Au terme de ces tribulations le chromosome Y s’est ratatiné, passant, par exemple chez l’Homme, de un millier à environ 100 gènes.
Certains vont jusqu’à pronostiquer sa disparition totale d’ici 10 Ma…
Le chromosome Y humain à la lumière du séquençage
L’analyse a progressé magistralement quand, en 2003, David Page et ses 39 collaborateurs du Massachussets Institute of Technology (USA) ont présenté la séquence de presque toute l’euchromatine d’un Y humain, comparée à celle de quelques fragments équivalents du Chimpanzé, du Bonobo et du Gorille, lesquels ont divergé de la lignée humaine il y a environ 6 millions d’années (voir références 1 et 4).
Ce travail est notamment venu à bout de la grande richesse en séquences répétées de cette euchromatine (1 million de répétitions Alu par exemple !).
Pour un rappel sur les méthodes de séquençage, voir « Le séquençage d'un ADN ».
Les différents types de séquences du chromosome Y
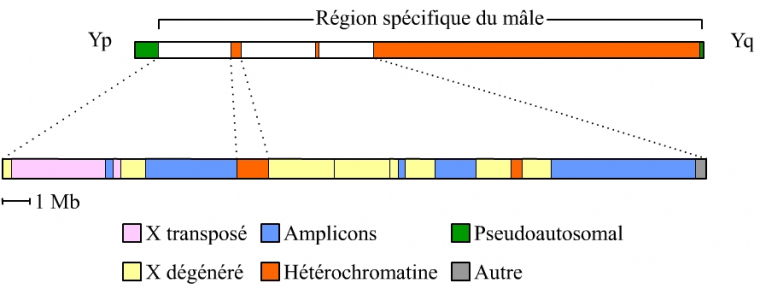
L’euchromatine du chromosome Y comprend trois types de séquences qui renseignent sur ce que fut l’évolution de ce chromosome et sur les fonctions qui sont les siennes aujourd’hui (voir figure ci-dessous) :
-
des séquences du chromosome X largement dégénérées, reliques des autosomes dont les chromosomes X et Y ont dérivé ; elles comprennent encore 16 gènes fonctionnels qui s’expriment dans toutes les cellules des deux sexes,
-
des séquences transposées récemment du chromosome X, il y a 3 à 4 Ma, donc après la divergence de l’Homme et des Gorilles, Chimpanzés et Bonobos ; elles comprennent 2 gènes fonctionnels.
-
des séquences acquises de diverses sources, puis amplifiées et pour cette raison nommées amplicons, qui contiennent 60 gènes fonctionnels dont l’expression est restreinte au testicule.
Ce sont ces amplicons, que seul le travail de séquençage permettait de discerner, qui ont changé du tout au tout l’idée que l’on se faisait des capacités du chromosome Y à se réparer.
Amplicons et palindromes
Les amplicons ont pour caractéristique de contenir deux ou quelques copies de gènes très homologues nécessaires à la fertilité mâle.
Ils sont bordés de séquences en miroir dont les deux éléments rassemblés constituent un palindrome, c’est-à-dire une séquence d’ADN qui se lit de la même façon dans les deux sens par rapport à un point central. Voici un exemple : deux séquences rencontrées successivement, GGTAC, puis CATGG, constituent ensemble le palindrome GGTAC - CATGG.
Le repliement l’une vers l’autre des deux séquences du palindrome produit une boucle qui met face à face les copies de gènes très homologues de l’amplicon, dont l’une peut être mutée et l’autre pas.
Les échanges de séquences selon le mécanisme de conversion transforment la version mutée en sa version non mutée, à l’intérieur même du chromosome Y donc, sans recours à la recombinaison homologue.
Bien sûr, à l’inverse, peut se produire la conversion du gène non muté en son équivalent muté ; mais on présage que cette double mutation court le risque d’être éliminée par sélection.
L’avenir du chromosome Y humain n’est donc, pour l’instant, pas si sombre que le prédisaient certains ! Pas plus d’ailleurs que celui des Gorilles, Chimpanzés et Bonobos chez qui des palindromes-amplicons similaires sont également à l’œuvre ; l’hypothèse la plus simple étant donc d’estimer que ces ensembles sont apparus avant la divergence des lignées humaine et simienne (référence 5).
Conclusion
L’histoire du chromosome Y humain, porteur notamment du gène SRY déterminant le sexe mâle, n’est pas de tout repos :
En 300 millions d’années, il a perdu les deux tiers de sa taille ; les inversions qu’il a connues à plusieurs reprises lui ont permis de garder le gène SRY sans le céder à son compagnon X, mais elles ont empêché en même temps de réparer maintes mutations sur d’autres portions du Y qui, dégénérant, ont été perdues, contribuant ainsi à le faire rétrécir (même si des transpositions autosomales ou provenant du X l’ont parfois un peu rallongé).
Mais malgré ce parcours mouvementé, le chromosome Y humain a fait la preuve de sa résistance : celle-ci est due à l’existence de palindromes-amplicons qui lui donnent la possibilité de corriger « en interne » les mutations qui affectent la fertilité mâle.
Résistance encore plus forte qu’on ne le pensait : le groupe de David Page a montré, en septembre 2005, que les gènes situés en dehors de ces zones résistaient mieux aux mutations chez l’Homme que chez le Chimpanzé (référence 6).
L’avenir du chromosome Y humain est-il assuré pour autant ? Le campagnol-taupe d’Arménie Ellobius lutescens nous enseigne que non, lui qui a perdu son Y et son gène SRY. Mâles et femelles devenus XO (le zéro indique l’absence de X ou de Y), sont pourtant parfaitement viables : chez le mâle, un autre gène, sur un autre chromosome, a dû prendre la relève de SRY ou de l’un des gènes sous sa commande.
L’histoire du chromosome Y n’est pas simple !
Bibliographie
-
Le chromosome Y humain
Charmot-Bensimon D. et Dudley K. Documents de cours (2005-2006) du Master BBSG de l’Université de la Méditerranée Aix-Marseille II. -
Sex chromosomes
Kimball J. -
La femme est l’avenir de l’homme. La Recherche juillet 2004
-
The male-specific region of the human Y chromosome is a mosaic of discrete sequence classes
Skaletsky et coll. (2003) Nature 423(6942) :825-837. -
Abundant gene conversion between arms of palindromes in human and ape Y chromosomes
Rozen S. et coll. (2003) Nature 423(6942) :873-876. -
Conservation of Y-linked genes during human evolution revealed by comparative sequencing in chimpanzee
Hughes J.F. et coll. Nature (2005) 437(7055) :100-103.
Merci aux membres du laboratoire Biologie et Multimédia pour leur relecture et commentaires.
Pour aller plus loin
- La différenciation du sexe, acquis et perspectives
Pannetier M. et Pailhoux E., 2011
- Sex determination and the control of Sox9 expression in mammals
Jakob S. and Lovell-Badge R., 2010
- Infertilité masculine de cause génétique et biologie moléculaire
Wallerand H., Bernardini S., Chabannes E., Bittard H., 2003
- L’étonnant chromosome Y
K. Jegalian et B. Lahn
Pour la science N°282, avril 2001
- Dossier pédagogique « Les déterminismes du sexe »
Équipe Access, 2001