Alors que l’on pensait la structure du cerveau fixe, la mise en évidence récente d’une production de nouvelles cellules dans le cerveau adulte a ouvert un tout nouveau champ d’investigation dans l’étude de la plasticité neuronale du cerveau adulte. Même si l’on connaît aujourd’hui mieux cette neurogenèse adulte, elle reste encore l’objet de nombreuses questions concernant son fonctionnement, sa régulation, ses fonctions mais aussi son éventuelle implication dans les maladies neurodégénératives.
Alors que l’on pensait la structure du cerveau fixe, la mise en évidence récente d’une production de nouvelles cellules dans le cerveau adulte a ouvert un tout nouveau champ d’investigation dans l’étude de la plasticité neuronale du cerveau adulte. Même si l’on connaît aujourd’hui mieux cette neurogenèse adulte, elle reste encore l’objet de nombreuses questions concernant son fonctionnement, sa régulation, ses fonctions mais aussi son éventuelle implication dans les maladies neurodégénératives.
Une petite histoire de la mise en évidence de la neurogenèse adulte
Pendant plus d’un siècle, il a été admis que la structure du cerveau adulte demeurait fixe et que les cellules nerveuses du cerveau n’étaient pas remplacées, contrairement aux autres cellules du corps. En effet, les techniques à disposition jusque dans les années 1950 ne permettaient pas d’observer des cellules en division dans le cerveau des mammifères adultes et l’architecture particulièrement élaborée du cerveau adulte rendait inenvisageable l’ajout de nouveaux neurones au sein de cette structure. On tenait donc pour dogme le fait que l’on naissait avec notre stock de neurones et que celui-ci ne faisait que décroître tout au long de la vie. Néanmoins, à la fin des années 1950, l’apparition d’une nouvelle méthode de détection de la division cellulaire – l’autoradiographie de la thymidine tritiée – a permis une avancée majeure dans la mise en évidence et l’analyse de la neurogenèse. En effet, la thymidine tritiée est un analogue radio-marqué de la thymidine qui s’incorpore à l’ADN lors de la réplication dans les cellules en division. Étant donné que ce composé est éliminé par l’organisme en quelques heures, son utilisation permet alors de dater la naissance des cellules marquées au moment de l’injection de cette molécule. Grâce à cette technique, une première série d’études réalisées chez le rat et le chat fut publiée dans les années 1960, montrant la présence de nouvelles cellules nerveuses dans différentes zones du cerveau (Altman, 1963, 1969; Altman and Das, 1965). Néanmoins, ces travaux sont restés largement ignorés car il n’était alors pas possible de déterminer sans ambiguïté l’identité neuronale ou gliale de ces cellules. Dans les années 70, l’apparition de techniques de microscopie électronique a permis de confirmer le statut neuronal des cellules en division dans le cerveau adulte (Kaplan and Hinds, 1977). Mais encore une fois, ces derniers travaux n’ont pas permis d’ébranler le dogme car l’idée de l’ajout de nouveaux neurones dans le cerveau adulte était en opposition complète avec la conception théorique de la nécessité d’une stabilité structurale des réseaux neuronaux, notamment pour le maintien à long terme de la mémoire. Différents facteurs ont finalement contribué à l’abolition de ce dogme au début des années 1990 : tout d’abord, la mise en évidence d’une neurogenèse adulte abondante chez l’oiseau, notamment chez le canari apprenant de nouveaux chants (Nottebohm, 2002) ; ensuite la mise en évidence de cellules souches adultes neurales dans le cerveau adulte de souris (Reynolds and Weiss, 1992) ; et enfin l’arrivée de nouvelles techniques de marquages qui permettent de distinguer les nouveaux neurones formés dans le cerveau adulte (Ming and Song, 2005). En effet, l’utilisation d’un nouvel analogue de la thymidine, la 5-bromo-2’-désoxyuridine (BrdU), qui s’incorpore spécifiquement dans l’ADN des cellules en division et qui présente l’avantage d’être facilement détectable par des techniques d’immunohistochimie, a permis d’identifier sans ambiguïté l’identité des cellules neuronales produites en microscopie. Aujourd’hui, l’existence d’une neurogenèse adulte est admise chez plusieurs espèces animales dont les Mammifères.
Qu’est-ce que la neurogenèse adulte ?
La neurogenèse adulte est la formation de nouveaux neurones au sein du cerveau adulte. Elle désigne l’ensemble des processus qui, à partir de la division des cellules souches neurales, donne naissance à des cellules capables de se différencier en neurones qui vont s’intégrer ensuite dans les circuits cérébraux existants.
La neurogenèse adulte, une caractéristique commune à de nombreuses espèces
La neurogenèse adulte est un processus que l’on retrouve chez de nombreuses espèces du règne animal, des invertébrés, incluant de nombreux Insectes (Orthoptères, Coléoptères et drosophiles) et les crustacés, aux Vertébrés, incluant les poissons, les Amphibiens, les reptiles, les Oiseaux et les Mammifères (Nottebohm, 2002; Raucci et al., 2006; Kaslin et al., 2008). Chez ces derniers, la neurogenèse adulte a été initialement mise en évidence chez le rat et le chat dans les années 1960, données ensuite confirmées chez le rat et les Primates dans les années 1980. Depuis, elle a été montrée dans le cerveau de nombreuses espèces de Mammifères : les rongeurs (souris, rat, cochon d’Inde, campagnol des prés, écureuil, rat taupe), les Scandentiens (petits mammifères arboricoles, incluant les toupayes), les hérissons, les taupes, les renards, les éléphants, les loutres, les chauves-souris, les lapins, les vaches, les chiens, les moutons (Amrein et al., 2011, 2015), mais également chez les singes (Gould et al., 1999; Kornack and Rakic, 2001) dont l’espèce humaine. L’étude de la neurogenèse adulte chez l’Homme est bien plus délicate pour des raisons liées à des limitations méthodologiques. Même si la présence d’une neurogenèse humaine adulte a été confirmée en utilisant la BrdU (Eriksson et al., 1998), la quantification du niveau de neurogenèse reste approximative (Bergmann et al., 2015). Chez le rat jeune, il a été montre qu’environ 9 000 cellules sont produites par jour ce qui représente quotidiennement moins de 1 % de la population totale des neurones (aussi appelés cellules granulaires) du gyrus denté. Récemment, une étude exploitant la hausse de carbone radioactif dans l’atmosphère suite aux essais nucléaires hors-sol des années 50 a permis de montrer chez l’Homme qu’environ 700 nouveaux neurones sont ajoutés chaque jour dans l’hippocampe (Spalding et al., 2013), une structure essentielle dans la mémoire, soit un taux non négligeable de renouvellement de 1,75% par an des cellules granulaires de cette structure. Bien que la neurogenèse adulte soit présente chez une grande majorité des Mammifères, elle se fait dans des proportions plus ou moins importantes selon les espèces.
Les zones de neurogenèse dans le cerveau adulte
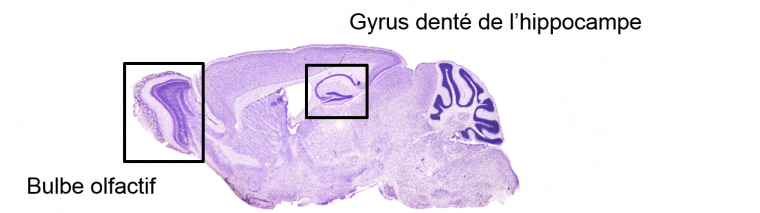
Depuis sa découverte dans le cerveau adulte des Mammifères, il a été montré que la neurogenèse est principalement confinée dans deux structures du cerveau chez ceux-ci (figure 1) : le bulbe olfactif, premier relais central de l’information olfactive, et l’hippocampe, structure essentielle dans la mémoire.
Exemple chez le rongeur. Les zones de neurogenèse adulte principales sont l’hippocampe et le bulbe olfactif. Coupe sagittale de cerveau de rats. Coloration de Nissl (crésyl violet) qui permet de mettre en évidence les neurones.
À l’origine, des cellules souches neurales
Dans le cerveau adulte, les nouvelles cellules nerveuses sont produites à partir de cellules souches neurales. Ce sont des cellules de nature gliale et plus précisément astrocytaire, qui sont caractérisées par :
- Leur capacité d’auto-renouvellement c’est-à-dire la capacité de proliférer et de générer au moins une cellule-fille présentant les mêmes caractéristiques morphologiques, biochimiques et fonctionnelles que la cellule-mère, par division symétrique ou asymétrique.
- Leur nature multipotente c’est-à-dire leur aptitude à produire les trois types cellulaires que l’on trouve dans le cerveau : neurones, astrocytes et oligodendrocytes.
Dans l’hippocampe, les données montrent une hétérogénéité de la nature des cellules à l’origine de la neurogenèse adulte. En effet, il semble que les cellules souches du gyrus denté de l’hippocampe présentent une capacité d’auto-renouvellement réduite contrairement aux cellules souches du bulbe olfactif. (Bonaguidi et al., 2011, 2012).
D’une cellule souche à un neurone mature
Que ce soit pour la neurogenèse olfactive ou hippocampique, les nouvelles cellules sont produites dans des zones spécifiques, appelés niches neurogéniques. Il s’agit de la zone sous-ventriculaire bordant les ventricules latéraux et qui alimente le bulbe olfactif en nouvelles cellules et de la zone sous-granulaire du gyrus denté de l’hippocampe. L’architecture et le fonctionnement de ces zones constituent un microenvironnement favorable à la production de nouvelles cellules (Zhao et al., 2008; Aimone et al., 2014; Crowther and Song, 2014). Ces niches neurogéniques sont composées de :
- Cellules : cellules endothéliales (cellules des vaisseaux sanguins), oligodendrocytes (cellule gliale), différents types de neurones et d’astrocytes (cellule gliale).
- Facteurs spécifiques : facteurs de croissance, neurotransmetteurs, facteurs épigénétiques.
Cet environnement particulier est nécessaire à la prolifération, la différenciation, la migration et à l’intégration fonctionnelle des nouveaux neurones au sein des réseaux neuronaux du cerveau. Cet ensemble de caractéristiques cellulaires et moléculaires font de ces niches des environnements uniques pour la production de nouvelles cellules.
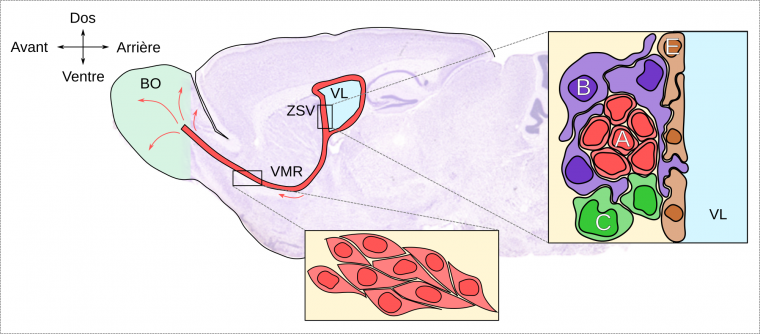
Concernant le bulbe olfactif, les nouvelles cellules sont d’abord produites dans la zone sous-ventriculaire (ZSV) à partir des cellules souches (cellule de type B, figure 2, médaillon de droite) qui prolifèrent. Ces cellules donnent naissance à des cellules progénitrices transitoires (cellule de type C, figure 2), elles-mêmes capables de proliférer et de se différencier en neuroblastes (figure 2). Chez les rongeurs, la zone sous-ventriculaire est la source la plus importante de nouvelles cellules dans le cerveau adulte avec plusieurs dizaines de milliers de cellules générées quotidiennement. Ces nouvelles cellules migrent ensuite le long de la voie de migration rostrale (VMR, figure 2, médaillon du bas), sur plusieurs millimètres, pour atteindre le bulbe olfactif où ils achèvent leur processus de maturation et deviennent majoritairement des interneurones GABAergique, et pour une très faible proportion en neurones dopaminergique (5 %). Ces nouveaux neurones fonctionnels s’intègrent alors dans les circuits préexistants du bulbe olfactif pour participer à son fonctionnement.
Légende : Coupe sagittale d’un cerveau de rongeur. Les neuroblastes produits dans la zone sous-ventriculaire (ZSV) s’engagent dans un processus de différenciation neuronale tout en migrant vers le bulbe olfactif (BO) via la voie de migration rostrale (VMR, médaillon du bas). Une fois arrivés au niveau du bulbe olfactif, les nouveaux neurones s’intègrent au sein des réseaux neuronaux préexistants. VL : ventricule latéral.
Médaillon de droite. La ZSV est constituée de 4 types cellulaires : les cellules épendymaires (E) qui participent à la formation de la paroi des ventricules latéraux (VL), les cellules souches de type B (se divisant lentement), les cellules de type C (se divisant plus rapidement) et les neuroblastes (cellules de type A). Dans cette niche neurogénique, les cellules astrocytaires de type B établissent des contacts étroits avec l’ensemble des autres types cellulaires de la niche, ainsi qu’avec le milieu ventriculaire. Les cellules de type B présentent les caractéristiques des cellules souches neurales et donnent naissance aux cellules de type C qui à leur tour produisent des cellules de type A.
Adapté en partie du travail d’Oscar Arias-Carrión, Wikimedia, licence CC-BY
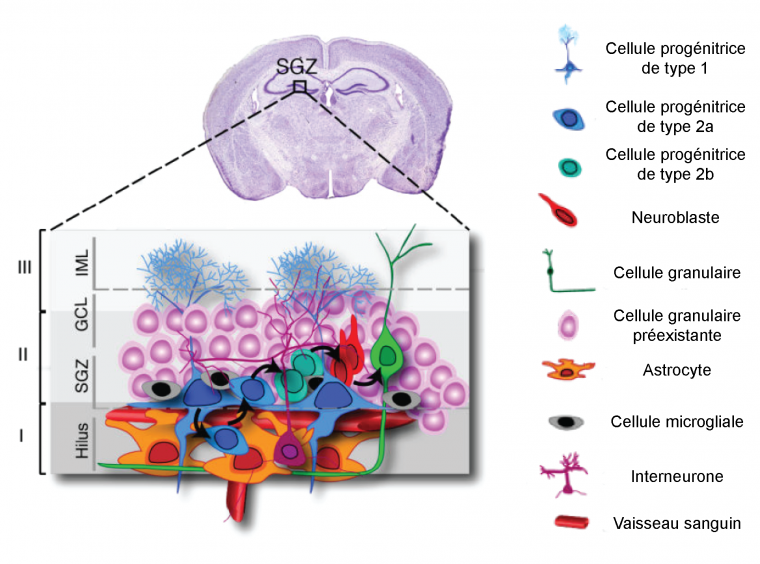
Dans l’hippocampe, la neurogenèse adulte prend son origine dans la zone sous-granulaire (SGZ) du gyrus denté (GD) à partir de cellules souches/progénitrices (cellules dites de type 1, figure 3). Après prolifération, ces cellules donnent naissance à une population de cellules progénitrices transitoires (cellules dites de type 2, figure 3) capables de proliférer abondamment et de se différencier en neuroblastes. Les cellules nouvellement formées migrent sur une courte distance (jusqu’à 200 µm) dans la partie interne de la couche granulaire du gyrus denté où elles achèvent leur processus de maturation pour devenir majoritairement (60 à 80 %) des cellules granulaires intégrées aux réseaux préexistants (figure 4). Environ 15 % des cellules se différencient en cellules GABAergiques et environ 10 % se différencient en cellules gliales, majoritairement en astrocytes, mais également en cellules microgliales. Dans l’hippocampe, les cellules produites restent dans cette structure pour participer à ses fonctions, notamment de mémorisation.
Légende : Haut : coupe coronale de cerveau de rongeurs (coloration de Nissl). Bas : La niche neurogénique est constituée d’astrocytes, de cellules microgliales, d’interneurones et de vaisseaux sanguins fournissant l’environnement nécessaire au maintien, à la prolifération et à la différenciation des cellules progénitrices. IML : inner molecular layer, GCL : granular cell layer, SGZ : sub-granular zone. Modifié d'après Donegà et al., 2013.
La production de nouvelles cellules a également été mise en évidence dans d’autres régions cérébrales telles que certaines aires du cortex, l’amygdale, le striatum, la substance noire, le complexe vagal ou encore l’hypothalamus, mais aussi dans la moelle épinière (Emsley et al., 2005; Inta et al., 2015; Li et al., 2015). Néanmoins, à l’heure actuelle, ces zones ne sont pas considérées comme étant neurogéniques car la production de nouvelles cellules dans ces régions est détectée seulement après un stress ou des manipulations pharmacologiques et leurs persistances à long terme restent controversées en conditions basales. De plus, la présence de cellules souches au sein de ces structures n’est à ce jour pas démontrée.
La neurogenèse adulte, une histoire de maturation, de survie et d’intégration
Le processus de maturation se traduit par la maturation morphologique des nouveaux neurones avec notamment la croissance des prolongements dendritiques et de l’axone, la maturation électrophysiologique des neurones, la mise en place des connexions synaptiques et ainsi leur intégration au sein des réseaux neuronaux préexistants (figures 2 et 4). Les nouvelles cellules produites subissent également un processus drastique de sélection au cours des quatre premières semaines après leur naissance et seule une faible proportion d’entre elles survit à long terme, les autres étant éliminées par apoptose (entre 50 et 70 %). Cette survie des nouveaux neurones est dépendante de leur intégration au sein des réseaux neuronaux préexistant et notamment de l’activité synaptique. Les nouveaux neurones présentent des caractéristiques morphologiques et électrophysiologiques fonctionnelles dès l’âge de deux ou trois semaines mais poursuivent leur maturation jusqu’à l’âge de quatre mois où ils présentent alors une morphologie complètement similaire à celle des cellules préexistantes. Le passage d’un neurone immature à un nouveau neurone mature complètement fonctionnel, indissociable d’un autre neurone mature du gyrus denté, est un mécanisme complexe comprenant de nombreuses étapes essentielles à la maturation et à la parfaite intégration des nouveaux neurones au sein des réseaux neuronaux de la structure dans laquelle ils s’intègrent (Aimone et al., 2014; Lepousez et al., 2015).
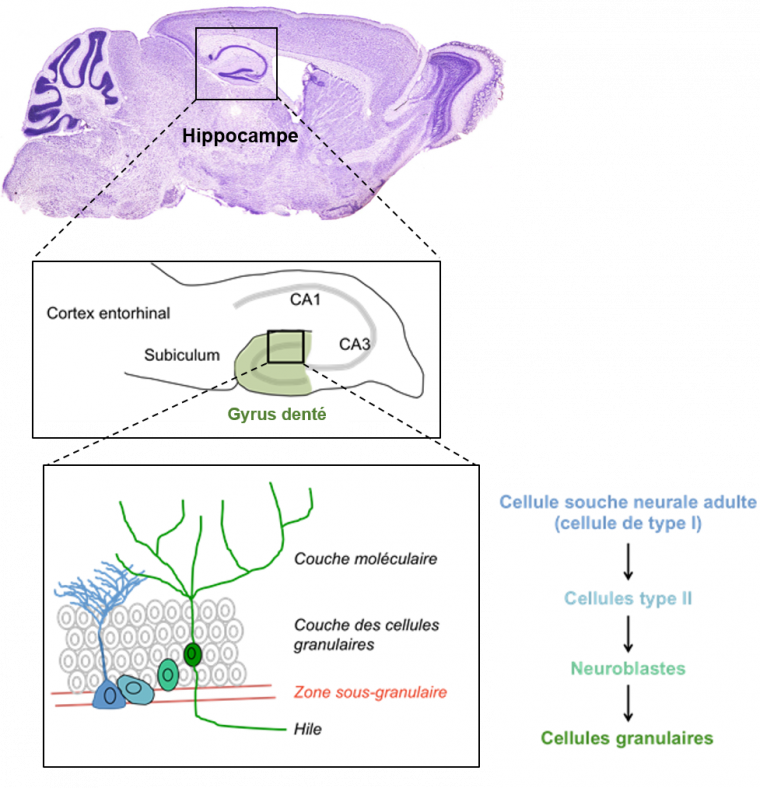
Haut : La neurogenèse adulte hippocampique se produit dans l’hippocampe, structure essentielle dans les processus de mémoire.
Milieu : Schéma de l’hippocampe. Les nouvelles cellules sont produites dans la zone sous-granulaire du gyrus denté de l’hippocampe, qui est une sous-partie de l’hippocampe (en vert). CA = champs ammoniens, qui sont des sous structures de l’hippocampe.
Bas : Gyrus denté de l’hippocampe. Les cellules souches neurales se divisent afin de donner naissance aux neuroblastes, qui deviennent matures et migrent au sein de la couche granulaire du GD puis sont sélectionnées pour s’intégrer au sein des réseaux neuronaux préexistants.
La régulation de la neurogenèse adulte
Les différentes étapes de la neurogenèse adulte, depuis la prolifération des cellules progénitrices jusqu’à la maturation et l’intégration fonctionnelle des nouveaux neurones au sein des réseaux neuronaux hippocampiques sont finement régulées (Abrous et al., 2005; Lledo et al., 2006; Aimone et al., 2014; Egeland et al., 2015). De nombreux facteurs régulent positivement ou négativement la neurogenèse adulte indiquant qu’il s’agit d’un mécanisme adaptatif en réponse aux modifications de l’environnement. On distingue les facteurs intrinsèques, produits directement par les cellules progénitrices et/ou nouvellement formées, des facteurs extrinsèques présents dans le milieu extracellulaire de la niche neurogénique. On trouve dans les facteurs intrinsèques, les facteurs génétiques (fond génétique et programmes cellulaires intrinsèques), les facteurs épigénétiques (méthylation de l’ADN, modifications post-traductionnelles des histones et régulation/expression d’ARN non codants dont les microARN) ainsi que les facteurs de transcription. Parmi les facteurs extrinsèques présents dans le milieu extracellulaire de la niche neurogénique et régulant la neurogenèse, on trouve les neuromédiateurs (glutamate, GABA, sérotonine, acétylcholine, noradrénaline et dopamine), les hormones (hormones stéroïdes sexuelles, corticostéroïdes et hormones thyroïdiennes), les facteurs de croissance, les drogues (nicotine, opiacés et cocaïne ainsi que l’alcool) ou encore les stimulations environnementales (stress, environnement enrichi, activité physique volontaire).
Les fonctions de la neurogenèse adulte
La fonction des nouveaux neurones dans le cerveau adulte a été évaluée d’une part en utilisant des techniques de blocage de la production des nouveaux neurones (antimitotiques qui empêchent la division des cellules souches, irradiation qui entraîne des dommages dans les cellules en division et bloque la neurogenèse, modèles génétiques dans lesquelles la production de nouvelles cellules est inhibée), ou au contraire en l’augmentant via des modèles génétiques, suite à l’exposition à un environnement enrichi ou à une période d’exercice physique (Aimone et al., 2014). Différentes fonctions et processus cérébraux ont ensuite été analysés à l’aide de ces modèles variés. La majorité des études montre un rôle de la neurogenèse adulte hippocampique dans les processus d’apprentissage et de mémoire dépendante de l’hippocampe (discrimination fine entre deux situations proches, mémoire spatiale, de travail, de peur, et même épisodique) (Dupret and Abrous, 2010; Sahay et al., 2011; Aimone et al., 2014; Gros et al., 2015), ainsi qu’un rôle de la neurogenèse adulte olfactive dans les apprentissages olfactifs (apprentissage perceptifs, mémorisation de nouvelles odeurs, représentation olfactive, discrimination fine entre différentes odeurs proches) (Lledo et al., 2006; Lepousez et al., 2015). Globalement, l’absence ou la diminution de neurogenèse perturbe fortement ces différents processus alors que l’enrichissement et l’exercice qui augmentent la production de nouveaux neurones, les améliorent. Par ailleurs, l’exercice ainsi que l’apprentissage et la mémorisation modifient le nombre de nouveaux neurones produits ainsi que leur survie, leur maturation morphologique et leur intégration au sein des réseaux neuronaux, indiquant que les nouveaux neurones participent à ces processus. De plus, les nouveaux neurones présentent une période critique au cours de leur maturation (entre une et quatre semaines après leur naissance chez les rongeurs) où ils sont plus susceptibles de participer aux processus d’apprentissage et de mémorisation, du fait de certaines particularités électrophysiologiques telle qu’une plus grande excitabilité par des stimuli même de faible intensité (Aasebø et al., 2011). L’intégration permanente de nouveaux neurones au sein des réseaux neuronaux du bulbe olfactif et de l’hippocampe permet aux systèmes d’être très plastiques, et ainsi de s’adapter à de nouveaux environnements.
La neurogenèse adulte au cours du vieillissement
Bien que la neurogenèse adulte persiste tout au long de la vie, c’est un processus fortement sensible au vieillissement (Drapeau and Abrous, 2008; Aimone et al., 2014; Dennis et al., 2016). La production de nouveaux neurones diminue avec l’âge chez les rongeurs tout comme chez les singes. Chez les rongeurs, la prolifération et la survie des cellules progénitrices diminue dès l’âge de 2 à 5 mois jusqu’à l’âge de 10 à 12 mois puis se stabilise jusqu’à l’âge de 24 à 27 mois. La diminution de la neurogenèse adulte est aussi associée à une altération de la morphologie dendritique, une diminution de la migration et une diminution de la différenciation neuronale au profit d’une augmentation de la différenciation gliale des cellules nouvellement formées. Une diminution de la neurogenèse est également observée chez l’humain. Cette diminution de la neurogenèse adulte au cours du vieillissement pourrait être expliquée par des modifications locales et environnementales des niches neurogéniques.
Neurogenèse adulte hippocampique et maladies neuronales
Étant donné le rôle des nouveaux neurones dans l’apprentissage et la mémorisation ainsi que l’altération des processus de neurogenèse adulte au cours du vieillissement normal, se pose la question de l’impact de cette altération lors du vieillissement pathologique, notamment avec l’apparition des maladies neurodégénératives telles que la maladie d’Alzheimer (Winner et al., 2011). Il a été montré une forte diminution de la neurogenèse adulte hippocampique chez des humains atteints de la maladie d’Alzheimer, tout comme chez les modèles animaux de cette maladie. Cette diminution de la neurogenèse adulte pourrait participer aux déficits mnésiques associés à cette maladie. De plus, l’augmentation de la neurogenèse adulte hippocampique dans des modèles rongeurs de la maladie, permet d’améliorer les performances mnésiques (Richetin et al., 2014). Il existe également un lien entre neurogenèse adulte et dépression (Sahay and Hen, 2007). En effet, la sérotonine impliquée dans la dépression, influence la prolifération des cellules progénitrices et la survie des cellules nouvellement formées. La majorité des traitements de la dépression stimule la neurogenèse adulte hippocampique mais le blocage de la neurogenèse adulte n’entraîne pas nécessairement d’état dépressif chez les modèles animaux. De nombreuses études suggèrent donc que la neurogenèse adulte pourrait être un des substrats possibles de l’action antidépresseur des traitements parmi d’autres mécanismes d’action. De même, de récentes études s’interrogent sur le lien entre neurogenèse adulte et le stress post-traumatique (Kheirbek et al., 2012; Besnard and Sahay, 2015), l’addiction (Canales, 2007), l’épilepsie (Jessberger and Parent, 2015), la maladie de Huntington, la maladie de Parkinson (rôle de la dopamine) ou d’autres troubles neurologiques. Certaines recherches s’intéressent aux propriétés de renouvellement de la neurogenèse adulte avec de potentielles applications dans la médecine régénérative en cas de perte neuronale comme c’est le cas après une lésion ou un AVC par exemple. Le lien entre neurogenèse adulte et maladies du système nerveux reste encore largement méconnu et fait l’objet de nombreuses études afin de mieux comprendre le rôle de la neurogenèse et l’impact de sa modulation au cours du vieillissement normal ou pathologique.
Références
- Aasebø IEJ, Blankvoort S, Tashiro A (2011) Critical maturational period of new neurons in adult dentate gyrus for their involvement in memory formation. Eur J Neurosci 33:1094–1100.
- Abrous DN, Koehl M, M.L. M (2005) Adult Neurogenesis: From Precursers to Network and Physiology. Physiol Rev 85:523–569.
- Aimone JB, Li Y, Lee SW, Clemenson GD, Deng W, Gage FH (2014) Regulation and Function of Adult Neurogenesis: From Genes to Cognition. Physiol Rev 94:991–1026
- Altman J (1963) Autoradiographic Investigation of Cell Proliferation in the Brains of Rats and Cats. Anat Rec 145:573–591.
- Altman J (1969) Autoradiographic and histological studies of postnatal neurogenesis. IV. Cell proliferation and migration in the anterior forebrain, with special reference to persisting neurogenesis in the olfactory bulb. J Comp Neurol 137:433–457
- Altman J, Das GD (1965) Autoradiographic and histological evidence of postnatal hippocampal neurogenesis in rats. J Comp Neurol 124:319–335.
- Amrein I, Isler K, Lipp H-P (2011) Comparing adult hippocampal neurogenesis in mammalian species and orders: influence of chronological age and life history stage. Eur J Neurosci 34:978–987
- Amrein I, Lipp H-P, Boonstra R, Wojtowicz JM (2015) Adult Hippocampal Neurogenesis in Natural Populations of Mammals. Cold Spring Harb Perspect Biol 7.
- Bergmann O, Spalding KL, Frise J (2015) Adult Neurogenesis in Humans. Cold Spring Harb Perspect Biol 7:1–12.
- Besnard A, Sahay A (2015) Adult Hippocampal Neurogenesis, Fear Generalization, and Stress. Neuropsychopharmacol Rev 41:24–44
- Bonaguidi MA, Song J, Ming GL, Song H (2012) A unifying hypothesis on mammalian neural stem cell properties in the adult hippocampus. Curr Opin Neurobiol 22:754–761
- Bonaguidi MA, Wheeler MA, Shapiro JS, Stadel RP, Sun GJ, Ming G-L, Song H (2011) In Vivo Clonal Analysis Reveals Self-Renewing and Multipotent Adult Neural Stem Cell Characteristics. Cell 145:1142–1155
- Canales JJ (2007) Adult neurogenesis and the memories of drug addiction. Eur Arch Psychiatry Clin Neurosci 257:261–270.
- Crowther AJ, Song J (2014) Activity-dependent signaling mechanisms regulating adult hippocampal neural stem cells and their progeny. Neurosci Bull 30:542–556
- Dennis C V, Suh LS, Rodriguez ML, Kril JJ, Sutherland GT (2016) Human adult neurogenesis across the ages: An immunohistochemical study. Neuropathol Appl Neurobiol 42:621–638.
- Donegà M, Giusto E, Cossetti C, Pluchino S (2013) Systemic Neural Stem Cell-Based Therapeutic Interventions for Inflammatory CNS Disorders Bonfanti L, ed. Intech:Chapter 11.
- Drapeau E, Abrous DN (2008) Stem Cell Review Series: Role of neurogenesis in age-related memory disorders. Aging Cell 7:569–589.
- Dupret D, Abrous DN (2010) Un nouveau chapitre dans le domaine de la mémoire : la néo-neurogenèse hippocampique. Biol Aujourdhui 204:113–129.
- Egeland M, Zunszain PA, Pariante CM (2015) Molecular mechanisms in the regulation of adult neurogenesis during stress. Nat Rev Neurosci 16:189–200
- Emsley JG, Mitchell BD, Kempermann G, Macklis JD (2005) Adult neurogenesis and repair of the adult CNS with neural progenitors, precursors, and stem cells. Prog Neurobiol 75:321–341
- Eriksson PS, Perfilieva E, Björk-Eriksson T, Alborn AM, Nordborg C, Peterson DA, Gage FH (1998) Neurogenesis in the adult human hippocampus. Nat Med 4:1313–1317.
- Gould E, Reeves AJ, Graziano MSA, Gross CG (1999) Neurogenesis in the neocortex of adult primates. Science (80- ) 286:548–552
- Gros A, Veyrac A, Laroche S (2015) Cerveau et mémoire : des nouveaux neurones pour se souvenir. Biol Aujourdhui 209:229–248
- Inta D, Cameron HA, Gass P (2015) New neurons in the adult striatum: from rodents to humans. Trends Neurosci 38:517–523
- Jessberger S, Parent JM (2015) Epilepsy and adult neurogenesis. Cold Spring Harb Perspect Biol 7.
- Kaplan MS, Hinds JW (1977) Neurogenesis in the adult rat: electron microscopic analysis of light radioautographs. Science (80- ) 197:1092–1094.
- Kaslin J, Ganz J, Brand M (2008) Proliferation, neurogenesis and regeneration in the non-mammalian vertebrate brain. Philos Trans R Soc Lond B Biol Sci 363:101–122
- Kheirbek MA, Klemenhagen KC, Sahay A, Hen R (2012) Neurogenesis and generalization: a new approach to stratify and treat anxiety disorders. Nat Neurosci 15:1613–1620
- Kornack DR, Rakic P (2001) The generation, migration, and differentiation of olfactory neurons in the adult primate brain. Proc Natl Acad Sci U S A 98:4752–4757
- Lepousez G, Nissant A, Lledo PM (2015) Adult neurogenesis and the future of the rejuvenating brain circuits. Neuron 86:387–401
- Li Q-Q, Qiao G-Q, Ma J, Fan H-W, Li Y-B (2015) Cortical neurogenesis in adult rats after ischemic brain injury: most new neurons fail to mature. Neural Regen Res 10:277–285
- Lledo P-M, Alonso M, Grubb MS (2006) Adult neurogenesis and functional plasticity in neuronal circuits. Nat Rev Neurosci 7:179–193.
- Ming G, Song H (2005) Adult neurogenesis in the mammalian central nervous system. Annu Rev Neurosci 28:223–250
- Nottebohm F (2002) Neuronal replacement in adult brain. Brain Res Bull 57:737–749 Available at: http://linkinghub.elsevier.com/retrieve/pii/S0361923002007505.
- Raucci F, Di Fiore MM, Pinelli C, D’Aniello B, Luongo L, Polese G, Rastogi RK (2006) Proliferative activity in the frog brain: a PCNA-immunohistochemistry analysis. J Chem Neuroanat 32:127–142
- Reynolds BA, Weiss S (1992) Generation of neurons and astrocytes from isolated cells of the adult mammalian central nervous system. Science (80- ) 255:1707–1710.
- Richetin K, Leclerc C, Toni N, Gallopin T, Pech S, Roybon L, Rampon C (2014) Genetic manipulation of adult-born hippocampal neurons rescues memory in a mouse model of Alzheimer’s disease. Brain 138:440–455
- Sahay A, Hen R (2007) Adult hippocampal neurogenesis in depression. Nat Neurosci 10:1110–1115.
- Sahay A, Wilson DA, Hen R (2011) Pattern Separation: A Common Function for New Neurons in Hippocampus and Olfactory Bulb. Neuron 70:582–588.
- Spalding KL, Bergmann O, Alkass K, Bernard S, Salehpour M, Huttner HB, Boström E, Westerlund I, Vial C, Buchholz B a, Possnert G, Mash DC, Druid H, Frisén J (2013) Dynamics of hippocampal neurogenesis in adult humans. Cell 153:1219–1227
- Winner B, Kohl Z, Gage FH (2011) Neurodegenerative disease and adult neurogenesis. Eur J Neurosci 33:1139–1151.
- Zhao C, Deng W, Gage FH (2008) Mechanisms and functional implications of adult neurogenesis. Cell 132:645–660.