Présentation des méthodes utilisées pour obtenir de nouvelles variétés végétales. Lumière sur l'utilisation de lignées inductrices chez le maïs et sur l'origine génétique de telles lignées.
Cet article est publié sous le DOI : 10.15454/1.4963001229144182E12
Importance de la création variétale
L’agriculture contemporaine doit faire face à de nombreux défis, comme ceux d’assurer une production alimentaire de qualité et de s’adapter aux effets du changement climatique, tout en diminuant son empreinte environnementale. Elle doit être réactive à des évolutions plus rapides qu’auparavant et imprévisibles, comme l’apparition de nouveaux pathogènes ou des amplitudes plus importantes des fluctuations climatiques. Un nouvel enjeu de l’agriculture du XXIe siècle est donc sa capacité à fournir des variétés adaptées à ces changements, ce qui passe entre autres par l’innovation variétale. Une variété représente une population homogène ayant des caractéristiques agronomiques bien définies, et créée en vue de son utilisation en agriculture. La création de nouvelles variétés résistantes aux maladies permet déjà de réduire l’utilisation des produits phytosanitaires ; les variétés présentant une utilisation plus efficace des nutriments aident à réduire le recours aux produits fertilisants ; et celles présentant des rendements stables sous contraintes environnementales fortes sont un outil de choix pour faire face au changement climatique.
Sélection phénotypique, lignées pures et hybrides
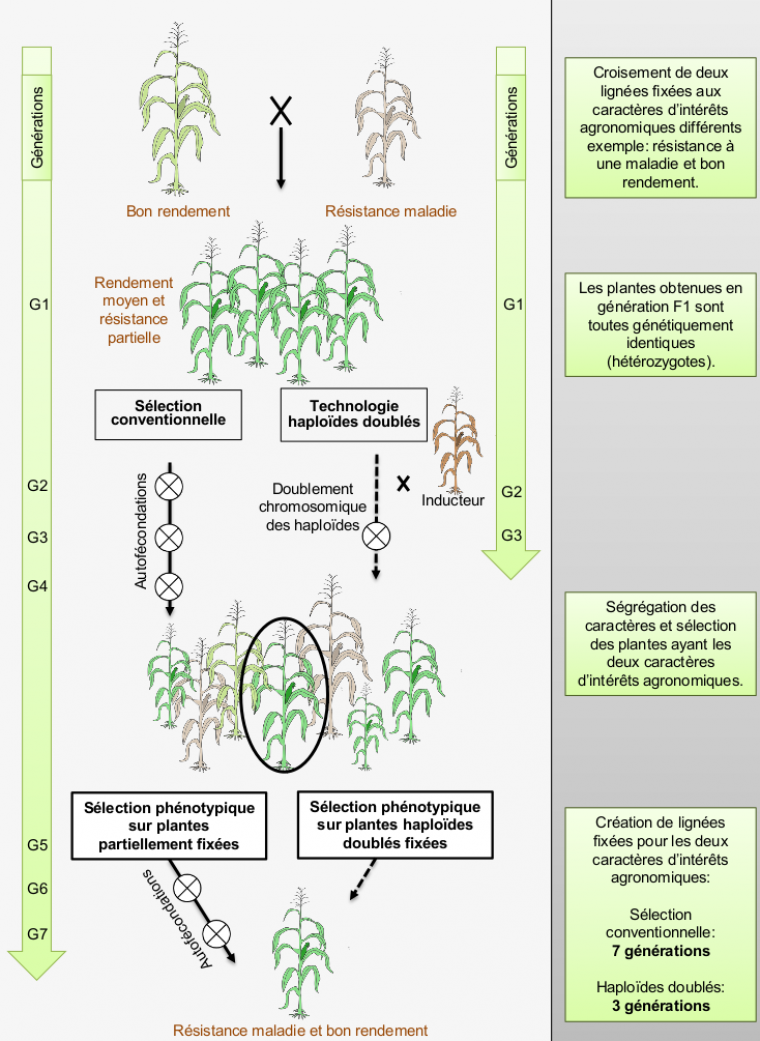
Dans le processus de la création variétale, un sélectionneur va dans un premier temps essayer de regrouper des propriétés agronomiques désirées dans une seule plante. Ceci est réalisé en croisant des plantes avec des propriétés différentes, puis en choisissant dans la descendance les individus combinant les caractères les plus intéressants : c’est la sélection phénotypique (Figure 1). Le sélectionneur souhaite fixer ces caractères afin d’obtenir une stabilité des caractères agronomiques au fil des générations. Pour cela, il crée des lignées pures ou lignées fixées. Ces lignées fixées sont utilisées en tant que telles ou comme parents afin d’obtenir des plantes dites hybrides. Ainsi le croisement de deux lignées fixées possédant chacune des caractères d’intérêts agronomiques particuliers, peut donner des plantes hybrides de performances supérieures aux deux plantes parents. C’est ce que l’on nomme la « vigueur hybride » ou hétérosis.
Obtention de lignées fixées
La méthode classique pour obtenir des lignées fixées repose en général sur la réalisation d’autofécondations successives. Ainsi après 7 générations successives, on atteint l’état d’un génome fixé, c’est-à-dire que plus de 99 % des gènes se trouvent à l’état homozygote (mêmes allèles sur les chromosomes paternel et maternel) (Figure 1).
Une autre méthode pour obtenir des lignées fixées repose sur l’utilisation de plantes haploïdes doublées. Elle se base sur l’obtention de plantes haploïdes qui ne possèdent qu’un seul exemplaire de chaque chromosome (maternel ou paternel). L’application d’agents chimiques qui bloquent la division cellulaire permet de « copier-coller » chaque chromosome présent dans la plante haploïde, et donc d’aboutir à une plante dite haploïde doublée. La colchicine est un exemple d’agent chimique fréquemment utilisé qui bloque la métaphase de la mitose. Ce doublement chromosomique du génome haploïde permet donc la création rapide d’une lignée pure, puisque tous les gènes se trouvent en deux copies identiques, c’est-à-dire à l’état homozygote en deux générations seulement (Figure 1).
Obtention de plantes haploïdes
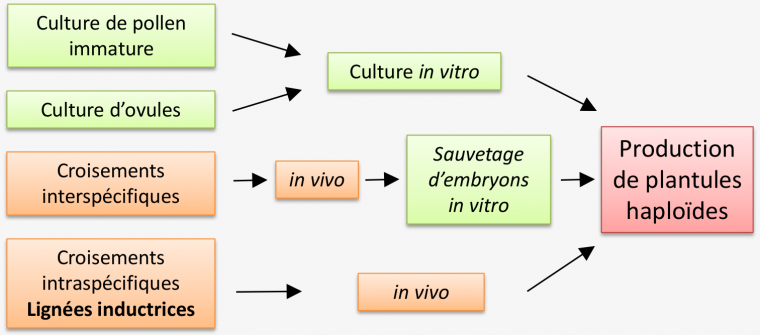
Plusieurs possibilités existent afin d’obtenir des plantes haploïdes (Figure 2). La méthode la plus fréquente repose sur la culture in vitro de tissus haploïdes, c’est-à-dire du gamétophyte mâle (pollen immature) ou femelle (sac embryonnaire). La culture in vitro permet de régénérer un embryon qui possède un génome haploïde, qui se développera en plante haploïde. Cela passe par la dédifférenciation du gamétophyte (mâle ou femelle) puis sa redifférenciation vers le stade embryon grâce à l’utilisation de cocktails d’hormones végétales et de conditions de culture in vitro particulières à chaque espèce et génotype. Il est aussi possible pour certaines espèces de réaliser des croisements interspécifiques, qui consistent à féconder l’oosphère de l’espèce d’intérêt avec le pollen d’une autre espèce. Les chromosomes paternels sont progressivement éliminés, mais ceci est suffisant pour déclencher un développement d’un embryon haploïde ayant uniquement les chromosomes maternels. Enfin, une autre possibilité pour la création in vivo de plantes haploïdes est l’utilisation de lignées particulières appelées « plantes inductrices ». Ce processus n’est pour l’instant connu que chez le maïs, car des plantes inductrices n’existent naturellement que chez cette espèce. Un croisement avec le pollen d’une lignée inductrice sur l’épi de n’importe quelle autre lignée (généralement non inductrice) entraîne le développement de l’oosphère en embryon haploïde. Les embryons ou plantules haploïdes doivent être doublés chimiquement pour donner des plantes haploïdes doublées contenant uniquement du matériel génétique de la plante mère. Cette induction d’haploïdes in vivo est un outil puissant de sélection car il requiert moins de travail, et donc un coût moindre, comparé aux systèmes qui nécessitent de la culture in vitro (Figure 2).
L’origine génétique du caractère inducteur
Ces plantes inductrices sont actuellement très largement utilisées comme outil dans les schémas de sélection du maïs afin de produire rapidement des lignées fixées. Cependant, les mécanismes cellulaires et moléculaires sous-jacents restent inconnus. Nos travaux de recherche, qui visent à comprendre comment un pollen provenant de plantes inductrices déclenche le développement d’une cellule œuf en embryon haploïde, nous ont récemment permis d’identifier un gène majeur intervenant dans ce processus (Gilles et al., 2017). Nous avons baptisé ce gène « Not Like Dad » (=NLD), ce qui se traduit par « pas comme papa », puisque l’information génétique du père ne se retrouve pas dans la descendance. Nous avons identifié une mutation dans ce gène qui est responsable de l’induction de plantes haploïdes (Figure 3). Cette mutation est présente dans toutes les lignées inductrices et absente dans toutes les autres lignées de maïs analysées. Une preuve de l’implication de ce gène NLD dans l’induction de plantes haploïdes a été apportée par l’expérimentation suivante : l’ajout du gène NLD intact à une lignée inductrice entraîne la perte de la capacité d’induction d’haploïde.
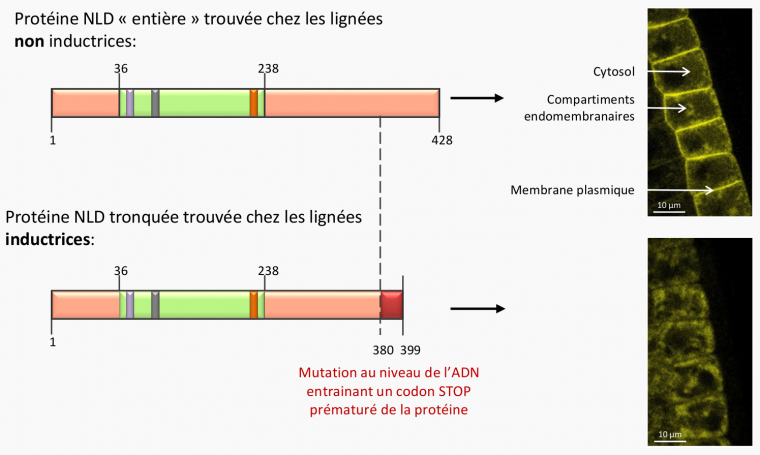
Ce gène NLD code une protéine qui est prédite pour avoir une activité de phospholipase (voir ci-dessous), et pour posséder une ancre lipidique lui permettant d’être liée à des membranes de la cellule. En fait, nous avons pu montrer que la protéine est effectivement associée à la membrane plasmique des deux gamètes mâles contenus dans le grain de pollen. Par ailleurs, la mutation identifiée chez toutes les lignées inductrices entraîne la formation d’une protéine tronquée sans ancre lipidique, qui perd sa localisation à la membrane plasmique dans notre système expérimental (Figure 3).
En expression hétérologue chez la plante Arabidopsis thaliana et fusionnée à la protéine fluorescente CITRINE (observations sur racines), on trouve la protéine NLD localisée à la membrane plasmique des cellules, dans le cytosol et dans des compartiments endomembranaires alors que la protéine NLD tronquée perd la localisation à la membrane plasmique.
Le rôle d’une phospholipase est le clivage d’un ou de plusieurs phospholipides, qui sont à la fois des composants structuraux de la membrane et des messagers secondaires mobiles. Nous tentons actuellement d’identifier le ou les phospholipide(s) précis coupé(s) par la protéine NLD, pour savoir si celle-ci joue plutôt un rôle dans la structure de la membrane, par exemple lors de la migration des gamètes mâles à l’intérieur du tube pollinique en croissance, ou plutôt un rôle de signal, par exemple dans le guidage du tube pollinique vers la cellule œuf ou lors de la fusion du gamète mâle avec la cellule œuf.
Notre découverte pourrait permettre d’exporter le système chez d’autres espèces pour les doter de lignées inductrices à leur tour. Notre hypothèse est qu’il suffit d’identifier le gène remplissant la fonction de NLD chez une autre espèce et de le muter de la même manière que chez le maïs pour obtenir une lignée inductrice.
Référence
Gilles, L.M. et al. (2017). Loss of pollen‐specific phospholipase NOT LIKE DAD triggers gynogenesis in maize. EMBO J. 36 : 707–717.