À la découverte de la diversité évolutive des histones.
Toutes les formes de vie cellulaire connues sur Terre stockent leur information génétique sous forme de longues molécules d’ADN qui sont fortement condensées, pouvant ainsi tenir à l’intérieur des cellules. Par exemple, l’ADN génomique d’une cellule humaine, de près de 2 mètres de long, est condensé et tient dans un noyau d’environ 6 micromètres de diamètre. Ce niveau impressionnant de condensation est en grande partie obtenu grâce à l’action de protéines histones. Chez tous les eucaryotes, l’ADN génomique s’enroule autour des histones en formant des structures appelées nucléosomes. Les nucléosomes interagissent entre eux et avec d’autres protéines pour former des niveaux supérieurs de condensation de la chromatine, ce qui permet ainsi une compaction dense de l’ADN dans le noyau.
L’arbre évolutif du vivant comprend trois grands domaines : les eucaryotes (organismes possédant un noyau délimité par une enveloppe nucléaire ; il s’agit d’un groupe qui comprend notamment les plantes, les animaux et les champignons), les archées (procaryotes unicellulaires qui se développent souvent dans des environnements extrêmes) et les bactéries (procaryotes unicellulaires omniprésents). De nombreuses innovations moléculaires sont partagées entre ces groupes. Cependant, les histones ont longtemps été considérées comme propres aux cellules eucaryotes. Des études récentes ont toutefois montré que ces dernières existent dans la plupart des archées et dans certaines bactéries, ce qui éclaire les mécanismes de condensation de l’ADN tout en soulevant de nouvelles questions sur l’évolution des histones.
Les histones chez les eucaryotes et les archées
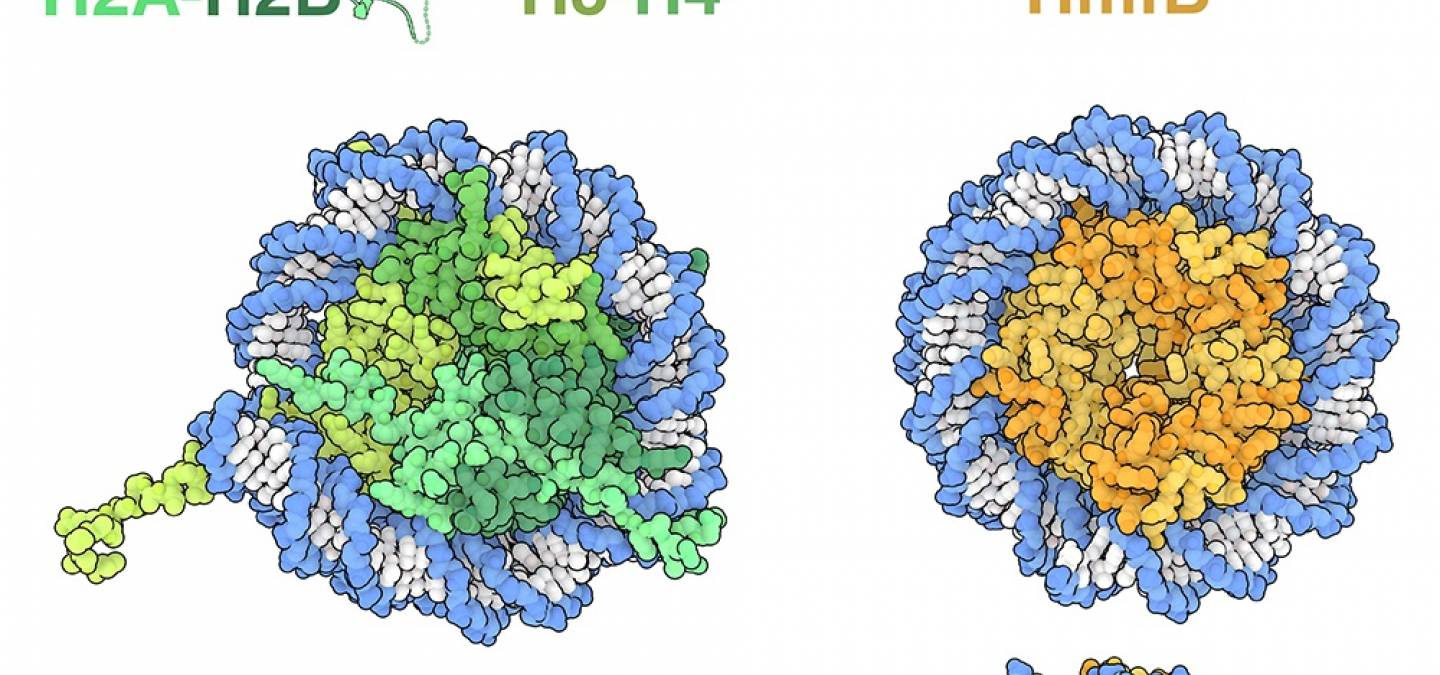
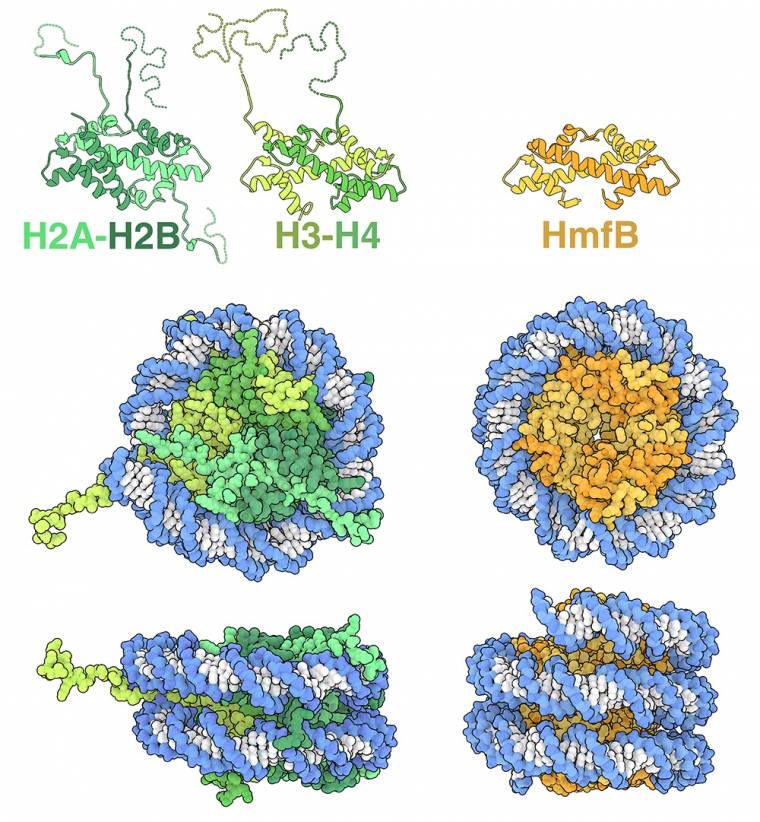
Chez les eucaryotes, il existe quatre histones centrales (H2A, H2B, H3 et H4) qui forment un octamère composé de deux hétérodimères H2A-H2B et deux hétérodimères H3-H4 1 (représentées en vert sur la figure 1, entrée de la base de données des protéines (PDB), 1aoi). Dans le nucléosome, les histones chargées positivement établissent de nombreuses liaisons indépendantes de la séquence des bases azotées puisqu’elles se forment avec le squelette phosphaté de l’ADN, chargé négativement. Toutes les histones eucaryotes présentent une structure très conservée et partagent un motif appelé « repliement de l’histone », composé de trois hélices alpha reliées par de courtes boucles de connexion.
Des études structurales ont montré que certaines lignées d’archées synthétisent des histones présentant une similitude structurelle remarquable avec les histones eucaryotes. Les histones de l’archée thermophile Methanothermus fervidus, appelées HMfA et HMfB, possèdent le repliement canonique des histones, se dimérisent et interagissent avec l’ADN d’une manière très similaire aux histones eucaryotes 2 (un dimère de HmfB est représenté en orange sur la figure 1, entrée PDB 5t5k). Toutefois, des différences significatives existent également. HMfA et HMfB partagent une grande similitude de séquence et forment facilement des homodimères ou des hétérodimères qui sont structurellement équivalents. Par conséquent, au lieu de construire des nucléosomes octamériques distincts, les dimères HMfA et HMfB peuvent s’oligomériser et former de longs assemblages superhélicoïdaux appelés hypernucléosomes. HMfA et HMfB ne possèdent pas non plus les longues queues présentes dans les histones eucaryotes. Bien que seul un nombre limité d’études structurales sur les histones archéennes aient été réalisées, les analyses génomiques suggèrent que la majorité des archées possède des protéines histones et que ces séquences présentent une plus grande diversité que celles trouvées chez les eucaryotes. Cette diversité suggère que de futures études révéleront de nouveaux assemblages histone-ADN et fourniront des informations supplémentaires sur l’évolution des histones eucaryotes 3.
Les histones eucaryotes (représentées en vert à gauche, entrée PDB 1aoi) forment des octamères à partir de paires de dimères d’histones. Les dimères H2A-H2B et H3-H4 sont représentés en haut, avec leurs queues complètes. À droite, HMfB (représentée en orange, entrée PDB 5t5k) est une histone d’archée qui forme des hypernucléosomes.
Les histones chez les bactéries
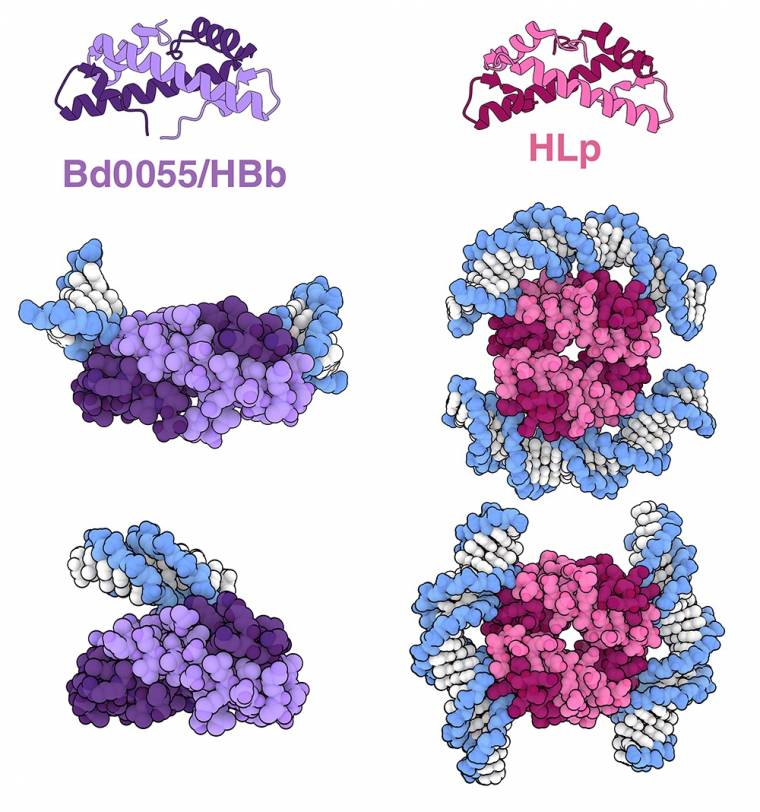
Étonnamment, les histones (généralement définies comme des protéines contenant un motif « repliement de l’histone » et se liant à l’ADN) ont également été récemment caractérisées chez les bactéries. En recherchant des protéines avec ce motif « repliement de l’histone » prédit dans une vaste base de données de génomes bactériens, les chercheurs ont identifié une protéine, appelée Bd0055 ou HBb, chez Bdellovibrio bacteriovorus, une bactérie omniprésente dans le sol et les milieux aquatiques. Des études structurales ont montré que la protéine Bd0055 forme des dimères qui peuvent se lier à l’ADN de deux manières distinctes (représentées en violet sur la figure 2). In vitro, la liaison à l’ADN se produit soit en périphérie sur ses extrémités 1 (entrées PDB 8fw7 et 9ezz), soit en position centrale 2 (entrée PDB 9f0e), avec une faible courbure de l’ADN observée dans les deux cas. On ne sait pas encore comment la protéine Bd0055 interagit et influence l’organisation de l’ADN dans un contexte cellulaire. Si des éudes biochimiques et des simulations suggèrent que les dimères de la protéine Bd0055 pourraient utiliser simultanément les deux surfaces de liaison et courber l’ADN, il a également été proposé que la protéine Bd0055 puisse former une enveloppe dense en protéines autour de l’ADN via son mode de liaison sur ses extrémités.
Des analyses bioinformatiques récentes ont permis d’identifier d’autres histones bactériennes, notamment l’histone HLp, une protéine contenant un repliement histone exprimée chez Leptospira perolatii, une bactérie à Gram négatif en forme de spirale. Des études structurales ont montré que HLp forme des tétramères qui peuvent se lier à l’ADN d’au moins deux manières distinctes 3 (représentées en rose sur la figure 2, entrées PDB 9qt1 et 9qt2). Des expériences complémentaires in vitro et in silico suggèrent que l’ADN pourrait s’enrouler autour des tétramères HLp d’une manière similaire aux nucléosomes eucaryotes.
Bien que la découverte des histones bactériennes soit surprenante, il semble que les histones soient rares chez les bactéries. On estime que seulement 2 % environ des génomes bactériens séquencés contiennent des protéines présentant un motif « repliement de l’histone » 4. La plupart des bactéries utilisent une variété de protéines associées au nucléoïde (NAP) permettant de condenser leur ADN génomique dans une petite région de la cellule, appelée le nucléoïde. Les bactéries qui expriment des histones expriment également des NAP, et la façon dont les histones bactériennes et les NAP peuvent agir ensemble et organiser l’ADN est actuellement inconnue.
Des assemblages d’histones bactériennes provenant de Bdellovibrio bacteriovorus (représentés en violet ; sur l’image du milieu, l’ADN est lié aux extrémités des histones, d’après les entrées PDB 8fw7 et 9ezz ; sur l’image du bas, la liaison est centrale, d’après l’entrée 9f0e) et de Leptospira perolatii (représentées en rose, entrées PDB 9qt1 et 9qt2).
Comparaison des histones des cellules eucaryotes, des archées et des bactéries
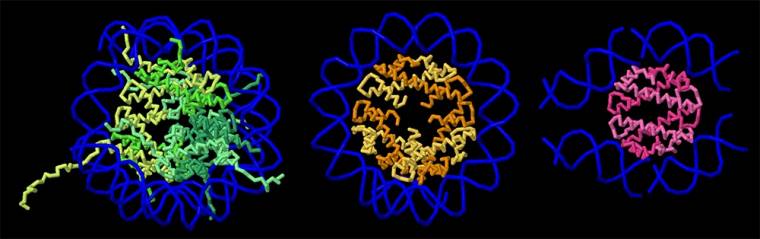
Vous pouvez examiner de plus près un nucléosome provenant du xénope lisse Xenopus laevis (entrée PDB 1aoi), un segment d’un hypernucléosome provenant de l’archée Methanothermus fervidus (entrée PDB 5t5k) et la protéine HLp liée à l’ADN provenant de la bactérie Leptospira perolatii (entrée PDB 9qt1) en vous rendant sur la page de l’article d’origine (en anglais), et en cliquant sur l’onglet JSmol de la section Exploring the structure.
Une comparaison des histones de l’organisme eucaryote Xenopus laevis (en vert, à gauche), de l’archée Methanothermus fervidus (en orange, au centre) et de la bactérie Leptospira perolatii (en rose, à droite).
Pour aller plus loin
- Vous pouvez en apprendre davantage sur les nucléosomes eucaryotes et sur l’ADN dans deux anciens articles de la molécule du mois.
- Le cisplatine est une petite molécule utilisée dans les traitements des cancers qui cause la mort des cellules en changeant la conformation de l’ADN.
Ce texte correspond à la traduction par Cédric Bordi de l’article Molecule of the Month : Histones Across the Tree of Life 1 écrit par Janet Iwasa en février 2026 sur le site PDB-101, le portail éducatif de la base de données sur les protéines (PDB).