Un médicament puissant à action prolongée qui cible la capside du VIH.
L’épidémie de sida, qui a débuté au début des années 1980, est causée par le virus de l’immunodéficience humaine (VIH), un rétrovirus qui attaque le système immunitaire. Bien qu’il n’existe actuellement aucun remède contre le VIH, un traitement antirétroviral pris de manière régulière peut supprimer la réplication virale, empêchant ainsi la progression de la maladie, ainsi que sa transmission, et permettant aux personnes séropositives de mener une vie longue et en bonne santé. Cependant, le respect d’un traitement médicamenteux quotidien strict et à vie peut représenter une contrainte pour de nombreuses personnes vivant avec le VIH, et tout manquement dans la prise régulière du traitement peut entraîner une prolifération virale et permettre la transmission du virus. Si le nombre de nouvelles infections par le VIH a considérablement diminué depuis son pic dans les années 1990, l’épidémie de sida persiste à l’échelle mondiale, avec environ 1,3 million de nouvelles infections par le VIH estimées en 2024.
La découverte d’un médicament qui cible la capside
Pendant des décennies, le développement de médicaments contre le VIH s’est concentré sur les enzymes virales comme la transcriptase inverse, la protéase et l’intégrase, ou sur les protéines structurales à la surface du virus, comme la protéine d’enveloppe. La protéine CA1, qui s’auto-assemble pour former une capside protéique conique autour du génome viral 2, n’était généralement pas considérée comme une cible d’intérêt pour des médicaments. Cependant, à partir de la fin des années 1990, un nombre croissant d’études scientifiques menées par des chercheurs spécialisés dans le VIH ont décrit la structure de la protéine CA ainsi que celle de la capside et ont montré que la réplication virale dépendait de l’intégrité de cette dernière 3. Ces découvertes ont convaincu une équipe des laboratoires Gilead Sciences de lancer un programme visant à découvrir et à développer un médicament ciblant la capside, dans le but de compléter les thérapies antirétrovirales existantes.
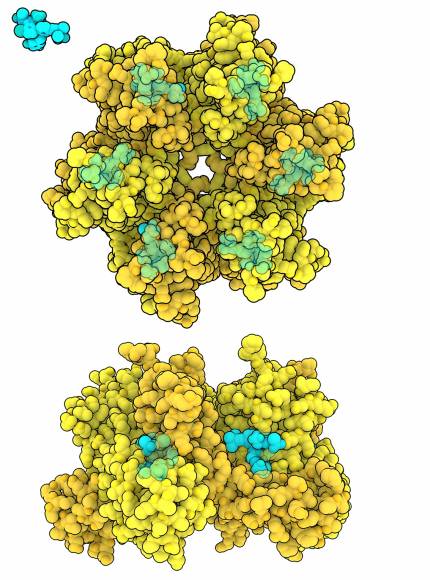
Le lénacapavir (représenté en cyan) se lie dans une poche entre les monomères de protéines CA d’un hexamère de capside du VIH (représentés en jaune, entrée PDB 6v2f).
Au cours des dix années suivantes, les scientifiques des laboratoires Gilead Sciences ont conçu, modifié et testé des milliers de composés se liant à la capside afin d’optimiser le potentiel thérapeutique, la stabilité et la biodisponibilité du médicament (certains de ces composés sont présentés dans la section Le développement du lénacapavir ci-après) 1. Le résultat final a été le lénacapavir, un médicament novateur par son mécanisme d’action, car ciblant la capside virale. Il a été approuvé pour le traitement du VIH multirésistant en 2022 et pour la prophylaxie pré-exposition (PrEP) en 2025 2. L’efficacité remarquablement grande et la longue demi-vie du lénacapavir dans l’organisme permettent une administration sous forme d’injection deux fois par an, ce qui améliore considérablement l’observance du traitement par rapport aux traitements antirétroviraux oraux quotidiens 3.
Comme le montre la figure 1, le lénacapavir se lie à l’interface entre deux sous-unités CA adjacentes (entrée de la base de données des protéines (PDB) 6v2f) 4. Des études ont montré que le lénacapavir est capable de perturber différentes étapes du cycle de vie du VIH, notamment en affectant l’importation du virus dans le noyau et l’intégration de l’ADN viral dans le génome de l’hôte, ainsi que l’assemblage et la maturation des virus nouvellement formés.
La fracturation de la capside
Des études structurales ont apporté de nouvelles informations sur le mécanisme d’action unique du lénacapavir. À l’aide de la cryotomographie électronique, les chercheurs ont découvert que le traitement des capsides intactes du VIH avec du lénacapavir entraîne leur rupture, celle-ci se produisant d’abord dans les zones de la capside présentant le plus haut niveau de courbure 1. Les parois des capsides traitées au lénacapavir se sont aplaties au début de l’expérience, puis se sont fragmentées. Ce processus est illustré dans l’animation visible en figure 2, créée par Rachel Torrez en collaboration avec Owen Pornillos (université de l’Utah). L’animation a été créée à partir des entrées PDB 9pry et 9y7j ainsi que de leurs modèles correspondants dans la banque de données de microscopie électronique (EM), EMD-71816 et EMD-72657.
Une étude plus approfondie des hexamères voisins dans les capsides ciblées a révélé que la liaison du lénacapavir induit une petite rotation entre deux hexamères, ce qui les déstabilise. Ces changements se produisent à des endroits distants du site initial de liaison du lénacapavir, ce qui démontre que le médicament agit de manière allostérique 1. Les chercheurs supposent que la liaison du lénacapavir induit une contrainte mécanique sur le réseau cristallin de la capside et que, à mesure que davantage de molécules de lénacapavir se lient, la contrainte s’accumule jusqu’à ce que la capside se rompe, perturbant ainsi la réplication virale. La rupture prématurée de la capside conduit probablement à l’activation de la réponse immunitaire innée et à l’élimination du virus.
Le développement du lénacapavir
Les scientifiques du laboratoire Gilead Sciences ont testé de nombreux composés avant de découvrir le lénacapavir. Vous pouvez examiner de plus près quelques-uns des composés qui ont été synthétisés, dont les structures ont été caractérisées et qui ont contribué à optimiser la structure chimique du lénacapavir en vous rendant sur la page de l’article d’origine (en anglais), et en cliquant sur l’onglet JSmol de la section Exploring the structure. Ce dernier permet d’observer le composé 6 (entrée PDB 9pgs), le composé 12 (entrée PDB 9pgt), le composé 24 (entrée PDB 9pgv), le composé 40 (entrée PDB 9pgu) et le lénacapavir (entrée PDB 6v2f).
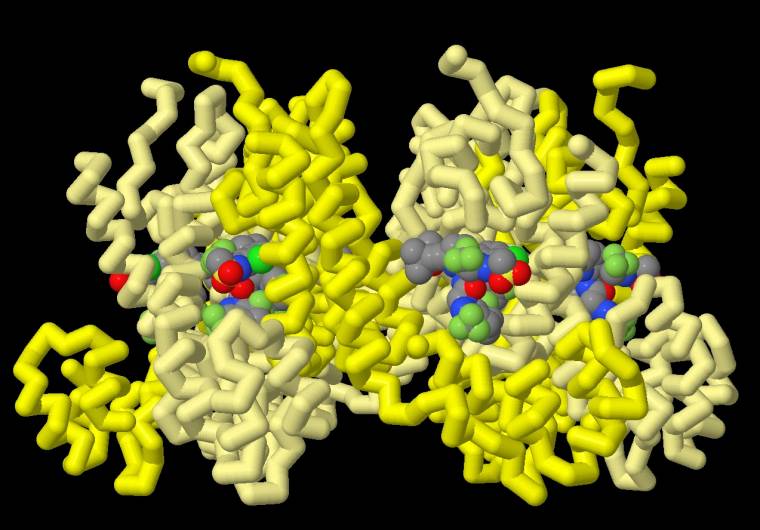
Fixation du lénacapavir (dont les atomes sont représentés sous forme de sphères colorées) sur les protéines CA de la capside du VIH (dont les hélices α sont représentées bâtonnets jaune et beige clair).
Pour aller plus loin
- Vous pouvez explorer d’autres contenus liés au VIH et au sida sur le site PDB-101.
- Vous pouvez examiner de plus près la structure de la capside du VIH dans un ancien article de la molécule du mois et construire un modèle en papier de celle-ci.
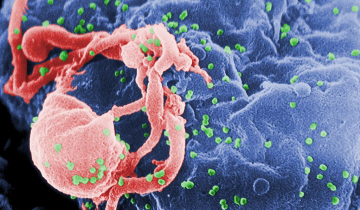
- Découvrez une illustration d’une cellule infectée par le VIH par David Goodsell.
- Découvrez le mode d’action des différentes classes d’antiviraux à travers une animation disponible sur le site PDB-101.

Ce texte correspond à la traduction par Cédric Bordi de l’article Molecule of the Month : Lenacapavir 1 écrit par Janet Iwasa en mars 2026 sur le site PDB-101, le portail éducatif de la base de données sur les protéines (PDB). La note de bas de page est un ajout du traducteur.