Le sida est le stade le plus avancé de la maladie causée par le VIH. Ce virus affaiblit lentement le système immunitaire en parasitant et détruisant l’ensemble des lymphocytes T CD4+ de l’organisme. Sans traitement, les personnes infectées se retrouvent peu à peu sans défenses immunitaires et sont alors plus susceptibles de contracter des maladies dites opportunistes, aboutissant à la mort de l’individu. Si la trithérapie permet aujourd’hui de vivre avec le VIH, la recherche se poursuit dans l’espoir de mettre un jour un terme à cette épidémie.
L’épidémie de sida dans le monde
Bref historique du sida
En 1981, aux États-Unis, une quarantaine de cas d’individus atteints de maladies rares, toutes associées à un système immunitaire affaibli, sont décrits. Syndrome initialement assigné à la population homosexuelle (nommé « peste gay » ou « syndrome gay »), son universalité est ensuite reconnue : en 1982 naît alors le terme sida (syndrome de l’immunodéficience acquise) pour caractériser cette maladie 1.
Le virus à l’origine de ce syndrome est isolé un an plus tard à l’Institut Pasteur (Paris) par Françoise Barré-Sinoussi et Luc Montagnier 2, dont les travaux seront récompensés d’un prix Nobel en 2008. Ce nouveau rétrovirus humain est baptisé virus de l’immunodéficience humaine (VIH) en 1986 3. Cette même année, un autre rétrovirus humain est isolé en Afrique de l’Ouest, similaire au VIH bien que moins virulent. Ce nouveau virus est nommé VIH-2, tandis que le premier, que l’on retrouve sur l’ensemble du globe est nommé VIH-1.
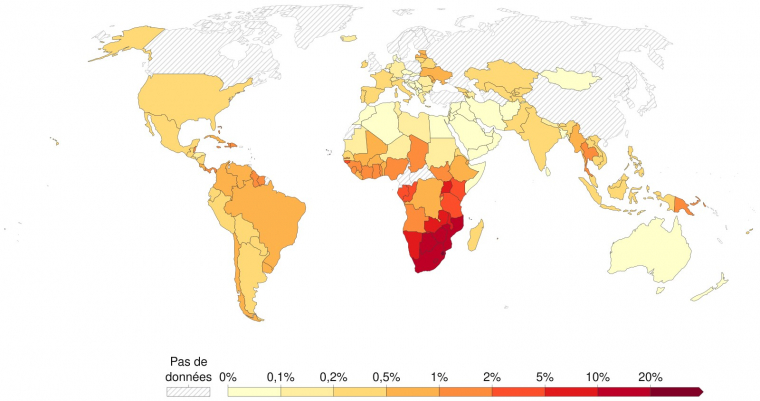
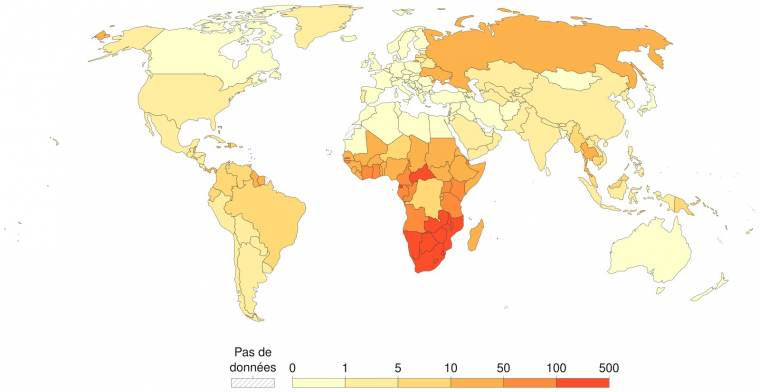
Aujourd’hui, plus de 40 ans après sa découverte, le VIH reste un problème majeur de santé publique, et ce à l’échelle mondiale (Figures 1 et 2). Depuis son apparition, on estime que le sida a causé 44,1 millions de décès 4. En 2024, on compte près de 41 millions de personnes vivant avec le VIH dans le monde, dont 5,3 millions de personnes l’ignorant et 1,3 million de nouveaux cas. Cette même année, 630 000 personnes sont décédées d’une maladie opportuniste liée au sida 5.
La prévalence du VIH (pourcentage de personnes infectées par le VIH) est la plus importante en Afrique subsaharienne, avec un gradient décroissant du sud vers le nord. Dans le reste du monde, la prévalence est généralement inférieure à 1 %.
L'échelle de couleur indique le nombre de morts dues au sida pour 100 000 habitants en 2021. Le sida (syndrome de l’immunodéficience acquise) correspond au dernier stade de l'infection par le VIH. Il est défini par la survenue d'au moins un des vingt cancers ou maladies opportunistes qui peuvent se produire dans le contexte d'un système immunitaire affaibli.
Origine du virus
Il a été démontré que le VIH est issu du virus de l’immunodéficience simienne (VIS), présent naturellement chez certains primates non humains (45 espèces de singes africains sont infectés par le VIS). En effet, les similitudes dans la séquence et l’organisation du génome viral, la prévalence chez l’hôte naturel, la coïncidence géographique et les voies de transmission plausibles laissent peu de doute quant à l’origine zoonotique de ce virus.
Ainsi, au début du XXe siècle, en Afrique de l’Ouest et en Afrique centrale, plusieurs événements indépendants de transmission du VIS du singe à l’être humain ont généré les différentes lignées de VIH-1 et VIH-2 1. Les dernières analyses génétiques indiquent que le VIH-1 est apparu suite à la transmission du VIS des chimpanzés et des gorilles à l’humain, tandis que le VIH-2 est issu des mangabeys fuligineux 2.
En ce qui concerne les modes de transmission, l’hypothèse la plus répandue suggère une transmission du SIV à l’humain par une exposition de la peau ou des muqueuses au sang et aux autres fluides biologiques d’animaux infectés (blessures lors de la chasse et du dépeçage de ces primates, consommation de cette viande crue, détention de ces singes comme animaux de compagnie…) 3.
Contaminations et risques
Le VIH est un virus très fragile, rapidement détruit à l’air libre. Il nécessite pour se propager une transmission directe par contact prolongé entre un liquide corporel riche en particules virales et une lésion. Les sécrétions sexuelles (sperme, liquide pré-séminal, sécrétions vaginales), le sang et le lait maternel sont ainsi susceptibles de transmettre le virus du sida. À cela s’ajoutent des liquides tels que le liquide céphalo-rachidien et le liquide amniotique qui, théoriquement, pourraient également constituer un risque pour les professionnels de santé y étant exposés. Aucun cas de transmission par ces fluides n’a cependant été rapporté à ce jour.
Le VIH est donc classiquement transmissible d’une personne à une autre par trois voies : la voie sexuelle, la voie sanguine, et la voie mère-enfant (Tableau 1). En revanche, le VIH ne se transmet pas par la salive, la sueur, les larmes, les gouttelettes produites par la toux, l’urine, les excréments ou encore via les piqûres d’insecte (le VIH ne survit pas dans les glandes salivaires des moustiques). Naturellement, le VIH n’est pas transmis par des contacts n’impliquant pas d’échanges de fluides corporels (accolades, poignées de main…) 4.
Aujourd’hui, 95 % des contaminations se font par voie sexuelle, les risques de transmission augmentant avec la durée du rapport, en cas d’inflammation ou lésions des muqueuses, en présence d’une autre infection sexuellement transmissible, et d’autant plus pendant les phases précoces et avancées de l’infection au VIH (lorsque la charge virale est particulièrement élevée). À l’inverse, la circoncision masculine diminue (mais n’élimine pas) le risque de contracter le VIH chez l’homme (dans le cas d’un rapport pénétrant), le prépuce favorisant un contact prolongé avec le virus 5.
| Voie d’exposition | Risque par type d’exposition | Remarques | |
|---|---|---|---|
| Voie parentérale | Transfusion | 92,5 % | Si de nombreuses contaminations ont eu lieu par transfusion dans les années 1980, lors de l’affaire du sang contaminé, ce risque est désormais pratiquement nul, de par la sélection des donneurs et la recherche du virus et d’anticorps anti-VIH dans les dons du sang. |
| Partage d’aiguille contaminée | 63 % | ||
| Piqûre percutanée | 23 % | ||
| Voie mère-enfant | Grossesse | 23 % | In utero, le risque de transmission du VIH est faible mais possible par la voie transplacentaire, essentiellement lors du 3e trimestre. |
| Accouchement | 65 % | Lors de l’accouchement, les contacts avec le sang et les sécrétions vaginales de la mère favorisent la contamination. Une césarienne réduit ainsi les risques de transmission au nouveau-né. | |
| Allaitement | 12 % | Pendant l’allaitement, une contamination via les muqueuses fragiles du bébé dans le tube digestif est possible. | |
| Voie sexuelle | Rapport anal réceptif | 1,38 % | Les pratiques sexuelles présentant un risque sont celles impliquant des traumatismes muqueux. En effet, les microlésions et inflammations dans les muqueuses (génitales, rectales ou buccales) sont des portes d’entrées pour le virus en cas de contact avec les sécrétions sexuelles contaminées. |
| Rapport anal pénétrant | 0,11 % | ||
| Rapport vaginal réceptif | 0,8 % | ||
| Rapport vaginal pénétrant | 0,4 % | ||
| Rapport oral réceptif | < 0,4 % | ||
Les estimations données dans le tableau 1 concernent des situations sans prise de traitements ni utilisation de préservatifs 678. Avec un traitement, les risques de transmission sont extrêmement faibles (voir plus bas). Pour la voie mère-enfant, peu d’études proposent une quantification des risques pour les trois modes de transmission (grossesse, accouchement, allaitement). Les probabilités données ici sont celles que la contamination avérée d’un nouveau-né ait eu lieu in utero, en péri-partum ou en post-partum.
Si les valeurs présentées concernant les risques de transmission par voie sexuelle peuvent a priori paraître peu élevées, il convient de souligner que ces valeurs sont des moyennes et qu’elles donc sont modulées par de nombreux facteurs individuels : système immunitaire plus ou moins efficace, inflammation en cours, présence de lésions, charge virale de l’individu séropositif… Un unique rapport non protégé peut suffire pour transmettre le VIH et le risque est multiplié par le nombre de rapports non protégés. La situation épidémique actuelle atteste d’ailleurs de ce risque important, avec près de 1,5 million de nouveaux cas chaque année dans le monde, dont la quasi-totalité résulte de rapports sexuels non protégés. La prévention reste donc primordiale pour éviter toute contamination.
Structure du VIH et cycle viral
L’épidémie mondiale du sida étant causée par le VIH-1, la suite de cet article sera consacrée aux caractéristiques et à l’étude du VIH-1. Le VIH-2 possède la même structure générale que le VIH-1, mais présente des différences génomiques aboutissant à quelques protéines différentes. Si la virulence est moindre, la physiopathologie causée par l’infection au VIH-2 est semblable à celle du VIH-1.
Structure du VIH-1
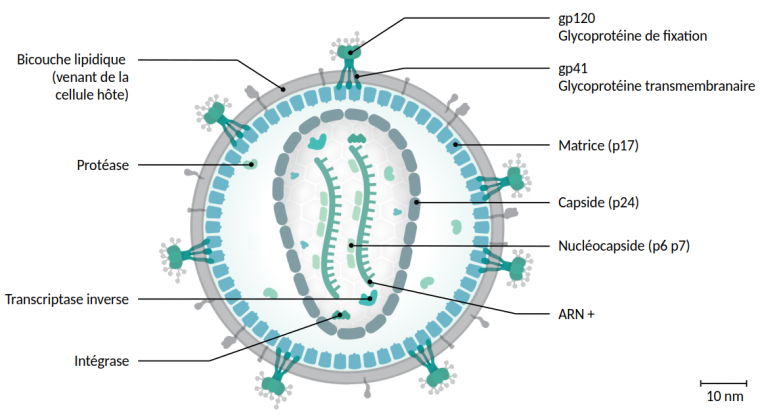
Le VIH-1 est une particule virale sphérique d’environ 120 nanomètres de diamètre, composée de trois éléments structuraux principaux : le génome (ARN), la capside (protéine p24) et l’enveloppe (bicouche lipidique comprenant les glycoprotéines gp120 et gp41) (Figure 3). Ce virus appartient à la famille des rétrovirus (Retroviridae), caractérisée par la présence d’une enzyme particulière : la transcriptase inverse.
La particule virale, d'un diamètre d'environ 120 nm, est composée de protéines structurelles : les protéines gp120 et gp41 de l’enveloppe, la protéine de matrice (p17), la protéine de capside (p24) et les protéines de la nucléocapside (p6 et p7) ainsi que de protéines essentielles au cycle de réplication : transcriptase inverse, intégrase et protéase.
Modèles 3D interactifs de virions de VIH
Le site Mesoscale explorer permet de partir à la découverte de différentes structures biologiques : protéines, virion de SARS-CoV-2, synapse… Parmi ces modèles, deux « visites guidées » du virion du VIH sont proposées. Le premier modèle se limite aux principales protéines et sera donc adapté pour des élèves de lycée. Le second modèle, plus détaillé, intéressera les étudiants, étudiantes et leurs professeurs.
Organisation génomique
Le génome viral est constitué de deux copies d’ARN simple brin, à polarité positive1, d’environ 10 kb chacune. Il comporte trois gènes principaux : gag (group specific antigens), pol (polymerase) et env (enveloppe) ; ainsi que quelques gènes accessoires et de régulation, encadrés des séquences non transcrites 5’LTR et 3’LTR (Figure 4) 2. L’épissage alternatif et trois cadres de lecture chevauchants permettent d’obtenir de nombreuses protéines à l’issue de la traduction. Les gènes accessoires et de régulation assurent la production de six protéines (vif, vpr, vpu, nef, tat et rev) contribuant notamment au pouvoir pathogène du virus.
Le génome du VIH étant formé d’ARN à polarité positive, il peut être directement traduit en protéines par les ribosomes de la cellule infectée. Les ARN peuvent également provenir de la transcription du génome viral, après son intégration dans le génome de l’hôte. Trois cadres de lecture peuvent être suivis par les ribosomes, ce qui mène à la synthèse des différentes protéines virales. Le 5’LTR est suivi des gènes gag (codant les protéines de structure : matrice p17, capside p24, nucléocapside p7/p6), pol (codant les protéines virales enzymatiques : protéase p10, transcriptase inverse domaine p51/domaine RNase p15, intégrase p31) et env (codant les protéines de l’enveloppe gp120 et gp41), ce dernier étant entouré des gènes accessoires et de régulation. Les gènes de régulation tat et rev sont chacun constitués de deux exons répartis sur deux cadres de lectures différents. Pour tat, après épissage, les exons restent sur deux cadres de lecture différents. Lors de la traduction, les ribosomes changent de cadre de lecture à la jonction entre l’exon 1 et l’exon 2 (frameshifting). Pour rev, le processus d’épissage permet de relier les exons sur un même cadre de lecture.
Cycle viral
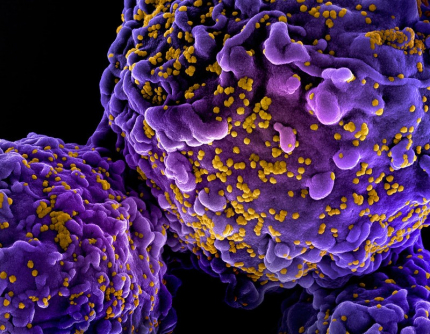
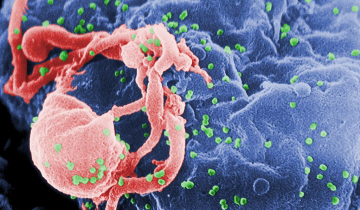
Les particules virales (jaune), d’un diamètre d’environ 100 nm, sont 100 fois plus petites que les lymphocytes (violet) qu’elles infectent. Image colorisée obtenue par microscopie électronique à balayage.
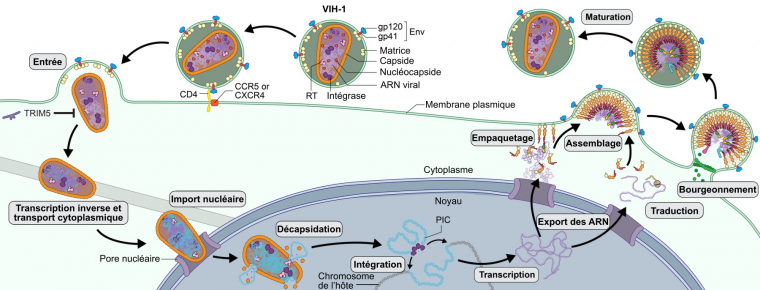
Le VIH infecte une cellule cible par fixation de la glycoprotéine virale gp120 à une protéine spécifique : le récepteur CD4 (associé à un co-récepteur : CCR5 ou CXCR4). Le VIH parasite ainsi les cellules immunitaires portant la protéine de surface CD4, soit les lymphocytes T auxiliaires ou CD4+ (nécessaires à l’activation et la multiplication des lymphocytes B et T), mais également certaines cellules présentatrices d’antigènes (macrophages, cellules dendritiques et cellules microgliales). Après entrée dans la cellule immunitaire, l’ARN viral est rétrotranscrit en ADN par une transcriptase inverse peu fidèle, processus clé responsable du taux de mutation élevé du VIH. Ce génome viral est ensuite intégré dans le génome cellulaire, et s’exprime grâce à la machinerie de transcription et traduction de la cellule-hôte, à l’origine de millions de copies (Figures 5, 6 et 7).
Le cycle viral du VIH-1 est composé de plusieurs étapes :
– fixation du virion à la cellule-hôte par interaction des protéines virales gp120 et gp41 avec le récepteur CD4 et le co-récepteur CCR5 ou CXCR4 de l’hôte ;
– entrée de la capside virale dans la cellule immunitaire par fusion de la membrane du virion et de la membrane plasmique de la cellule grâce au changement de conformation de gp41 (mécanisme majoritaire) ou entrée par endocytose puis fusion avec la membrane de l’endosome (mécanisme minoritaire, non représenté sur ce schéma) ;
– rétrotranscription de l’ARN viral en ADN viral par la transcriptase inverse ;
– décapsidation dans ou au contact du noyau ;
– intégration de l’ADN viral au génome de la cellule-hôte par l’intégrase ;
– production de nombreux ARN viraux ;
– traduction de l’ensemble des protéines virales ;
– assemblage et libération par bourgeonnement de très nombreuses particules virales (héritant de la membrane de la cellule–hôte) provoquant peu à peu la destruction du lymphocyte T CD4+ ;
– maturation des virions et passage dans le sang.
Documents à télécharger
Une fois intégré dans la cellule hôte, le génome viral s’exprime jusqu’à la mort de la cellule. Celle-ci peut être causée par le virus, par l'apoptose déclenchée par des signaux intracellulaires ou suite à l'action de lymphocytes cytotoxiques : lymphocytes T CD8 et cellules tueuses naturelles NK. Dans certaines conditions, en particulier dans des lymphocytes T CD4 mémoires quiescents, le génome viral est intégré mais ne s’exprime pas 1. Certains signaux d’activation lymphocytaire peuvent provoquer la sortie de la latence virale et la propagation du virus dans l’organisme. Ces cellules immunitaires constituent ainsi des réservoirs du VIH et représentent un obstacle majeur à l’éradication du virus chez les individus infectés, puisqu’il faudrait une destruction de toutes ces cellules hôtes (par ailleurs essentielles à l’immunité) pour définitivement éliminer le virus de l’organisme.
Conséquences physiopathologiques de l’infection
Diagnostic
Le diagnostic de l’infection par le VIH repose généralement sur la détection d’anticorps anti-VIH et de l’antigène p24 (capside) dans le sang. Ces deux types de protéines sont détectées, en laboratoire d’analyses médicales, grâce à un test Elisa suivi d’un Western blot en cas de positivité. Ces tests sont fiables 3 à 6 semaines après la situation à risque, le temps que les anticorps anti-VIH soient produits ou que la protéine p24 devienne détectable. En cas de suspicion d’infection très récente, les tests de détection des ARN viraux par PCR (soumis à prescription médicale) permettent de déterminer la présence du VIH plus rapidement, dès la fin de la phase éclipse de l’infection (7 à 10 jours après l’exposition). Il est également possible, après un délai minimal de 12 semaines, de se dépister par test rapide d’orientation diagnostique (TROD) ou par autotest. Ces deux méthodes ont l’avantage de donner des résultats immédiats. En cas de résultat positif, une confirmation par prise de sang est nécessaire, auquel cas l’individu est dit séropositif (positif aux anticorps anti-VIH dans son sérum). Toutefois, il est désormais d’usage de ne plus parler de « patients » ou « d’individus séropositifs » mais de préférer les termes de personnes « avec VIH » ou « vivant avec le VIH » afin de lutter contre la stigmatisation associée à l’infection, d’autant plus que les individus commençant un traitement antirétroviral très précocement peuvent ne pas devenir séropositifs (malgré la présence du VIH dans leur organisme), rendant ce terme inadéquat.
Plus d’informations sur les méthodes et les lieux de dépistage en France sont disponibles sur le site de l’Assurance maladie, Ameli.
Manifestations cliniques et stades d’infection
En l’absence de traitement, l’évolution de l’infection par le VIH se déroule en trois étapes chez l’adulte (Figure 8) :
-
Dans les semaines suivant l’infection, la phase de primo-infection (4 à 8 semaines) est caractérisée par une prolifération rapide du virus et une diminution importante des lymphocytes T CD4+ dans le sang. Le système immunitaire produit ensuite des anticorps anti-VIH neutralisant les particules virales et des lymphocytes T CD8+ tuant les cellules infectées. Cette première phase, avec peu ou pas de symptômes apparents (symptômes pseudo-grippaux), est la période pendant laquelle le virus est le plus susceptible d’être transmis par l’individu porteur du virus.
-
Ensuite, l’infection devient chronique et asymptomatique, résultat d’un équilibre entre réplication virale et défense de l’organisme. Cette phase dure en moyenne de 7 à 10 ans (mais parfois moins d’un an). Le patient ne présente pas de symptômes, malgré une réplication active et constante (environ 109 nouvelles particules virales sont produites chaque jour), le nombre de virus reste faible (mais suffisant pour la transmission) en raison d’une réponse immunitaire qui parvient à contrôler partiellement l’infection. Cependant, en l’absence de traitement, le virus échappe peu à peu à la pression immunitaire, la quantité de lymphocytes T CD4+ diminue progressivement durant toutes ces années, jusqu’à ce que les premiers symptômes apparaissent (perte de poids, infections de la peau, fièvre, diarrhée…).
-
Passé le seuil de 200 lymphocytes T CD4+/mm3 de sang, le patient entre en phase sida. La virémie augmente drastiquement du fait d’un système immunitaire défaillant : les lymphocytes T CD4+ trop peu nombreux ne jouent plus leur rôle d’activateur des lymphocytes B et T CD8+. Cela entraîne une chute de la quantité d’anticorps (reconnaissant les agents pathogènes) et de lymphocytes T cytotoxiques (lysant les cellules infectées). Il n’y a plus de réponse immunitaire spécifique, le patient développe alors de multiples maladies opportunistes (tuberculose, zonas, lymphomes, pneumocystoses, mycoses, cancers…) conduisant au décès.
Chez les bébés, l’immaturité du système immunitaire explique que, sans traitement, la moitié d’entre eux n’atteignent pas l’âge de deux ans.
Prévention et prise en charge thérapeutique
Antirétroviraux et trithérapie
Les antirétroviraux ont pour objectif de réduire la charge virale et de restaurer l’immunité chez les individus infectés. Ces médicaments agissent en bloquant la multiplication du virus à différentes étapes du cycle de réplication de ce dernier :
- les inhibiteurs d’entrée empêchent la pénétration du virus dans la cellule (inhibiteurs de CCR5, inhibiteurs de fusion) ;
- les inhibiteurs de la transcriptase inverse et de l’intégrase bloquent les mécanismes d’expression génétique ;
- les inhibiteurs de la capside, nouvelle classe d’antirétroviraux puissants à longue durée d’action, ciblent la capside virale et bloquent plusieurs étapes du cycle (transport de la capside au noyau, assemblage et relargage des nouvelles particules virales) ;
- les inhibiteurs de la protéase bloquent la maturation des précurseurs des protéines constitutives de la particule virale (pas d’assemblage de nouveaux virus).
L’utilisation d’un unique antirétroviral aboutissant à des échecs, les premières combinaisons d’antirétroviraux entièrement suppressifs sont apparues dans les années 1990, montrant une synergie d’action avec l’utilisation de trois antirétroviraux. En plus de maximiser l’efficacité du traitement, cette association permet de limiter drastiquement les résistances virales induites par un unique médicament (phénomène fréquent du fait du haut taux de mutation du VIH) : c’est le début de la trithérapie 1. Grâce à ce traitement la charge virale chez les personnes vivant avec le VIH devient indétectable (< 50 copies/mL).
Aujourd’hui, un seul comprimé quotidien (contenant trois molécules) permet d’obtenir une charge virale indétectable de façon durable chez la quasi-totalité de ces personnes 2. Le traitement antirétroviral n’est cependant pas curatif, il bloque l’infection de nouvelles cellules, mais n’éradique par les populations cellulaires dites « réservoirs », ayant déjà intégré l’ADN viral dans leur génome. Le traitement doit donc être pris à vie afin d’empêcher en permanence la réplication du virus et l’augmentation de la charge virale. En cas d’arrêt de traitement, la réplication reprend et le virus est détectable en quelques jours à quelques semaines.
La recherche sur les antirétroviraux continue et permet d’améliorer le quotidien des individus vivant avec le VIH. Depuis 2021, les patients présentant une charge virale indétectable depuis plus de 6 mois peuvent remplacer la prise quotidienne de leur médicament par une injection intramusculaire à renouveler tous les 2 mois 3. Des recherches sont toujours en cours afin d’étendre ce mode d’administration à l’ensemble des personnes séropositives 4, et de proposer des médicaments à plus longue durée d’action (une injection tous les 6 mois) 5.
Grâce à ces avancées, l’infection à VIH est devenue une pathologie chronique permettant de vivre longtemps et en bonne santé avec une prise en charge adaptée. Des limites demeurent cependant dans l’accès à ces thérapies dans certaines régions du monde puisque seulement 77 % des personnes infectées ont accès à ces traitements. Ainsi, en 2024, ce sont encore 630 000 personnes, soit 1,5 % des personnes vivant avec le VIH, qui sont décédées du sida 6, et la situation risque de se dégrader dramatiquement dans les mois et années à venir, du fait des récentes décisions politiques américaines suspendant les programmes d’aide internationale (lesquels représentaient 40 % des financements mondiaux en 2024). Faute de moyens, de nombreuses structures de soins ferment, compromettant gravement les programmes de prévention, de dépistage et de prise en charge du VIH, notamment en Afrique. L’arrêt de l’approvisionnement en antirétroviraux menace ainsi 20 millions de personnes actuellement sous traitement, mais également les populations à risque bénéficiant de traitements prophylactiques 7.
Prévention
Aujourd’hui, la méthode la plus simple et accessible à tous pour prévenir la transmission par voie sexuelle du VIH et d’autres infections sexuellement transmissibles consiste en l’utilisation correcte de préservatifs masculins ou féminins.
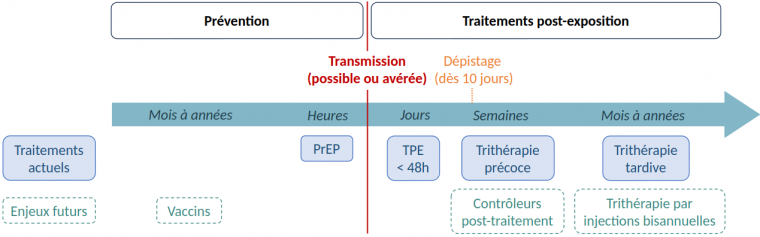
L’utilisation d’antirétroviraux permet également de prévenir la transmission du VIH (Figure 11). Les individus souhaitant se protéger du VIH peuvent avoir recours à 8 :
-
La prophylaxie pré-exposition (PreP), consistant en la prise d’antirétroviraux en amont d’une situation à risque. Cette méthode s’adresse aux personnes à haut risque de contracter le VIH de par leurs pratiques (relations sexuelles non protégées, échanges de matériel d’injection de drogues).
-
La prophylaxie post-exposition (PPE), également appelée traitement post-exposition (TPE). Après une situation à risque, cela permet de réduire le risque d'infection par VIH grâce à la prise d’antirétroviraux durant 30 jours, dès les 4 heures suivant l’exposition (au plus tard dans les 48 h).
Pour les individus porteurs du VIH, la prise continue d’un traitement antirétroviral, en plus d’empêcher la réplication du VIH dans leur organisme, permet aussi de prévenir la transmission du virus, et constitue le TAsP (Treatment as Prevention). Une personne sous traitement qui a une charge virale indétectable depuis 6 mois ne transmet plus le virus (indétectable = intransmissible) : elle peut avoir des rapports non protégés et entreprendre une grossesse sans risque de transmission du VIH 910. Cela souligne l’importance du dépistage dans la gestion de cette épidémie : aujourd’hui, dans les pays ayant accès aux traitements, ce sont majoritairement les individus séropositifs ignorant leur statut (et donc sans traitement) qui transmettent le virus et participent à la dynamique actuelle du VIH. Le dépistage, en permettant un diagnostic précoce, constitue ainsi un levier essentiel dans le contrôle de l’épidémie.
Enfin, dans le cas de l’usage de drogues injectables, l’emploi de matériel stérile non réutilisable permet d’éviter les risques de contamination.
Traitements du futur et enjeux de la recherche
Si les antirétroviraux ont considérablement changé la qualité de vie des personnes vivant avec le VIH, ils présentent tout de même des effets secondaires à long terme et ne permettent pas de guérir de l’infection. Par ailleurs insuffisants pour mettre un terme à l’épidémie, il est nécessaire de poursuivre la recherche dans la mise au point de nouvelles stratégies.
Cas rares de résistance : des patients inspirants
De rares cas de résistance à l’infection par le VIH ont été documentés ces dernières décennies, représentant de précieuses pistes de traitements pour les chercheurs.
Ainsi, certains individus (1 % de la population caucasienne) sont porteurs de la mutation CCR5-∆32 à l’état homozygote, leur conférant une protection naturelle face aux souches majoritaires du VIH, qui utilisent le co-récepteur CCR5. Chez ces individus, ce co-récepteur n’est pas exprimé à la surface des cellules. Les virions ne peuvent donc pas se fixer aux lymphocytes T CD4 et les infecter 11. Par ailleurs, si l’hétérozygotie CCR5-∆32 n’empêche pas l’infection, celle-ci progresse tout de même moins rapidement 12. La mutation CCR5-∆32 ne confère pas de résistance aux souches du VIH utilisant le co-récepteur CXCR4, mais ces virus sont plus rarement transmissibles.
D’autres individus sont également résistants à l’infection malgré une exposition répétée au virus. Cette population résistante comprend notamment des travailleuses du sexe au Kenya, chez qui des chercheurs ont constaté la présence, dans le sang et au niveau des muqueuses génitales, de lymphocytes T cytotoxiques reconnaissant les cellules infectées par le VIH. Ces lymphocytes sont de plus surreprésentés au niveau du col de l’utérus (site d’exposition virale) par rapport aux femmes infectées par le VIH 13. Ils seraient responsables d’une réponse cytotoxique rapide et plus efficace que la normale, qui permettrait l’élimination du virus avant sa propagation dans l’organisme. Il semblerait par ailleurs qu’une exposition constante ou fréquente au VIH soit nécessaire pour maintenir cette réponse cytotoxique protectrice 14.
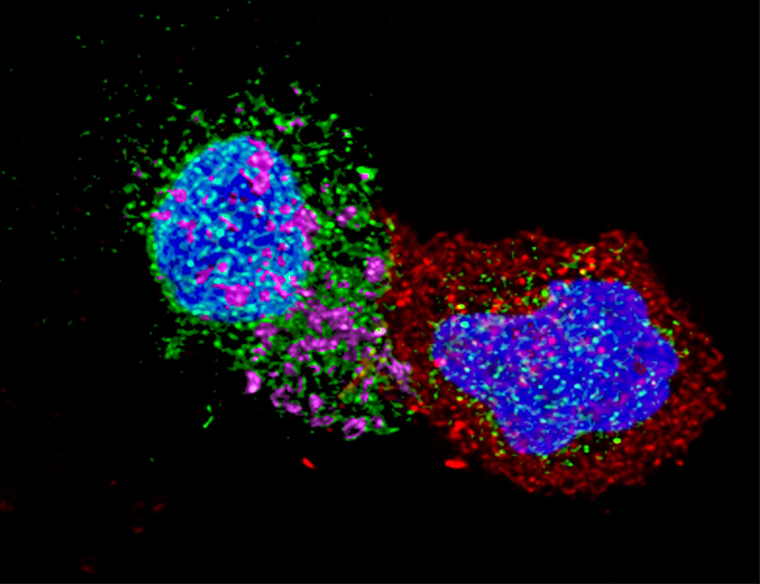
D’autre part, certains individus (<0,5 % des personnes vivant avec le VIH) n’y sont pas résistants mais maintiennent naturellement une charge virale très faible dans leur organisme, et ne présentent donc pas de progression vers la maladie : ce sont des contrôleurs naturels. Ce contrôle spontané est dans certains cas associé à un fond génétique particulier, à l’origine de fortes réactions immunitaires dirigées contre le VIH 15. Leur capacité à maintenir une faible charge virale aurait plusieurs origines. Certaines de ces personnes présentent par exemple des mutations diminuant l’expression de CCR5 en surface des lymphocytes T CD4 (limitant l’infection par le virus), ou bien une fine sensibilité des lymphocytes T CD4 au VIH, provoquant une réponse antivirale accrue 16. Parallèlement, les lymphocytes T CD8 de ces individus ont une activité cytotoxique très efficace, permettant de détecter et d’éliminer rapidement les cellules infectées par le VIH (Figure 9).
Image, obtenue par microscopie confocale, de cellules d'un contrôleur naturel (personne infectée par le VIH, mais dont la charge virale est naturellement très faible). Un lymphocyte CD8, en rouge, est au contact d'une cellule CD4 infectée par le VIH (protéine gp120 du virus marquée en vert). Les noyaux des cellules sont en bleu. En rose, la molécule cytotoxique granzyme B libérée par le lymphocyte T CD8.
Enfin, sur le même principe, certains individus porteurs du VIH-1 ayant bénéficié d’un traitement antirétroviral précoce et durant plusieurs années, ont la capacité de contrôler le virus après l’arrêt du traitement 1. On parle de contrôleurs post-traitement. Les études suggèrent que les lymphocytes T CD8 de certains de ces patients ont acquis, grâce au traitement précoce, les caractéristiques mémoires et le pouvoir antirétroviral des cellules CD8 des contrôleurs naturels. Ces découvertes renforcent la piste des lymphocytes T CD8 dans la recherche contre le sida. Dans d’autres cas, le contrôle post-traitement semble associé à la présence de cellules de l’immunité innée (cellules tueuses naturelles NK) qui empêchent le rebond viral.
Thérapie cellulaire et thérapie génique
Une thérapie cellulaire déjà évaluée dans le cadre de l’infection par le VIH consiste en la greffe de cellules souches afin de remplacer les globules blancs d’une personne avec VIH par des versions résistantes au VIH. C’est ainsi qu’en 2008, une personne avec VIH atteinte d’une leucémie a bénéficié d’une greffe de cellules souches lui permettant également de guérir de l’infection par le VIH, grâce à un donneur compatible qui était par ailleurs homozygote pour le gène muté CCR5-∆32 2. Aujourd’hui, on compte cinq personnes ainsi greffées en rémission ou guéries de l’infection par le VIH dans le monde. Un sixième cas, le patient de Genève, est également en rémission après une greffe de cellules pourtant issues d’un donneur présentant l’allèle sauvage de CCR5 3. La diminution progressive du réservoir viral chez ce patient suite à la greffe pourrait résulter, d’une part, des réactions du greffon contre l’hôte ou de cellules immunitaires particulièrement efficaces contre les dernières traces virales présentes (cellules infectées ou virus circulants), et d’autre part, du traitement immunomodulateur associé à la greffe qui contribuerait à empêcher la réactivation virale. Si ces résultats sont prometteurs, ces interventions lourdes et dangereuses sont uniquement utilisées chez des personnes nécessitant une greffe pour traiter un cancer du sang agressif, et ne peuvent être envisagées comme solution pour toutes les personnes vivant avec le VIH (protocole hautement toxique, risque de rejet de la greffe, difficulté de trouver un donneur compatible avec la mutation CCR5-∆32…).
Des autogreffes sont également envisagées sur le modèle des contrôleurs naturels. Une piste de traitement en cours d’investigation consiste en la reprogrammation ex vivo des lymphocytes T CD8+ des personnes ne contrôlant par le VIH pour leur donner le phénotype des lymphocytes T CD8+ ultra-performants trouvés chez les contrôleurs naturels. Une fois reprogrammés, ces lymphocytes seraient réinjectés dans le cadre d’une thérapie cellulaire 4. L’objectif final étant une interruption de la trithérapie chez ces individus.
Anticorps neutralisants à large spectre
Les anticorps neutralisants à large spectre (broadly neutralizing antibodies – bNAbs) sont des anticorps polyvalents capables de neutraliser de nombreux variants viraux. Découverts dans les années 1990 chez des patients « élites neutralisants » (1 % de la population infectée), ces anticorps capables de reconnaître et neutraliser de nombreuses souches du VIH (95 % des variants pour certains anticorps neutralisants à large spectre) représentent un potentiel d’intérêt majeur pour les chercheurs 5. Un des intérêts de ces anticorps réside en leur maturation sur le long terme : ils sont façonnés au cours du temps en réaction aux mutations du virus, comme par coévolution 6. Il existe en effet une évolution concomitante du virus et de la maturation de ces anticorps : à mesure que le virus échappe à la reconnaissance des anticorps par mutation de l’épitope ciblé, les lymphocytes B continuent de muter et de s’affiner, produisant de nouveaux clones d’anticorps dont le spectre de neutralisation s’élargit progressivement. Ces anticorps neutralisants à large spectre peuvent ainsi mettre deux à trois années à atteindre leur forme définitive et donc leur pleine efficacité, neutralisant une multitude de variants par la reconnaissance d’une région généralement très conservée du virus.
Fixés aux virus circulants, ces anticorps les empêchent de pénétrer dans les cellules immunitaires par formation de complexes immuns favorisant par ailleurs leur élimination. En outre, lorsqu’ils se lient aux lymphocytes T CD4+ infectés, ces anticorps empêchent le relargage des particules virales et attirent les cellules tueuses naturelles, provoquant la destruction des lymphocytes par cytotoxicité cellulaire (Figure 10) 7. Ces anticorps sont ainsi caractérisés par de bonnes capacités neutralisantes et effectrices, ce qui constitue un avantage par rapport aux trithérapies qui ne permettent pas d’éliminer les cellules infectées. Comme pour la trithérapie, ces anticorps neutralisants à large spectre sont plus efficaces lorsqu’utilisés en association 8.
Des lymphocytes T CD4+ sont infectés avec le VIH-1 pendant 48 heures puis cultivés pendant 24 h avec des anticorps neutralisant à large spectre (broadly neutralizing antibodies – bNAbs).
A. Observation en microscopie électronique à transmission. Rétention virale au site de bourgeonnement, comprenant des bNAbs entre une particule virale et un virion bourgeonnant. Les pointes de flèches rouges pointent vers les bNAbs (points noirs). La pointe de flèches jaune montre une particule virale bourgeonnante. Barre d’échelle : 200 nm
B. Observation en microscopie électronique à balayage, avec agrandissement d’une zone présentant une forte fixation de bNAbs (points blancs). Barre d’échelle : 100 nm.
La fixation des anticorps sur les particules virales agrège celles-ci à la surface du LT CD4, empêchant la libération des nouveaux virions et attirant les cellules tueuses naturelles, qui élimineront le lymphocyte infecté.
Vaccination
Plus de 40 ans après sa découverte, il n’existe toujours pas de vaccin contre le VIH, pourtant essentiel pour mettre fin à l’épidémie. Ce virus évolue rapidement du fait d’une transcriptase inverse peu fidèle (1 à 10 mutations par génome viral) associée à un fort taux de réplication virale (109 virions produits par jour sans traitement). La diversité des virions produits rend la mise au point d’un vaccin complexe, les anticorps induits par la vaccination devenant rapidement inefficaces. Par ailleurs, le virus est recouvert d’une couche de glycanes rendant difficile l’interaction des anticorps avec les protéines virales. Le fait que le système immunitaire lui-même soit la cible du virus est aussi une limitation majeure. Enfin, il faut obtenir un vaccin efficace contre le VIH mais également assurer l’élimination du réservoir viral au sein des lymphocytes T CD4+. Deux types de vaccins sont ainsi envisagés : un vaccin prophylactique dont le but est d’éviter l’implantation d’un réservoir, et un vaccin thérapeutique permettant l’élimination d’un large réservoir déjà établi 1.
Aujourd’hui, un espoir majeur réside en la compréhension du développement des anticorps neutralisants à large spectre et la capacité à produire en laboratoire des antigènes similaires aux antigènes viraux : une stratégie prometteuse consiste ainsi à développer un vaccin induisant la production de ces anticorps, capables de neutraliser les divers antigènes du VIH. Les premiers essais cliniques, aux résultats encourageants, sont en cours 23. Cette stratégie vaccinale consiste à concevoir des glycoprotéines d’enveloppe induisant, in vivo, des précurseurs d'anticorps neutralisants à large spectre, puis d’administrer par la suite des immunogènes4 en série permettant de guider la maturation des lymphocytes B naïfs, induisant les multiples mutations nécessaires à la production d’anticorps matures pleinement neutralisants et polyvalents 5.
Une autre approche vaccinale consiste à cibler les cellules dendritiques (centrales dans la mise en place des réponses immunitaires) via un anticorps monoclonal couplé à des molécules de l’enveloppe du VIH. Cet anticorps cible le récepteur CD40 des cellules dendritiques, et dirige de cette façon les antigènes viraux vers ces cellules. Le but de cette méthode est d’accroître l’immunogénicité des antigènes viraux en induisant une réponse immunitaire précoce via les cellules dendritiques 6.
En parallèle, d’autres recherches visent à stimuler la réponse des lymphocytes T cytotoxiques 7. À terme, cette stratégie pourrait être associée à celles des anticorps neutralisants à large spectre dans un vaccin unique afin d’assurer une protection la plus optimale possible, combinant une réponse immunitaire cellulaire et humorale à la fois forte et durable.
PrEP : Prophylaxie pré-exposition. TPE : Traitement post-exposition.
Conclusion
Plus de 40 ans après sa découverte, le VIH reste une préoccupation mondiale. L’épidémie persiste malgré les progrès de la trithérapie dont l’accès demeure inégal dans le monde. Si les dernières avancées sont prometteuses et qu’on entrevoit la mise au point d’un vaccin sur la prochaine décennie, la meilleure solution reste à ce jour la prévention et le dépistage, assurant une protection à la fois individuelle et collective, en espérant atteindre l’objectif international « zéro décès du VIH en 2030 » fixé par l’Organisation mondiale de la santé, le Fonds des Nations unies pour l’enfance (Unicef) et le Programme commun des Nations unies sur le VIH/sida (ONUSIDA). Néanmoins, en raison notamment des suspensions drastiques des financements humanitaires américains survenues début 2025, cet objectif initialement porteur d’espoir semble à ce jour peu réalisable.