De très nombreux organismes vivent dans le sol et y exercent des fonctions écologiques variées. Cette faune du sol est particulièrement étudiée dans le cas des agrosystèmes car elle a un impact sur la production primaire. Elle intervient en effet dans le recyclage des nutriments, dans la structure du sol, dans le contrôle des bioagresseurs et peut modifier les interactions entre espèces végétales.
Les sols, milieux vivants
Une immense diversité
De par leur structure tridimensionnelle, leur large gamme de porosité, la diversité des caractéristiques physico-chimiques et des conditions microclimatiques, les sols abritent un nombre considérable d’organismes. Ainsi, les sols hébergeraient environ un quart des espèces animales actuellement décrites [1]. Cette faune du sol couvre plusieurs échelles de taille, depuis les organismes microscopiques jusqu’à des animaux de plusieurs dizaines de centimètres. Elle regroupe une multitude de taxons exprimant une diversité de formes, de stades de développement, de modes de vie et régimes alimentaires qui ont une incidence sur le fonctionnement physico-chimique du sol à toutes les échelles, depuis l’arrangement des particules élémentaires (échelle texturale) jusqu’à l’arrangement macroscopique des agrégats, des macropores et des horizons de sol (échelle structurale). Tous ces organismes, liés dans les réseaux d’interactions, participent au flux d’énergie dans les écosystèmes.
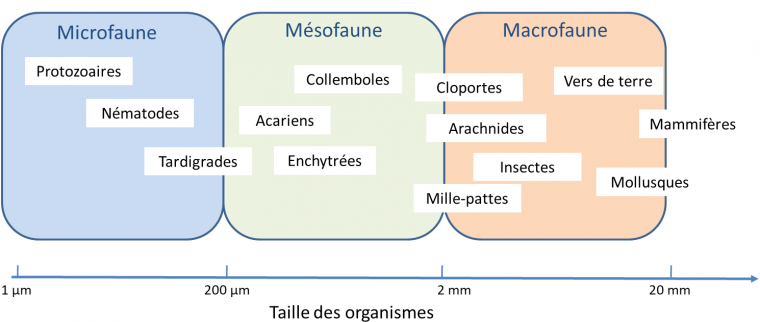
Pour simplifier cette diversité d’organismes, une pratique courante en écologie est de grouper les espèces selon leur taille (Figure 1).
Les animaux dont la taille excède 2 mm sont considérés dans la macrofaune (les cloportes, les mille-pattes, les mollusques, les vers de terre et beaucoup d’arachnides et d’insectes, mais aussi les mammifères), ceux dont la taille est comprise entre 200 μm et 2 mm appartiennent à la mésofaune (collemboles, acariens ou encore enchytrées), et les organismes dont la taille est inférieure à 200 µm sont regroupés dans la microfaune (protozoaires et nématodes). Ces limites sont arbitraires et la gamme de taille de certains taxons chevauche plusieurs groupes.
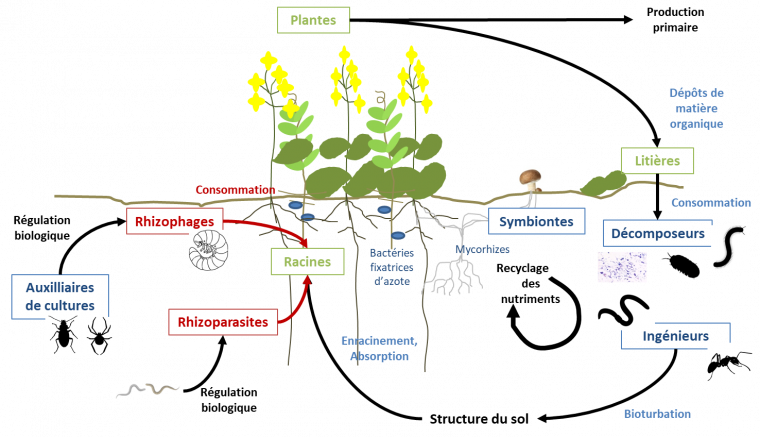
Selon les auteurs, la faune du sol peut aussi être regroupée en groupes fonctionnels, selon leur type d’activités (Figure 2) ou leur niveau trophique.
| Caractéristiques | Ingénieurs chimiques | Régulateurs biologiques | Ingénieurs de l’écosystème |
|---|---|---|---|
| Principaux organismes |
Bactéries |
Protozoaires Nématodes Acariens Collemboles Carabes |
Fourmis Termites Vers de terre |
| Fonctions | — Décomposition de la matière organique — Minéralisation et libération de nutriments — Dégradation des composés toxiques — Transformation de la litière et décomposition de la matière organique |
— Régulation des communautés microbiennes — Régulation de la disponibilité en nutriments |
Création et stabilité des habitats dans le sol — Modification des propriétés physiques — Accumulations de la matière organique — Compaction et décompaction du sol — Formation des sols |
| Taille de l’organisme | 0,5 – 5 µm (bactéries) 2 – 10 µm (diamètre des hyphes mycorhiziens) |
2 – 200 µm (protozoaires) ~ 100 µm (nématodes) 0,5 – 2 mm (acariens) 0,2 – 6 mm (collemboles) |
0,1 – 5 cm (fourmis) 0,3 – 7 cm (termites) 0,5 – 20 cm (vers de terre) |
| Densité dans le sol | 109 cellules/g de sol (bactéries) 10 m/g sol (hyphes) |
106 individus / g sol (protozaires) 10 à 50 individus/ g sol (nématodes) 103 à 105 individus / m² sol (acariens) 102 à 104 individus / m² sol (collemboles) |
102 à 103 individus / m² sol (fourmis) 10 à 500 individus /m² sol (vers de terre) |
Cette approche est basée sur le postulat que ces espèces ainsi groupées impactent de façon identique certaines fonctions écologiques, telles que la bioturbation ou le biocontrôle. Même s’il ne permet pas de prendre en compte toute la variabilité des espèces, leur renouvellement et leurs interactions, ce regroupement est utile car il satisfait un besoin de simplification.
Écologie fonctionnelle des sols autour des plantes
Un des enjeux de l’écologie fonctionnelle des sols est de comprendre les relations entre la plante cultivée et son environnement biophysique incluant les interactions biologiques et les effets de la biodiversité. Si le service final attendu est la production agricole, certains services intermédiaires (ensemble de fonctions qui ont un effet sur le service final) peuvent être mobilisés. Ainsi, on note un nombre d’études croissant sur ce sujet depuis les 30 dernières années. Ces études ont relayé l’importance des organismes des sols dans la réalisation de grandes fonctions écologiques des sols agricoles telles la production primaire, la dynamique du carbone et le recyclage des nutriments, le maintien de la structure des sols, la dynamique de l’eau et la régulation des bioagresseurs. Cependant les sols hébergent aussi des organismes néfastes pour les cultures ou qui peuvent indirectement affecter la production primaire via des boucles de rétroaction. Par exemple, des effets positifs et négatifs des communautés des sols peuvent s’annuler et la résultante sur la productivité des plantes reste inchangée [2]. En réalité, le bilan net de l’effet de la biodiversité des sols sur le fonctionnement des écosystèmes dépend du nombre de fonctions étudiées [3]. C’est pourquoi il est important de considérer la multifonctionnalité des organismes des sols pour mieux comprendre le rôle de la biodiversité des sols sur la production agricole.
Implications de la faune du sol pour la production primaire
D’après une méta-analyse, la présence de vers de terre augmente significativement le rendement (+ 25 %) et la biomasse (totale, aérienne et souterraine, d’environ + 20 % chacune) des plantes cultivées [4]. Plus généralement, l’impact de la faune du sol sur la production primaire peut être vu au travers de ses effets sur les fonctions de (i) recyclage des nutriments, (ii) entretien de la stabilité/structure du sol, (iii) contrôle des bioagresseurs et (iv) support de biodiversité (Figure 3). Ces fonctions écosystémiques sont respectivement associées du point de vue des plantes à (i) leur nutrition, (ii) le milieu physique dans lequel les plantes se développent, (iii) leur santé et (iv) les interactions entre plantes. L’effet de la faune du sol sur chaque fonction peut être expliqué par de nombreux processus et mécanismes qui impliquent l’ensemble des organismes des sols. Ces différents processus sont abordés dans les paragraphes suivants.
Les boites indiquent les différents groupes fonctionnels impliqués dans les services écosystémiques (en noir), les éléments bleu représentent les processus à effets positifs sur les plantes, les éléments en rouge représentent les processus à effets négatifs.
Fonction 1 : recyclage des nutriments pour la nutrition des plantes
Disponibilité des nutriments
L’effet positif des vers de terre sur la croissance des plantes serait principalement dû à la modification de la disponibilité des nutriments et, en particulier, de l’azote (Van Groeningen et coll., 2014b). Néanmoins, cet effet des vers de terre varie d’une espèce de plante à l’autre. Par exemple, il tend à disparaître en présence de légumineuses, car ces plantes sont capables de fixer l’azote atmosphérique grâce à une symbiose racinaire avec une bactérie Rhizobium sp.
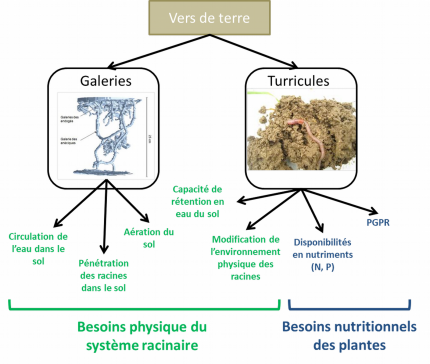
Plusieurs mécanismes permettent d’expliquer l’effet positif des vers de terre sur la disponibilité de l’azote (Figure 4).
PGPR = plant growth promoting rhizobacteria, rhizobactéries favorisant la croissance des plantes. Crédits photo : Guénola Pérès, AgroCampusOuest.
Tout d’abord, les turricules (rejet des vers de terre présents à la surface du sol) fraîchement produits sont riches en ammonium (NH4+) issu de la minéralisation de la matière organique ingérée. Ce NH4+ est progressivement nitrifié. On observe alors une bascule entre ammonium et nitrate (NO3-) à mesure que les turricules vieillissent. Selon les quantités en NO3- et leur humidité, les turricules sont aussi un siège de la dénitrification (émissions de N2O), ce qui peut varier d’une espèce lombricienne à une autre. Les parois de galeries, tapissées de mucus ou déjections, sont aussi enrichies en NO3-, NH4+ et ont des populations de bactéries nitrifiantes et dénitrifiantes plus importantes que le reste du sol. Cela peut faciliter le transport vertical du NO3- vers les couches plus profondes du sol où les conditions sont moins favorables à la nitrification. Enfin, les mucus et les tissus en décomposition des animaux sont aussi des voies d’entrée d’azote dans le système sol-plante. Ainsi, les vers de terre pourraient contribuer à hauteur de 10-30 % de l’azote assimilé par les plantes selon les conditions climatiques et la végétation considérée.
Les turricules et le mucus des vers de terre contiennent aussi des quantités de phosphore disponible plus fortes que celles du sol et équivalentes à 50 % des besoins annuels des plantes. Des modifications de la forme et de la localisation du phosphore ont lieu dans le tube digestif des vers de terres par au moins trois voies [5] : (i) une modification de pH, (ii) l’émission forte de mucus qui modifie la sorption du phosphore et augmente sa disponibilité, et (iii) l’augmentation de l’activité microbienne pendant le processus de digestion.
Mis à part les lombriciens, d’autres groupes d’animaux des sols participent à la disponibilité des nutriments pour les plantes. Le NO3- issu du NH4+ excrété par les protozoaires est suspecté d’influencer l’architecture racinaire, avec une prolifération des racines latérales dans les microzones plus riches en nitrates. De plus, le broutage des microorganismes par les nématodes augmente la disponibilité des nutriments et leurs prélèvements par la plante [6]. Les collemboles sont également reconnus pour leur contribution à la dynamique de l’azote, par leur activité de broutage des champignons.
Effets sur les mycorhizes
Les interactions entre les invertébrés des sols et les champignons mycorhiziens ont des impacts indirects mais importants sur la croissance des plantes. Des études ont établi que les microarthropodes (en particulier les collemboles) influencent négativement la distribution et la densité des champignons mycorhiziens par le broutage. L’intensité du broutage des hyphes dépend des espèces mycorhiziennes, les organismes de la faune du sol ayant des préférences dans leur diète. Les collemboles et les acariens préfèrent brouter des champignons saprophages, et en présence de champignons mycorhiziens, ils consomment les extrémités les plus distantes des racines [7].
D’autres organismes, en particulier certains détritivores tels les termites et les mille-pattes, ont au contraire un effet positif sur le réseau mycélien car ils ingèrent puis dispersent l’inoculum mycorhizien. Des coléoptères carabiques et scarabéides ont aussi été retrouvés avec des spores dans leur système digestif. Les lombriciens accumulent et dispersent les spores via leurs turricules, probablement en consommant les racines mycorhizées sénescentes.
L’usage de pesticides est susceptible de profondément modifier les interactions entre faune du sol et symbiose mycorhizienne. En effet, l’usage de glyphosate a un faible effet à court terme sur les vers de terre mais un effet important sur les champignons mycorhiziens et sur l’interaction entre champignons et lombrics [8]. Or, un déclin des champignons mycorhiziens implique une fertilisation plus forte des cultures avec de forts coûts écologique et économique.
Fonction 2 : dynamique de la structure des sols
Généralités
La bioturbation est la formation, par l’action des êtres vivants, de biostructures et biopores dont les propriétés sont différentes de celles du sol environnant. Cela s’explique par (i) le remaniement du sol pouvant venir d’horizons profonds, (ii) la modification texturale des sols suite au tri granulométrique effectué par les organismes (à l’inverse des éléments grossiers, les éléments fins peuvent être ingérés puis rejetés dans les déjections), et (iii) la modification des agrégats du fait du passage dans le tube digestif des organismes humivores ou du remaniement par les pièces buccales des termites, par exemple. En conséquence, les effets de la bioturbation se répercutent sur plusieurs échelles, de la particule d’argile au profil de sol.
Activité fouisseuse
On distingue (i) les organismes fouisseurs (taupes, campagnols, scarabées) qui creusent essentiellement avec leurs pattes modifiées ou non, (ii) les mineurs qui creusent leur chemin avec leurs mandibules ou leurs dents transportant la terre à l’extérieur (fourmis, termites) ou la repoussant derrière eux (larves de hannetons), et (iii) les tunneliers forant des galeries soit en forçant le passage et en profitant d’une porosité déjà existante (mille-pattes type diplopode, vers de terre) soit en consommant la terre et en la rejetant sous forme de déjection (vers de terre) [9].
L’activité fouisseuse des lombriciens va aboutir à la création de macropores sous la forme de galeries et de logettes d’estivation. En prairie tempérée, la longueur totale des galeries peut atteindre 890 m par m² de sol. Par ailleurs, l’activité fouisseuse des vers va aussi être conditionnée par les caractéristiques environnementales, notamment la teneur en matière organique des sols et l’accès à la ressource trophique, la compaction du sol, les interactions entre espèces, l’usage des sols et la saison. Ces galeries ont un rôle très important dans le fonctionnement hydrique des sols car elles constituent des voies d’écoulement préférentiel pour l’eau et ses solutés. L’effet des galeries sur l’infiltration est très fortement conditionné par les caractéristiques des réseaux de galeries ; ainsi le diamètre des galeries, la tortuosité et l’interconnexion augmentent l’infiltration et la conductivité. Une contrainte majeure à notre appréciation du rôle de ces galeries dans le fonctionnement hydrodynamique des sols est notre faible connaissance de leurs durées de vie.
Production d’agrégats
Les organismes du sol produisent des agrégats lors de l’ingestion de sol combinée ou non à l’ingestion de la matière organique prélevée à la surface du sol. Ces fractions minérales et organiques ingérées sont mixées lors du transit dans le tube digestif des organismes et excrétées sous la forme de déjections, soit dans le sol soit à la surface du sol. Les propriétés de ces déjections dépendent des groupes biologiques, de la localisation de la ressource trophique, des conditions pédoclimatiques et de la densité du sol. On estime que 240 tonnes de déjections (endogées et de surface) sont produites annuellement par hectare pour une densité de 1 tonne de vers de terre en prairie. Ces déjections déposées dans le sol vont influencer directement la compaction des sols. La production de ces agrégats, soit de surface (turricules) soit souterrains, va aussi agir sur la régulation hydrique. Ainsi, en climat tempéré, l’introduction de vers de terre permet, au bout de 10 ans, d’améliorer de 25 % la capacité de rétention en eau du sol, et donc la réserve en eau utilisable par les plantes.
Stabilité structurale des agrégats
La stabilité structurale des agrégats du sol est fortement liée aux propriétés du sol, notamment la texture, la minéralogie des argiles, la teneur en cations et en oxydes d’aluminium et de fer, ou encore la teneur en matière organique. Cela étant, les organismes du sol contribuent aussi au maintien de cette structure. Les champignons créent un maillage d’hyphes autour des particules. Les bactéries et dans une moindre mesure les champignons agissent aussi en produisant des exopolysaccharides qui constituent une colle entre les agrégats. En complément, les invertébrés agissent aussi sur la stabilité des agrégats. Par exemple, les lombriciens augmentent la taille des agrégats, la quantité d’agrégats stables et leur distribution en stimulant l’activité microbienne et en enrichissant en carbone organique leurs déjections. Mais cette action est très variable dans le temps : les déjections récentes sont peu stables alors qu’elles sont plus stables que le sol environnant lorsqu’elles sont plus âgées. De plus, l’influence des lombriciens sur l’agrégation dépend aussi des espèces et de leurs interactions.
Fonction 3 : contrôle des bioagresseurs
Généralités
La faune du sol modifie les relations entre les plantes et leurs bioagresseurs. Lorsque ces effets sont bénéfiques à l’agriculture, les animaux prédateurs sont considérés comme des auxiliaires des cultures. Toutefois, dans certains cas l’effet des animaux du sol peut ne pas être bénéfique. Les effets connus sur la régulation des adventices, des ravageurs et des pathogènes sont détaillés dans les trois sous-parties ci-après.
Régulation des adventices
La faune du sol participe à la régulation des adventices de nombreuses manières. Certains animaux consomment les graines, participent à la distribution spatiale et temporelle des graines ou encore influencent la croissance des plantules. Il existe de nombreuses observations de la consommation de graines sur la plante avant la dispersion, notamment par les coléoptères carabiques. Après dispersion, beaucoup d’invertébrés se nourrissent de graines comme les carabiques, les cloportes, les vers de terre ou les limaces.
Bien que les graines soient généralement de bonne valeur énergétique, elles sont, d’un point de vue structurel et nutritionnel, différentes selon les espèces végétales. La consommation ne se fait pas au hasard, et les animaux ont des préférences pour certaines graines en fonction de leur taille, leur forme, leur ornementation ou leur contenu lipidique. Par exemple, les carabiques sont des coléoptères primitivement prédateurs mais plusieurs espèces ont établi des symbioses digestives avec des bactéries qui leur permettent de consommer certaines graines. D’autre part, les vers de terre ont une action directe sur la distribution verticale, horizontale et temporelle des graines, avec des quantités dans les turricules plus importantes que dans le sol adjacent. De plus, il a été démontré que le mucus des lombriciens a des effets qui peuvent être à la fois négatifs (forte concentration en NH4+ qui peut induire une dormance des graines ou un retard de germination) et positifs (présence de molécules rhizogéniques) sur la germination des graines. Ainsi, les préférences des vers ont des répercussions sur la compétition entre plantes.
Atténuation de l’effet des ravageurs aériens
Les relations biotiques aériennes et souterraines sont d’une importance majeure sur les traits de défense des plantes [10], et sur leur variation génétique. Or, les travaux actuels sous-estiment le potentiel des ennemis naturels des herbivores sur la tolérance aux ravageurs (croissance) et la défense des plantes. Il devient donc nécessaire d’appréhender la réponse des plantes aux bioagresseurs dans un réseau d’interactions faisant intervenir plusieurs niveaux trophiques souterrains et aériens.
De nombreux herbivores ravageurs des cultures passent par un stade de développement inféodé au sol (par exemple larve, nymphe, pupe) ou transitent par la surface du sol par exemple lors d’une chute. On peut citer certains coléoptères (par exemple pucerons, altises, charançons, méligèthes), diptères (par exemple cécidomyies et autres mouches), les chenilles de lépidoptères (par exemple pyrales, tordeuses), les hémiptères (par exemple pucerons, cicadelles, cochenilles) ou les gastéropodes (limaces). Les prédateurs en surface du sol (carabes, araignées, staphylins, perce-oreilles, larves d’insectes) sont des auxiliaires dans la lutte contre ces ravageurs. D’autre part, les organismes herbivores souterrains (consommant des racines) peuvent modifier la survie, la fécondité, la croissance des herbivores aériens. De façon synthétique, deux grands ensembles de mécanismes relient les bioagresseurs aériens et souterrains. D’une part, l’action des herbivores aériens, en limitant le développement foliaire par exemple, peut avoir un effet sur le développement racinaire et donc sur les herbivores souterrains. L’inverse est également possible. D’autre part, l’induction par des bioagresseurs de la synthèse de composés de défense par la plante va affecter l’ensemble des bioagresseurs, quelle que soit leur localisation
Enfin, un autre réseau d’interactions relie détritivores, plantes et herbivores. Les effets des détritivores semblent aller dans le sens d’une amélioration de la résistance des plantes aux herbivores aériens.
Régulation des populations de pathogènes
Le broutage des champignons pathogènes par les fongivores dans les sols modifie (i) les interactions plante-champignon, (ii) la compétition entre champignons et (iii) la dispersion des spores. Les collemboles sont connus pour consommer sélectivement les champignons, dont certains pathogènes. La viabilité des spores fongiques après passage dans le tube digestif de collemboles est faible, et n’est pas considérée comme suffisante pour induire une maladie chez les plantes.
Toutefois, les organismes des sols peuvent participer à la dissémination de propagules des pathogènes. Ainsi, les collemboles, les fourmis, les termites, ou les escargots sont d’importants disséminateurs.
Plusieurs mécanismes sont impliqués dans la régulation des pathogènes, et notamment lors des phases libres. Ainsi, il a été montré que les nématodes phytoparasites peuvent être grandement affectés par la bioturbation due aux vers de terre. D’autre part, l’augmentation de la diversité des nématodes participe à l’augmentation de la compétition entre espèces et réduirait la pathogénicité des nématodes phytoparasites.
Fonction 4 : modification des interactions entre plantes
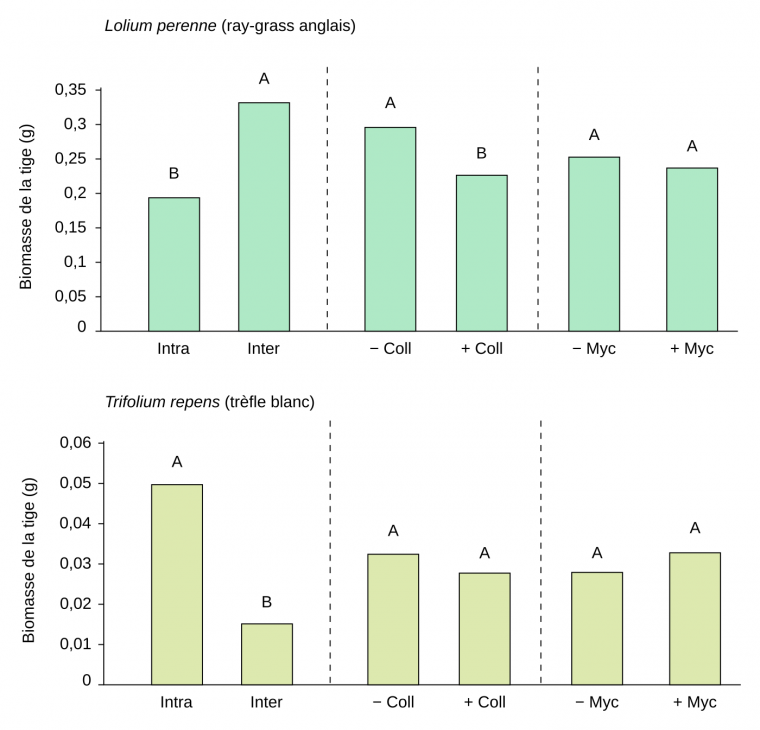
Un nombre croissant d’études ont été réalisées depuis le milieu des années 1990 pour élucider le rôle des animaux du sol sur les interactions entre plantes. Cependant le sujet d’étude est vaste et les conclusions apportées aujourd’hui par ces études restent fragmentaires. Par exemple, le collembole Protaphorura fimata modifie la compétition entre une légumineuse, le trèfle blanc, et une graminée, le ray-grass [11]. Alors qu’en l’absence de collembole, le ray-grass est plus compétitif que le trèfle, la présence du collembole diminue la biomasse aérienne du ray-grass (Figure 5). De plus, la composition (et non le nombre d’espèces) des communautés de collemboles module la productivité, mais uniquement de certains types de plantes, les collemboles ayant un effet positif plus marqué sur les herbacées dicotylédones non fixatrices que sur les graminées ou les légumineuses. La composition en espèces de collemboles joue un rôle important car deux espèces fonctionnellement proches ont une forte probabilité d’interaction négative et donc de diminution de leur performance sur la dynamique des nutriments.
Des plants de ray-grass anglais (Lolium perenne) et de trèfle blanc (Trifolium repens) sont cultivés dans différents conditions : en situation de compétition intraspécifique (Lolium-Lolium ou Trifolium-Trifolium) ou de compétition interspécifique (Lolium-Trifolium), avec ou sans collembole de l'espèce Protaphorura fimata et avec ou sans champignon mycorhizien de l'espèce Glomus intraradices. La biomasse de la tige est mesurée après huit semaines. Des colonnes ayant des lettres identiques ne présentent pas de différence statistiquement significative.
D’autre part, l’activité des vers de terre s’oppose à la dominance de la légumineuse (trèfle blanc) en augmentant fortement la biomasse du ray-grass [12]. L’augmentation de la disponibilité en azote par l’activité lombricienne a probablement augmenté les capacités compétitrices du ray-grass. D’un autre côté, les vers de terre augmentent la croissance et les performances du trèfle douteux dans un assemblage de trois espèces comprenant cette légumineuse, un pâturin et un séneçon [13]. Les mécanismes proposés sont l’augmentation de la disponibilité du phosphore et de la nodulation des légumineuses. Puisque les animaux augmentent la disponibilité du phosphore et de l’azote dans le sol, mais avec des ordres de grandeur différents, ils peuvent changer le rapport N/P disponible et affecter la dominance des espèces à court terme et à long terme [14], les légumineuses étant supposées être plus compétitrices dans les sols avec des rapports N/P faibles. Ainsi, les turricules de sub-surface produits par les vers de terre jouent un rôle important dans la structuration des communautés de plantes en affectant spécifiquement certains groupes fonctionnels (herbacées vs légumineuses) [15].
Enfin, les rhizophages altèrent les peuplements végétaux en consommant certaines racines plutôt que d’autres. Par exemple, l’herbivorie d’un peuplement végétal par des larves de taupin peut induire des effets à long terme en (i) augmentant la biomasse végétale totale d’un nouveau peuplement végétal poussant dans le même sol, (ii) augmentant la capacité de résistance des plantes à une attaque d’herbivore et (iii) en changeant la compétitivité de certaines de ces espèces [16]. L’hypothèse principale est une modification des communautés de champignons mycorhiziens lors de la première phase d’herbivorie.
Toutefois, il existe aussi des cas où les communautés de plantes ne sont pas affectées par une manipulation des organismes des sols, principalement dans le cas de plantes pérennes. Les observations suggèrent que (1) ces communautés végétales sont moins réactives ou réagissent plus lentement aux modifications de disponibilité en nutriments, (2) les effets sur le long-terme (modification de la structure physique du sol) semblent être plus importants que les effets à court-terme (modification de la disponibilité des nutriments), (3) les manipulations d’abondance/biomasse réalisées dans ces essais étaient trop faibles pour induire des effets et (4) les contraintes en termes de disponibilité en nutriments ou de milieu physique étaient trop faibles, de sorte que les lombriciens n’ont pas pu avoir d’effet levier par suppression/diminution de contrainte.
Piloter la biodiversité des sols ?
La biodiversité représente un atout pour l’agriculture. Pourtant, de nombreuses publications énoncent une diminution de la biodiversité dans les agroécosystèmes sous l’effet de la forte utilisation des produits phytosanitaires ainsi que de la fragmentation des habitats naturels. Cette diminution peut agir sur les interactions biologiques et induire un plus faible niveau de services rendus, notamment concernant la pollinisation ou le contrôle des ravageurs, la disponibilité en nutriments ou la stabilité des sols. Cette prise de conscience a conduit à une évolution des pratiques agricoles et à la création de nouvelles agricultures, telles que l’agroécologie ou l’agriculture de conservation, en plaçant les interactions biotiques et les régulations biologiques au cœur des processus de production. L’idée est de « cultiver la biodiversité » du sol afin de maintenir, voire d’améliorer, des services rendus grâce au pilotage de la biodiversité.
Références
- Decaëns T., Jiménez J.J., Gioia C., Measey J., Lavelle P., 2006. The values of soil animals for conservation biology. European Journal of Soil Biology, 42, 23-28.
- Wurst S., Allema B., Duyts H., Van Der Putten W.H., 2008. Earthworms counterbalance the negative effect of microorganisms on plant diversity and enhance the tolerance of grasses to nematodes. Oikos, 117 (5), 711-718.
- Wolters V., 2001. Biodiversity of soil animals and its function. European Journal of Soil Biology, 37 (4), 221-227.
- Van Groenigen J.W., Lubbers I.M., Vos H.M.J., Brown G.G., De Deyn G.B., Van Groenigen K.J., 2014. Earthworms increase plant production : a meta-analysis. Scientific Reports, 4.
- Le Bayon R.C., Milleret R., 2009. Effects of earthworms on phosphorus dynamics – a review. Dynamic Soil, Dynamic Plant, 3 (Special Issue 2), 21-27.
- Irshad U., Villenave C., Brauman A., Plassard C., 2011. Grazing by nematodes on rhizosphere bacteria enhances nitrate and phosphorus availability to Pinus pinaster seedlings. Soil Biology & Biochemistry, 43 (10), 2121-2126.
- Klironomos J.N., Kendrick W.B., 1996. Palatability of microfungi to soil arthropods in relation to the functioning of arbuscular mycorrhizae. Biol. Fert. Soils, 21, 43-52.
- Zaller J.G., Heigl F., Ruess L., Grabmaier A., 2014. Glyphosate herbicide affects belowground interactions between earthworms and symbiotic mycorrhizal fungi in a model ecosystem. Scientific Reports, 4, 5634.
- Gobat J.-M., Aragno M., Matthey W., 2003. Le sol vivant. Bases de pédologie – Biologie des sols, Lausanne, Gérer l’environnement, 568 p.
- Van Geem M., Gols R., Van Dam N., Van Der Putten W., Fortuna T., Harvey J., 2013. The importance of aboveground–belowground interactions on the evolution and maintenance of variation in plant defense traits. Frontiers in Plant Science, 4 (431).
- Endlweber K., Scheu S., 2007. Interactions between mycorrhizal fungi and Collembola : effects on root structure of competing plant species. Biology and Fertility of Soils, 43 (6), 741-749.
- Wurst S., Langel R., Scheu S., 2005. Do endogeic earthworms change plant competition ? A microcosm study. Plant and Soil, 271, 123–130.
- Thompson L., Thomas C.D., Radley J.M.A., Williamson S., Lawton J.H., 1993. The effect of earthworms and snails in a simple plant community. Oecologia, 95 (2), 171-178.
- Wurst S., Langel R., Reineking A., Bonkowski M., Scheu S., 2003. Effects of earthworms and organic litter distribution on plant performance and aphid reproduction. Oecologia, 137 (1), 90-96.
- Partsch S., Milcu A., Scheu S., 2006 Decomposers (Lumbricidae, Collembola) affect plant performance in model grasslands of different diversity. Ecology, 87 (10), 2548-2558.
- Sonnemann I., Hempel S., Beutel M., Hanauer N., Reidinger S., Wurst S., 2013. The root herbivore history of the soil affects the productivity of a grassland plant community and determines plant response to new root herbivore attack. Plos One, 8 (2), e56524.