Les poissons téléostéens communiquent entre eux selon des modalités diverses. Après avoir présenté les caractéristiques de la communication acoustique chez les poissons, cet article détaille des expériences réalisées chez l'espèce Maylandia zebra et qui visent à caractériser les rôles des communications acoustique et visuelle dans le contexte d'interactions agonistiques.
Généralités sur la communication
Pourquoi communiquer ?
Les animaux peuvent communiquer avec leurs congénères (communication intraspécifique) ou avec les membres d’autres espèces (communication interspécifique). Les fonctions remplies par la communication sont variées : se signaler auprès d’un partenaire sexuel, indiquer une source de nourriture, défendre son territoire, communiquer avec ses petits, dissuader un prédateur…
Qu’est-ce que la communication ?
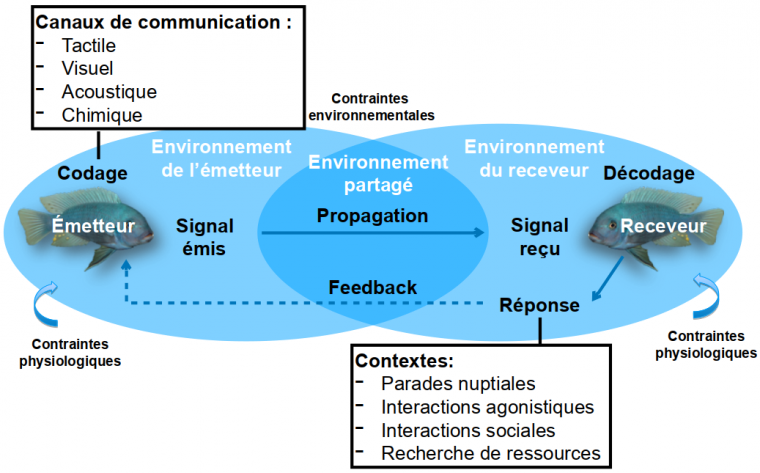
Si plusieurs définitions existent, la communication est généralement définie comme la production, la transmission et la réception d’un signal porteur d’information, impliquant au moins deux individus : l’émetteur qui envoie le signal et le receveur qui le perçoit (Figure 2). Les messages peuvent transmettre des informations spécifiques et individuelles sur l’émetteur, comme son sexe, sa taille, son âge, sa motivation, son état physiologique… La réception du signal peut provoquer une réponse comportementale et/ou physiologique du receveur qui, elle-même, peut engendrer une réponse de l’émetteur en retour.
Il existe plusieurs types de canaux de transmission des signaux : visuel, acoustique, chimique ou encore mécanique (avec, par exemple, les signaux tactiles). En fonction de leur nature et des caractéristiques du milieu de propagation, les signaux se propagent plus ou moins loin. Par exemple le chant d’un oiseau ne se propagera pas de la même façon dans un milieu ouvert ou dans une forêt. Si les signaux visuels, acoustiques et mécaniques sont éphémères, les signaux chimiques peuvent, eux, persister plus longtemps dans l’environnement. Enfin, la communication peut être unimodale, c’est-à-dire n’employer qu’un seul canal, ou multimodale, en reposant sur plusieurs canaux utilisés de façon conjointe ou séquentielle chez une même espèce et dans différents contextes.
Les caractéristiques de la communication acoustique
L’exemple développé dans la seconde partie de cet article, repose sur la communication acoustique dont les modalités sont donc présentées plus en détails dans ce qui suit.
Le son est constitué d’ondes qui se définissent suivant trois paramètres principaux : la fréquence, l’amplitude, la durée. La fréquence est le nombre de vibrations par unité de temps, elle exprime la hauteur du son (grave ou aigu). Trois gammes de fréquences sont définies en référence aux capacités auditives humaines : les fréquences inférieures à 20 Hz ou infrasons, les fréquences comprises entre 20 Hz et 20 kHz qui sont audibles par l’oreille humaine et les fréquences supérieures à 20 kHz ou ultrasons. L’amplitude correspond à l’ampleur de chaque vibration, conférant ainsi au son une intensité. La durée du son correspond au temps mesuré depuis le début de la première pulsation jusqu’à la fin de la dernière (Tanzarella, 2006).
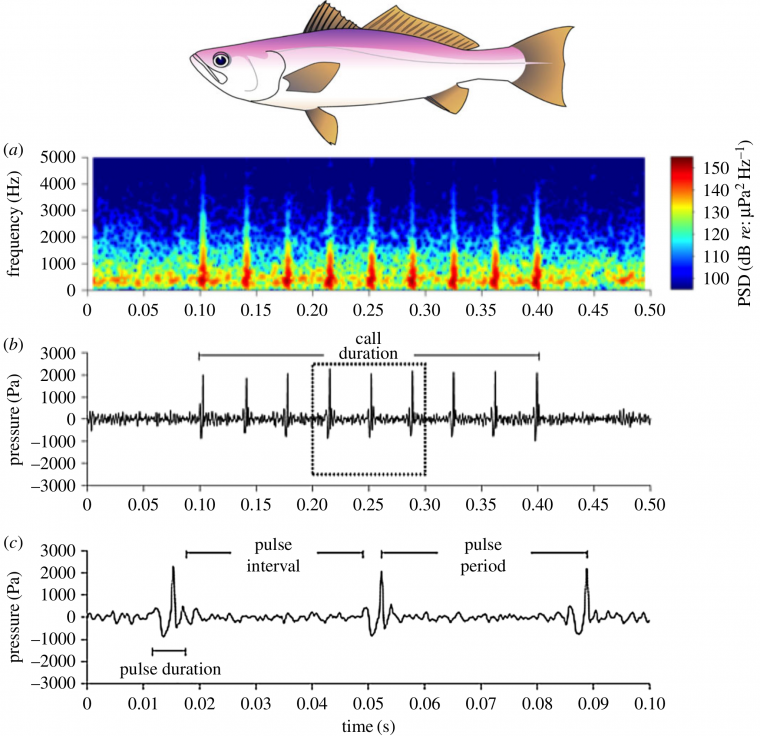
La diversité des modalités de production sonore chez les poissons (que l’on abordera plus loin) engendre différents types de sons de par leur fréquence, leur intensité, leur rythme et leur durée. D’une manière générale et pour simplifier, les sons produits par les poissons, sont constitués de trains de pulsations (pulses en anglais). La représentation de l’amplitude du son en fonction du temps, appelée oscillogramme, est très utile pour déterminer les paramètres temporels d’un son comme sa durée, sa période (rythme), le nombre de pulses, etc. Le spectrogramme représente la fréquence et l’intensité d’un son en fonction du temps (Figure 3).
Cynoscion othonopterus est l’espèce qui détient le record du son le plus fort émis par des poissons. Le son est composé de neuf pulses. A. Spectrogramme. La gamme de couleurs indique la densité spectrale de puissance (PSD, pressure spectral density) B. Oscillogramme du son entier. C. Oscillogramme montrant le détail de trois pulses. Illustration du poisson par L. G. Allen.
Les mécanismes de production des signaux acoustiques chez les poissons
Les mécanismes de production du son chez les poissons sont très variés, en voici quelques exemples.
Les vibrations musculaires
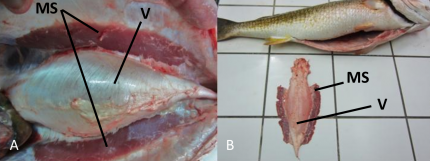
Les tambours rouges mâles émettent, pendant la saison de reproduction, de puissants sons ressemblant au bruit d’un tambour (Parmentier et al. 2014). A. La vessie et les muscles soniques dans la cavité abdominale après retrait du système digestif et de la graisse. B. La vessie natatoire et les muscles soniques une fois retirés. Source : Jérémy Tock, Étude du mécanisme de production de son chez Sciaenops ocellatus, mémoire de master.
La contraction de muscles spécialisés capables de se contracter très rapidement, appelés muscles soniques, provoque des vibrations souvent amplifiées par la vessie natatoire qui joue alors le rôle d’une caisse de résonance (Figure 4).
Les stridulations
Les stridulations correspondent aux sons obtenus suite au frottement entre deux éléments durs, comme les dents ou des os. Chez certaines espèces de poisson chat, les stridulations sont obtenues par frottement entre la nageoire pectorale et la ceinture scapulaire.
Le passage d’air à travers un orifice
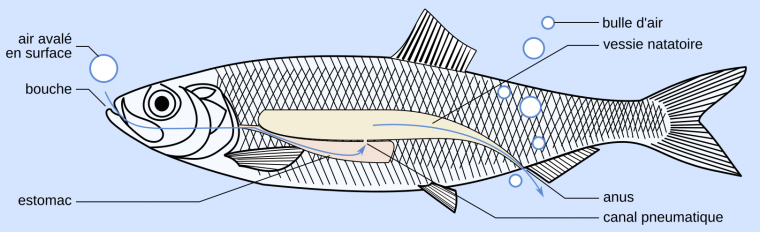
Une vibration peut être obtenue par le passage d’un fluide (eau ou air) à travers une partie du corps de l’animal. Par exemple chez le hareng, les sons sont produits par expulsion de bulles de gaz par l’anus (Wahlberg & Westerberg, 2003) (Figure 5).
Les harengs produisent des sons en émettant de l'air par leur anus. L'air avalé en surface passe dans l'estomac, la vessie natatoire, puis peut être émis au niveau de l'anus (flèches bleues). Les auteurs d'une étude suédoise parue en 2003 à ce sujet ont nommé ces sons « gazouillis pulsés » (pulsed chirps). Ils consistent en une série de 7 à 50 pulsations de 32 à 133 ms de long et dont la fréquence décroît de 4 à 3 kHz au cours du gazouillis. Cette baisse de fréquence s'expliquerait par le mécanisme proposé d'émissions des bulles. D'abord petite et collée à l'anus, la bulle grandirait par l'ajout de petites quantités d'air, ce qui provoquerait à chaque fois une pulsation. Une fois devenue trop grande, la bulle se détacherait. Ces bulles pourraient être utilisées par les bancs de harengs pour créer une barrière face aux prédateurs ou pour la communication intraspécifique. NB : les bulles ne sont à l'échelle puisqu'elles mesurent, en laboratoire, entre 0,5 et 1,5 mm de rayon.
D'après Wahlberg et Westerberg, 2003, Aquatic Living Resources. Image de hareng : MaxxL, CC BY-SA, Wikimedia
Les mécanismes de perception des signaux acoustiques chez les poissons
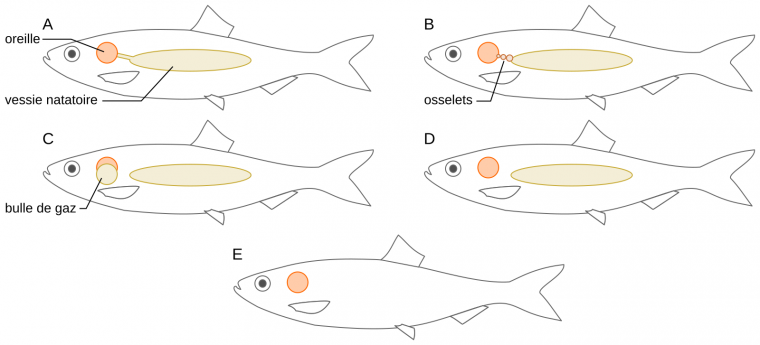
La plupart des Téléostéens (poissons osseux dont la nageoire caudale présente une symétrie apparente) possèdent des oreilles internes consistant en trois canaux semi-circulaires et trois otolithes. Toutefois, ils présentent des capacités auditives variées en fonction des structures impliquées dans l’audition qu’ils possèdent. D’une façon générale les poissons téléostéens peuvent être divisés en deux grands groupes : les spécialistes et les généralistes de l’audition. Dans le premier groupe, l’oreille interne est reliée à la vessie natatoire, ou à des cavités remplies d’air, par des structures variées allant de simples conduits à des structures formant des osselets (ou organe de Weber). Chez les poissons dits généralistes, l’oreille interne n’est pas reliée à la vessie natatoire ou à d’autres cavités (Figure 6). Chez les Cichlidés, différents systèmes existent en fonction de l’espèce considérée (voir la revue de Ladich, 2016).
Relations schématiques entre l’oreille interne et les structures périphériques chez des poissons spécialistes de l’audition (A-D) ou généralistes (D-E). A. Connexion directe entre la vessie natatoire et l’oreille interne via une extension antérieure de la vessie. Cette situation se retrouve par exemple chez le cichlidé Etroplus maculatus. B. Présence d’un organe de Weber constitué d’une chaîne d’osselets. C. Connexion entre l’oreille interne et des cavités remplies d’air. D. Aucune connexion entre l’oreille interne et la vessie natatoire. Dans ce cas la vessie natatoire peut jouer un rôle dans l’audition (chez les poissons demoiselles) ou pas (chez le poisson crapaud). E. Absence de vessie natatoire (poissons plats).
Chez les poissons il existe aussi un système sensoriel impliqué dans la perception des stimuli hydromécaniques. Le moindre mouvement d’un poisson, d’un prédateur ou d’un objet dans le milieu produira un signal qui sera capté par des groupes de cellules ciliées localisés sur la peau ou à l’intérieur de canaux, sur la totalité du corps de l’animal et plus particulièrement le long de leur ligne latérale (Janssen & Strickler, 2006). Ces stimuli seront utiles dans la traque d’une proie par un prédateur (Hanke et coll., 2000), ou pour coordonner les individus au sein d’un banc de poisson (Partridge, 1982).
Le rôle de la communication acoustique chez un poisson cichlidé
Le modèle biologique : Maylandia zebra
Maylandia zebra est un poisson de la famille des Cichlidés, endémique du lac Malawi en Afrique du Sud. C’est un poisson territorial vivant en groupes hiérarchisés dans les parties rocheuses du lac qui leur offrent de multiples abris. Leurs larges mâchoires leur permettent de se nourrir d’algues à la surface des rochers ainsi que de plancton présent dans l’environnement (Konings, 2007). Pour délimiter leur territoire, les mâles M. zebra déplace du sable avec leur bouche et leur corps. C’est sur ce territoire que les mâles fécondent les ovocytes émis par les femelles. Celles-ci récupèrent les œufs fécondés et les incubent dans leur cavité buccale durant trois semaines. Chez cette espèce, les mâles n’apportent ni ressources ni soins parentaux aux femelles et aux jeunes. À leur naissance, les juvéniles se dispersent très peu et les adultes sont fortement philopatriques, c’est-à-dire qu’ils restent proches de l’endroit où ils sont nés. Les mâles dominants arborent des rayures très marquées sur un corps bleu ; les femelles ont une coloration plus terne.
M. zebra appartient au groupe des poissons mbunas qui rassemble une grande diversité d’espèces associées à de nombreux comportements différents. Les poissons mbunas sont donc particulièrement intéressants pour l’étude des spéciations comportementales (Greenberg et coll., 2016). Ils présentent des postures stéréotypées que ce soit pendant la parade nuptiale ou bien dans un contexte plus agressif. En plus de ces signaux visuels, M. zebra émet des sons dans différents contextes comme la parade nuptiale, la défense du territoire ou des interactions sociales agonistiques (luttes) entre les individus d’un même groupe (Simoes et coll. 2008, Amorim et coll. 2015).
L’ensemble de ces caractéristiques, associées à son élevage facile en captivité, font de M. zebra un modèle bien adapté aux études de laboratoire sur la communication intraspécifique.
Dans l’équipe de neuroéthologie sensorielle de l’université de Saint-Étienne, nous étudions le rôle de la communication multimodale (utilisant plusieurs canaux sensoriels) chez M. zebra, ainsi que la hiérarchisation de ces canaux dans un contexte de défense du territoire. Nous présentons ici des recherches menées pour répondre à trois interrogations :
- Les sons émis par les mâles en contexte de défense du territoire portent-ils une signature individuelle ?
- Quelle est l’importance des signaux visuels et acoustiques dans le comportement de défense du territoire ?
- La fréquence des sons émis est-elle importante pour la communication ? Si oui, quelle est l’importance relative du signal porté par la fréquence et des signaux visuels ?
Conditions d’hébergement au laboratoire
Les poissons présents au laboratoire proviennent le plus souvent de notre propre élevage mais peuvent également être commandés auprès de fournisseurs.
Les individus adultes mâles et femelles sont maintenus au laboratoire au sein de groupes communautaires mixtes, dans des aquariums de 300 litres, à l’intérieur d’une salle climatisée réservée à cet effet (Figure 8). Chaque bassin est équipé d’une pompe filtrante, d’un bulleur et d’un chauffage. Les conditions physicochimiques de l’eau et le cycle photopériodique sont contrôlés et maintenus constants (25 ± 2 °C, pH = 8, alternance de 12 h de « jour », 12 h de « nuit »). Pour le respect du bien-être des animaux et afin de recréer en partie leur milieu naturel, le milieu a été enrichi par l’ajout de sable sur le fond de l’aquarium, de plantes décoratives et d’abris formés de rochers et/ou de tuyaux PVC. Les poissons sont alimentés quotidiennement avec de la nourriture sous forme de granulés spécialisés pour les Cichlidés.
Les méthodes d’études
L’analyse du comportement : réalisation d’un éthogramme
Avant de décrire les processus de communication, il faut connaître et déterminer les séquences comportementales du modèle étudié dans un contexte donné. Concrètement, l’animal est observé dans son milieu avec ses congénères et les comportements exprimés dans les différents contextes (défense du territoire, parade nuptiale…) sont notés. Dans notre cas, les animaux ont été observés directement et filmés dans leur aquarium d’élevage et pendant les expérimentations, dans un contexte de défense du territoire. La description des comportements retenus, correspondant à ce que l’on appelle un éthogramme, est détaillée ci-après.
Les comportements agressifs sont observés en situation de défense du territoire lorsqu’un mâle s’approche du territoire d’un autre mâle.
- Les lateral displays : le poisson se place de façon perpendiculaire à son adversaire, présentant son flanc. Le corps est légèrement arqué et les nageoires impaires (dorsale, caudale, anale) sont déployées.
- Les quivers (tremblements) : Le poisson s’immobilise un bref instant avant de faire vibrer son corps. Ce comportement est souvent associé à une production de sons.
- Les charges/poursuites : afin de repousser un congénère qui s’approche de son territoire ou durant un combat, un poisson nage rapidement en direction de son adversaire. Il y a parfois contact entre la tête de l’attaquant et le flanc de sa cible. Souvent, le poisson cible rebrousse chemin, poursuivi sur une courte distance par le mâle territorial avant que ce dernier ne retourne dans son abri. Lors de l’établissement de la hiérarchie, les poursuites peuvent être beaucoup plus longues, et l’un des adversaires harcèle l’autre. Lors des expériences où une paroi transparente séparait les deux compartiments, les poissons heurtaient cette dernière en tentant de charger.
- Les morsures : suite à une charge, lors du contact physique, l’un des combattants peut tenter de mordre les flancs de son adversaire. Les deux poissons peuvent également se mordre mutuellement au niveau de leur bouche et l’un des protagonistes bloque la bouche de son adversaire dans la sienne (mouth locking) (Figure 9C). Durant les expériences, on assistait à des tentatives de morsures avec des poissons frottant leurs dents contre la paroi transparente.
- Les sons : ils sont produits lorsque deux individus sont proches l’un de l’autre. Ils consistent en une série de pulses successifs de basse fréquence. La durée des sons, le nombre de pulses et leur période sont variables.
En dehors de ces comportements agressifs, les poissons présentent également d’autres comportements :
- La maintenance ou digging : en devenant territoriaux, les mâles aménagent leur territoire autour d’un abri. En particulier, ils déplacent le substrat depuis cet abri vers la périphérie (Figures 9A et 9B) en collectant du sable dans leur cavité buccale pour le rejeter aux frontières de leur territoire.
- Les visites de l’abri : dans les aquariums communautaires ou expérimentaux, les individus disposaient de pots de briques en terre-cuite ou de tubes PVC créant des abris (Figure 9D). Les poissons, en particulier dominants, visitent ces abris régulièrement, les entretiennent en déplaçant du substrat et peuvent même rester à l’intérieur et n’en sortir que pour repousser un congénère qui s’approche.
- La nage haut/bas : ce comportement est typiquement observé dans les aquariums expérimentaux lorsque deux individus sont séparés par une paroi transparente. Les poissons vont alors essayer d’atteindre leur adversaire et se retrouvent face à la paroi.
A-B : Comportement de digging ou maintenance. Entre le temps t0 en A et t0 + 24 h en B, du sable a été déplacé par le poisson (a : abri, s : sable, h : hydrophone, HP : haut-parleur). C. Deux poissons réalisant un mouth locking pendant un combat. D. Poisson dans un abri.
Les protocoles expérimentaux
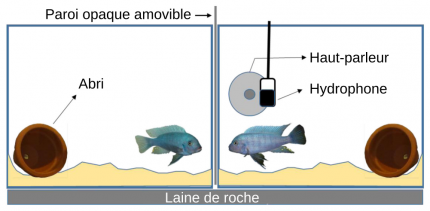
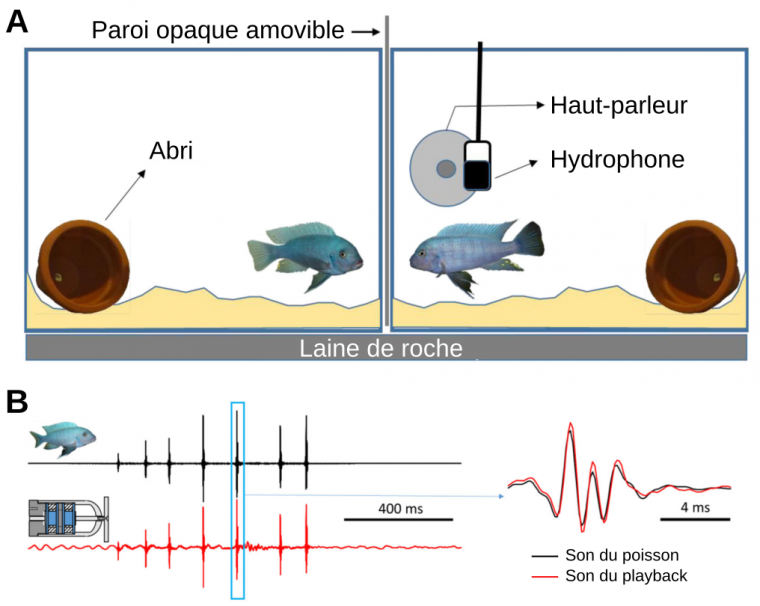
Les expériences décrites ici sont réalisées dans un contexte agonistique de défense du territoire. Pour ce faire, nous avons placé deux mâles dans deux aquariums entre lesquels se trouve une cloison opaque amovible. Chaque aquarium comprend un système de filtration, un abri, du sable sur le fond. L’aquarium du poisson testé est équipé d’un haut-parleur (pour diffuser des sons) et d’un hydrophone (pour enregistrer les sons émis). L’autre poisson sert de stimulus visuel (Figure 10). Les aquariums reposent sur de la laine de roche et l’ensemble du dispositif est placé dans des chambres acoustiques permettant de limiter les effets des vibrations extérieures.
Pour les trois expériences, les animaux sont placés dans leur aquarium respectif 24 h avant le début de l’expérience afin qu’ils s’approprient le territoire. Pendant les expérimentations, des signaux (stimuli) visuel et/ou acoustique sont envoyés et les réponses comportementales sont filmées puis analysées. Le stimulus visuel est réalisé en enlevant la paroi opaque amovible entre les deux poissons : les deux mâles se voient et peuvent interagir. Les poissons peuvent être de même taille ou de taille différente, en fonction de la question posée. Le stimulus acoustique est un playback diffusé par le biais du haut-parleur. Il est constitué par des sons de congénères enregistrés préalablement pendant des combats.
L’analyse acoustique
À partir des vidéos enregistrées lors des sessions expérimentales, un logiciel (par exemple Audacity, GoldWave, Praat…) permet d’extraire et d’isoler les sons en vue de leur analyse et de la réalisation d’une banque de sons qui servira pour l’envoi de playback (voir plus de détail dans Bertucci, 2011).
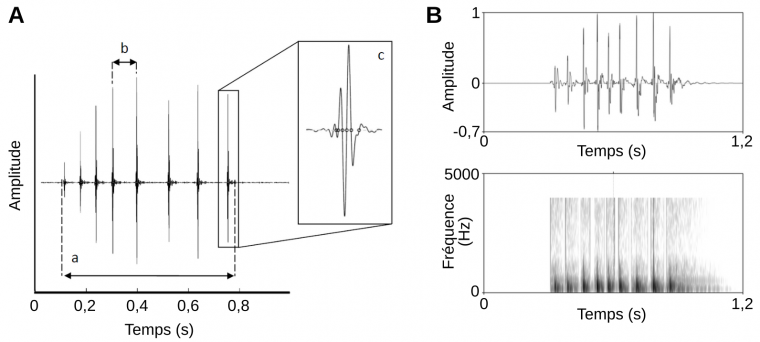
L’analyse des sons consiste à décrire la structure acoustique des sons émis (Figure 11). Plusieurs paramètres acoustiques sont étudiés dont les principaux :
- le nombre de pulses composant un son ;
- la durée totale du son, mesurée du début du premier pulse à la fin du dernier pulse ;
- la période des pulses : correspond à la durée moyenne de l’intervalle de temps entre les pics d’amplitude de deux pulses consécutifs ;
- la fréquence dominante du son.
A. Oscillogramme (amplitude du son en fonction du temps) sur lequel quelques variables mesurables sont présentées : (a) nombre d’impulsions (pulses) et durée du son, (b) période des pulses, (c) détail d’un pulse. B. Autre oscillogramme avec le spectrogramme (fréquence en fonction du temps) correspondant.
Crédits : A : Bertucci et coll., 2012, Journal of Fish Biology ; B : Marilyn Beauchaud
Résultats et discussion
Dans cette partie, les titres des différents paragraphes correspondent à une question biologique donnée. Trois expériences ont été réalisées pour répondre à ces questions qui s’articulent autour de la recherche d’une signature individuelle dans les sons émis et de l’estimation de l’importance relative des signaux visuel et acoustique au cours d’un combat. Les protocoles expérimentaux utilisés suivent le schéma général énoncé plus haut.
Les sons émis sont-ils porteurs d’une signature individuelle ?
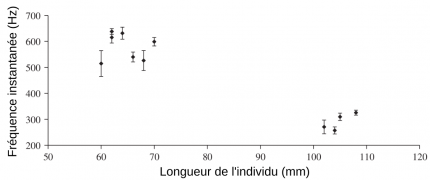
Les losanges indiquent les moyennes et les barres verticales les écarts-types.
Quand deux mâles de Maylandia zebra ne se voient pas (paroi opaque entre les deux aquariums), ils ne produisent pas de sons. Par contre, une fois la paroi opaque retirée, les mâles émettent des sons. Leur analyse ne permet pas de mettre en évidence une signature sonore qui serait propre à chaque individu. Par contre, il existe une corrélation négative entre la taille de l’individu et la fréquence du son émis : plus les individus sont grands, et plus ils émettent des sons de basse fréquence (Figure 12). Or, chez les poissons, la taille d’un individu est souvent liée à son statut social dans le groupe, les poissons dominants étant généralement de plus grande taille (Ladich, 1998). Au-delà de l’information sur la taille de l’individu, le message contenu dans le son d’un individu pourrait donc permettre à ses congénères d’avoir des informations sur sa position sociale dans le groupe. Cette information pourrait jouer un rôle au cours du choix du partenaire pendant la période de reproduction ou pourrait permettre l’évaluation d’un congénère avant d’engager un combat (Amorim et coll. 2019).
Comment interagissent les signaux visuel et acoustique au cours d’un combat ?
Les poissons de la famille des Cichlidés sont connus pour communiquer par le canal visuel. Les mâles M. zebra dominants possèdent un corps d’une couleur bleue intense strié de rayures noires bien visibles alors que les individus de rang inférieur portent une robe moins colorée et contrastée. Cette coloration peut être modifiée très rapidement pendant une interaction avec un autre mâle, leur coloration bleue devient plus pâle augmentant le contraste des rayures noires sur leur flan. Les postures, décrites précédemment, sont aussi des signaux forts au cours des interactions agonistiques. Par ailleurs, nous avons vu que des informations individuelles, comme la taille de l’émetteur, étaient transmises par le canal acoustique. Pendant un combat, les signaux visuels et acoustiques sont émis en même temps et, d’une manière générale, l’émission de sons est souvent associée à des comportements comme les quivers ou les lateral displays.
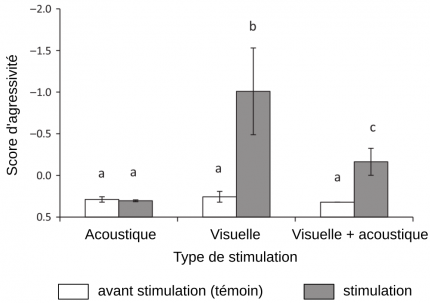
Des mâles de Maylandia zebra sont soumis à différents traitements : stimulation acoustique seule, stimulation visuelle seule ou stimulation acoustique et visuelle. L'observation du comportement des poissons en réponse à ces stimulus permet de leur attribuer un score d'agressivité, d'autant plus négatif que la réponse est agressive. Les différentes lettres indiquent les différences significatives.
Dans l’expérience suivante, nous avons voulu savoir comment les messages visuel et acoustique interagissent dans un contexte de défense du territoire. Pour ce faire, des stimuli visuel et acoustique ont été envoyés de façon séparée ou simultanée dans des expériences d’interactions entre deux mâles dominants. Un score d’agressivité est alors déterminé en comptabilisant le nombre de comportements agressifs (lateral displays, quivers, charges…) observés sur un temps donné. Plus le score est négatif et plus la réponse de l’individu est agressive. Les résultats montrent qu’à l’inverse du signal visuel seul, le signal acoustique seul ne provoque pas de réaction agressive. Par contre, l’association des deux canaux de communication diminue le niveau d’agressivité du combat (Figure 13). Ces résultats suggèrent que les signaux acoustiques émis pendant un combat complètent les signaux visuels et permettraient une modulation des comportements agonistiques des mâles en diminuant l’agressivité et évitant ainsi une escalade de violence (Bertucci 2010).
Quelle est l’importance du signal visuel par rapport au signal acoustique dans l’évaluation d’un congénère ?
Pour tester l’importance relative entre les modalités sensorielles visuelle et acoustique impliquées dans l’estimation de la taille d’un opposant, nous avons diffusé des sons qui ne correspondaient pas à la taille du stimulus visuel (opposant) au cours d’une interaction entre deux mâles dominants (Amorim et coll., 2019). Les protagonistes sont de la même taille (de 8,5 à 9,5 cm) seuls diffèrent les sons envoyés au poisson testé : des sons mimant un individu de plus petite (6,5 cm) ou de plus grande taille (10,5 cm).
L’expérience se déroule en trois étapes, de cinq minutes chacune :
- préplayback : stimulus visuel uniquement ;
- playback : stimulus visuel et acoustique. Différents stimulus acoustiques sont utilisés :
- sons de haute fréquence (environ 600 Hz), normalement émis par des poissons de petite taille (6,5 cm) ;
- sons de basse fréquence (environ 300 Hz), normalement émis par des poissons de grande taille (10,5 cm) ;
- bruit blanc ;
- silence.
- postplayback : stimulus visuel uniquement. Cette condition permet de voir si les sons peuvent avoir un effet qui ne serait visible qu’à long terme, après l’arrêt de leur émission.
A. Deux mâles de M. zebra de même taille ont été placés dans chaque aquarium 24 h avant les essais. Les essais démarrent en supprimant la paroi opaque pour permettre des interactions agonistiques et consistent en trois périodes de 5 min : préplayback, playback (présentation des stimuli acoustiques) et postplayblack. Pendant la période de playback, 10 stimuli acoustiques (sons agonistes ou stimuli de contrôle) ont été envoyés lorsque l’adversaire a interagi de manière agoniste avec le sujet. B. Oscillogrammes d’un son agonistique (à gauche) produit par un mâle (en noir) ou par le haut-parleur (en rouge). À droite : détail d’un pulse.
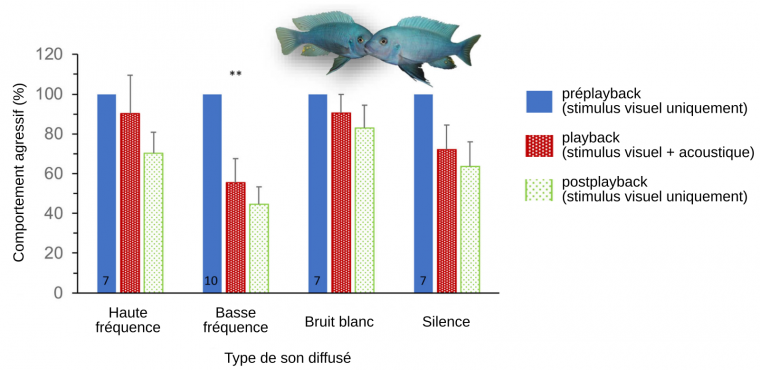
La comparaison entre la condition playback et préplayback permet de voir si les signaux acoustiques perçus modulent ou non le comportement d’agressivité face à un signal visuel donné. Les résultats montrent que seuls les sons de basse fréquence ont un effet significatif sur la diminution de l’agressivité (Figure 15). Autrement dit, quand la fréquence du son indique un opposant de grande taille le signal acoustique prévaut sur le signal visuel Ces résultats suggèrent que M. zebra est capable d’évaluer les informations provenant d’un signal visuel et/ou acoustique et de s’en servir pour prendre une décision.
Réaction agressive des poissons mâles face à des signaux acoustique et visuel incongrus de l’adversaire. Chaque poisson testé est, durant les trois périodes de l'expérience (préplayback, playback et postplayback) en contact visuel avec un autre poisson mâle. Pendant le playback, les poissons testés sont soumis à des signaux acoustiques de différentes natures : sons de haute fréquence (mimant un adversaire de petite taille), sons de basse fréquence (mimant un adversaire de grande taille), bruit blanc et silence. La période préplayback sert de référence (100 %) pour la mesure de la variation d'agressivité. Les résultats sont donnés sous forme de valeur moyenne associés à l'erreur type de la moyenne ; *** P < 0,001 tests DSH de Tukey.
Conclusion et perspectives
Les signaux acoustiques de M. zebra portent des informations sur la taille des individus. Comme chez d’autres espèces de poissons, par exemple les blennies, les poissons les plus gros produisent des sons de fréquence plus basse (De Jong et coll., 2007). Toutefois, à l’heure actuelle, il est difficile de savoir si d’autres informations sont codées dans le signal acoustique chez M. zebra. Si la signature acoustique individuelle de M. zebra semble être peu développée, peut-être existe-t-il une signature de statut social liée à la taille de l’individu. Des études chez le tilapia du Mozambique montrent que les sons produits peuvent renseigner sur l’expérience sociale des individus : les sons de vainqueurs ont une durée de pulses plus longue et également une fréquence dominante plus basse (Amorim et Almada, 2005). Chez le gourami grogneur, les sons des vainqueurs de combats ont une intensité plus élevée et une fréquence dominante plus faible que les sons de perdants (Ladich, 1998). Pour compléter nos données sur le codage de l’information, des expérimentations sur le rôle de la communication acoustique au cours de la parade nuptiale et de la reconnaissance mâle/femelle sont en cours de réalisation dans l’équipe de neuroéthologie sensorielle de l'université de Saint-Étienne (ENES).
Les signaux acoustiques jouent un rôle important dans l’évaluation d’un congénère pendant un combat puisqu’ils modulent le comportement agressif des mâles en association avec des stimuli visuels. Ces signaux permettraient d’éviter une escalade dans les agressions et un possible combat physique coûteux en temps et en énergie. Cette hypothèse semble renforcée par les résultats obtenus dans l’expérience visant à déterminer l’importance relative des signaux visuels et acoustiques dans l’évaluation d’un congénère. Cette dernière expérience montre aussi comment les signaux visuels et acoustiques peuvent être interprétés pour prendre des décisions et pour évaluer un danger potentiel.
Chez les poissons, il existe aussi une communication chimique par le biais de molécules qui peuvent diffuser sur de longues distances et persister longtemps dans l’environnement. Des expériences préliminaires, réalisées à l'ENES, montrent que les mâles M. zebra urinent pour marquer leur territoire. Toujours chez cette espèce, Escobar-Camacho & Carleton (2015) ont observé l’émission d’urine par les mâles au cours de la parade nuptiale. Nous avons réalisé des expériences de playback chimique fondées sur les mêmes principes que celles décrites pour les signaux acoustiques et visuels. Les premiers résultats obtenus montrent une interaction et une hiérarchisation complexe des canaux visuel, acoustique et chimique (Chabrolles et coll., 2017).
Références
- Amorim, M.C.P. & Almada, V.C. (2005). The outcome of male-male encounters affects subsequent sound production during courtship in the cichlid fish Oreochromis mossambicus. Animal Behaviour, 69, 595-601.
- Amorim M.C.P., Vasconcelos R.O., Fonseca P.J. (2015) Fish Sounds and Mate Choice. In : Ladich F. (eds) Sound Communication in Fishes. Animal Signals and Communication, vol 4. Springer, Vienna. https://doi.org/10.1007/978-3-7091-1846-7_1
- Amorim, M. C., Fonseca, P. J., Mathevon, N. & Beauchaud, M.(2019) Assessment of fighting ability in the vocal cichlid Metriaclima zebra in face of incongruent audiovisual information. Biology open, vol. 8, no 12.
- Bertucci F. (2011) Communication acoustique chez un poisson Cichlidé : Analyse expérimentale du rôle et de la structure des signaux. Thèse de Doctorat, Université Jean Monnet Saint-Étienne, 154pp.1
- Bertucci, F., Attia, J., Beauchaud, M. & Mathevon, N. (2012). Sounds produced by the cichlid fish Metriaclima zebra allow reliable estimation of size and provide information on individual identity. Journal of Fish Biology, 80(4), 752-766.
- Bertucci, F., Beauchaud, M., Attia, J., & Mathevon, N. (2010). Sounds modulate males’ aggressiveness in a cichlid fish. Ethology, 116(12), 1179-1188.
- Chabrolles, L., Ammar, I. B., Fernandez, M. S. A., Boyer, N., Attia, J., Fonseca, P. J., Amorim, M.C, Beauchaud, M. (2017). Appraisal of unimodal cues during agonistic interactions in Maylandia zebra. PeerJ, 5, e3643. https://doi.org/10.7717/peerj.3643
- De Jong, K., Bouton, N. & Slabbekoorn, H. (2007). Azorean rock-pool blennies produce size dependent calls in a courtship context. Animal Behaviour, 74, 1285-1292.
- Escobar-Camacho, D., & Carleton, K. L. (2015). Sensory modalities in cichlid fish behavior. 102 Current Opinion in Behavioral Sciences, 6, 115–124. https://doi.org/10.1016/j.cobeha.2015.11.002
- Greenberg, J., Jordan, R.C., and Sorensen, A.E. (2016). The effect of territory quality on female preference in Metriaclima zebra. African Journal of Ecology 54, 162–166.
- Hanke, W., Brüker, C. & Bleckmann, H. (2000). The ageing of the low-frequency water disturbances caused by swimming goldfish and its possible relevance to prey detection. Journal of Experimental Biology, 203, 1193-1200.
- Janssen, J., & Strickler, J. R. (2006). Hydromechanical Communication via the Lateral Line : Copepodology for the Ichthyologist. Communication in Fishes, 1, 207-222.
- Kasumyan, A. O. Acoustic signaling in fish. Journal of Ichthyology, 2009, vol. 49, no 11, p. 963-1020.
- Konings, A. (2007). Malawi cichlids in their natural habitat, 4th edn. El Paso, Texas : Cichlid Press.
- Ladich F (2016) Peripheral Hearing Structures in Fishes : Diversity and Sensitivity of Catfishes and Cichlids. Adv Exp Med Biol. 2016 ; 877:321-40. doi : 10.1007/978-3-319-21059-9_15. PMID : 26515321
- Ladich, F. (1998). Sound characteristics and outcome of contests in male croaking gouramis (Teleostei). Ethology, 104(6), 517-529
- Parmentier, E. & Fine, M. (2016) Springer International Publishing Switzerland 19 R.A. Suthers et al. (eds.), Vertebrate Sound Production and Acoustic Communication, Springer Handbook of Auditory Research 53, DOI 10.1007/978-3-319-27721-9_2
- Parmentier, E., Tock, J., Falguière, J. C., & Beauchaud, M. (2014). Sound production in Sciaenops ocellatus : preliminary study for the development of acoustic cues in aquaculture. Aquaculture, 432, 204-211.
- Partridge, B.L. (1982) Structure and function of fish schools. Scientific American, 245, 114-123.
- Simões, J.M., Duarte, I.G., Fonseca, P.J., Turner, G.F. & Amorim, M.C. (2008). Courtship and agonistic sounds by the cichlid fish Pseudotropheus zebra. Journal of the Acoustical Society of America, 124, 1332-1338.
- Tanzarella, S. (2006) Perception et communication chez les animaux, de Boeck.
- Tock (2013) Étude du mécanisme de production de son chez Scianops ocellatus. Mémoire de Master 1. Université de Liège. Belgique. 58p.
- Vignal, C., Mathevon, N., & Mottin, S. (2008). Mate recognition by female zebra finch : analysis of individuality in male call and first investigations on female decoding process. Behavioural processes, 77(2), 191-198.
- Wahlberg, M. & Westerberg, H. Sounds produced by herring () bubble release. Aquatic Living Resources, 2003, vol. 16, no 3, p. 271-275.