Est-il possible d'identifier des gènes qui influencent le comportement animal ? Cet article présente deux cas dans lesquels une relation directe entre gène et comportement sexuel a été mise en évidence.
Introduction
Est-il possible d’identifier des gènes qui influencent le comportement animal ?
Le doute est légitime : les gènes sont si nombreux à interagir entre eux que l’étude d’un seul gène pourrait bien ne rien apprendre de significatif sur un comportement. Ils interagissent avec leur environnement, et le débat nature/culture pourraient remplir des encyclopédies entières.
Pourtant, un élément de réponse a été apporté à cette question par l’étude de certains comportements innés peu influençables par l’environnement, et par les techniques actuelles de séquençage des gènes qui offrent tous les moyens d’en comprendre l’expression.
Il sera donc ici question de transcription de gènes et de sa mise en relation avec deux comportements innés, l’un chez les campagnols, l’autre chez la drosophile.
Le comportement social et parental inné des campagnols
Les campagnols, petits rongeurs ressemblant aux hamsters, sont des animaux de choix pour étudier les comportements sociaux et parentaux, car ils offrent deux modèles de comportements. Les campagnols des prairies (Microtus ochrogaster) comme les campagnols sylvestres (Microtus pinetorum) sont des espèces grégaires et monogames : ils forment des couples stables à l’intérieur desquels mâles et femelles élèvent ensemble leur progéniture. Ceux des montagnes (Microtus montanus) comme ceux des prés (Microtus pennsylvanicus) sont des espèces relativement asociales et polygames. Les femelles s’occupent seules des petits. D’où viennent ces différences de comportement entre espèces si voisines ?
Le rôle de la vasopressine
La vasopressine (également appelée arginine vasopressine, AVP, et hormone antidiurétique, ADH) a été associée à un grand nombre de comportements chez de nombreuses espèces animales : vie en groupe, comportement paternel, agressivité, anxiété…
C’est une hormone fabriquée dans l’hypothalamus qui, relâchée dans le sang par l’intermédiaire de la neurohypophyse, joue un rôle antidiurétique sur sa cible rénale. Mais c’est aussi un neuromodulateur fabriqué dans d’autres régions cérébrales que l’hypothalamus, et qui se lie à différentes zones du cerveau. C’est cette deuxième fonction qui a été étudiée chez les campagnols.
Un lot d’individus de l’espèce monogame Microtus ochrogaster, le campagnols des prairies, et un autre lot de l’espèce polygame Microtus pennsylvanicus, le campagnol des prés, ont été sacrifiés. Leurs cerveaux ont été découpés en lamelles ultra minces, incubés avec de la vasopressine radioactive et soumis à autoradiographie, ce qui à permis de repérer la distribution du récepteur à la vasopressine de type V1a (V1aR).
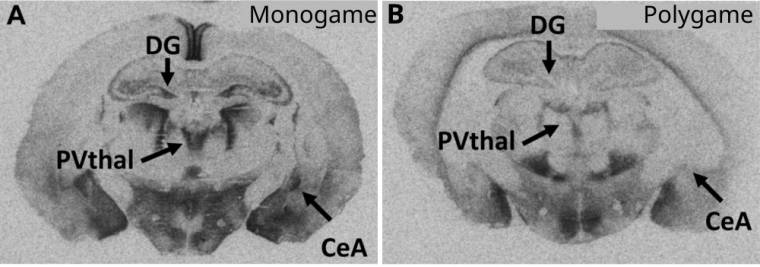
On a alors découvert que la distribution de ce récepteur cérébral est différente selon l’espèce : chez l’espèce monogame, sa densité est toujours bien plus forte que chez l’espèce polygame à différents endroits du cerveau (Figure 1).
Des coupes de cerveau sont incubées avec de la vasopressine marquée à l'iode radioactif. Une autoradiographie permet ensuite de révéler la localisation des récepteurs à la vasopressine, davantage exprimés chez les campagnols monogames que chez les polygames. DG : gyrus denté ; PVThal : noyau paraventriculaire du thalamus ; CeA : amygdale centrale.
Le gène du récepteur V1a à la vasopressine
Les chercheurs sont remontés au gène codant ce récepteur, l’ont cloné et séquencé. Il est apparu que la séquence diffère entre l’espèce monogame de prairie et l’espèce polygame, mais pas dans la partie codante du gène. Cette différence se situe au niveau du promoteur proximal qui gouverne sa transcription (référence 1).
Une séquence répétée, dite « microsatellite », située à – 760 nucléotides du site de démarrage de la transcription, y est toujours plus longue chez l’espèce monogame que chez la polygame. Au sein de chaque espèce, des différences interindividuelles existent dans le nombre de lettres répétées. Il est à noter que le promoteur proximal des deux espèces ne contient pas de « boîte TATA » ou de « boîte CAAT » et, autant qu’on le sache, il n’existe pas de promoteur distal de type « enhancer » (amplificateur).
Jusque-là, il ne s’agit que d’une corrélation entre longueur du microsatellite, densité du récepteur V1a à la vasopressine et comportement. Mais peut-on apporter la preuve qu’il existe un lien de causalité entre différence de longueur du microsatellite, différence de densité de ce récepteur dans le pallidum ventral et différences des comportements ?
Des campagnols polygames deviennent monogames
Cette démonstration a été brillamment apportée en juin 2004 par Miranda Lim et ses collègues de l’université d’Emory à Atlanta (référence 2) : ils ont injecté dans le pallidum ventral des campagnols polygames des prés (Microtus pennsylvanicus) des virus inoffensifs porteurs du gène codant récepteur V1a à la vasopressine propre aux campagnols monogames de prairie (Microtus ochrogaster).
Dans leur cage, les campagnols des prés précédemment volages se sont mis à préférer leur partenaire du moment aux nouvelles femelles qui y étaient introduites. Bien entendu, pour garantir l’objectivité nécessaire, les observateurs chargés d’établir l’intérêt ou non manifesté par le mâle ne connaissaient pas l’identité des différentes actrices. Le constat fut également établi que la densité des récepteurs V1a dans le pallidum ventral des campagnols injectés était devenue très importante.
Conclusion sur les campagnols
Il était ainsi montré qu’un seul gène peut influencer un comportement complexe. Qui plus est, la différence comportementale mise en évidence est le résultat d’une différence génétique située dans la partie non codante du gène, au niveau de son promoteur proximal et des séquences répétées qu’il contient, séquences dénommées un peu vite autrefois « ADN poubelle » ou « junk DNA » par simple ignorance de leurs fonctions ; double enseignement donc, apporté par les petits campagnols.
La parade sexuelle de la drosophile
La mouche du vinaigre (Drosophila melanogaster) est un autre animal de choix pour étudier la base génétique des comportements innés, en l’occurrence ici la parade sexuelle du mâle et de la femelle, avec l’avantage, cette fois-ci, de disposer d’un témoin à l’intérieur même de l’espèce.
La parade des mâles et des femelles
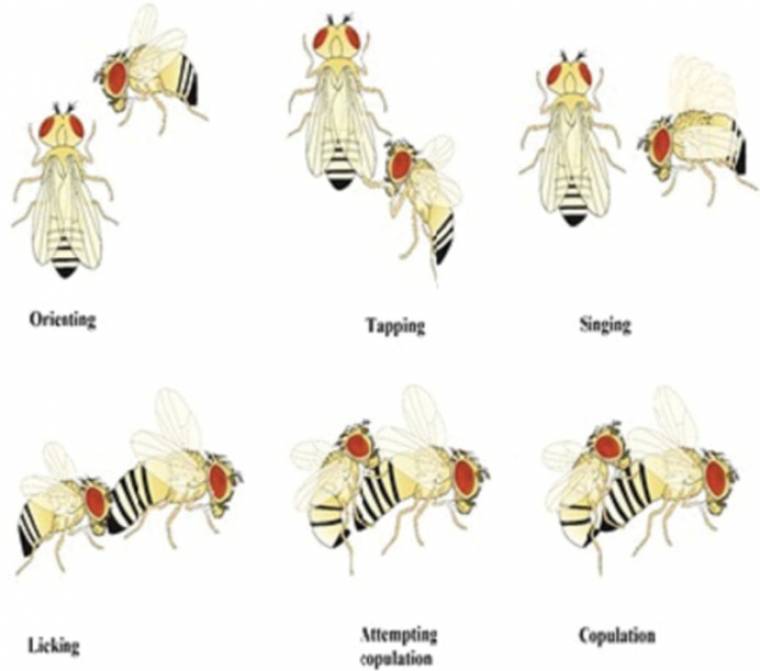
Elle est innée, élaborée et stéréotypée (Figure 2). Le mâle procède en six étapes :
- il s’oriente vers la femelle qu’il vient de repérer ;
- il la suit et la tapote de ses pattes antérieures ;
- il lui chante une sérénade en faisant vibrer une aile déployée à la verticale de son corps ;
- il lui lèche les plaques génitales ;
- il tente une copulation en incurvant son abdomen ;
- enfin il copule… si la femelle a été suffisamment stimulée par la parade.
Un mâle inexpérimenté courtise souvent d’autres mâles au début de sa vie d’adulte.
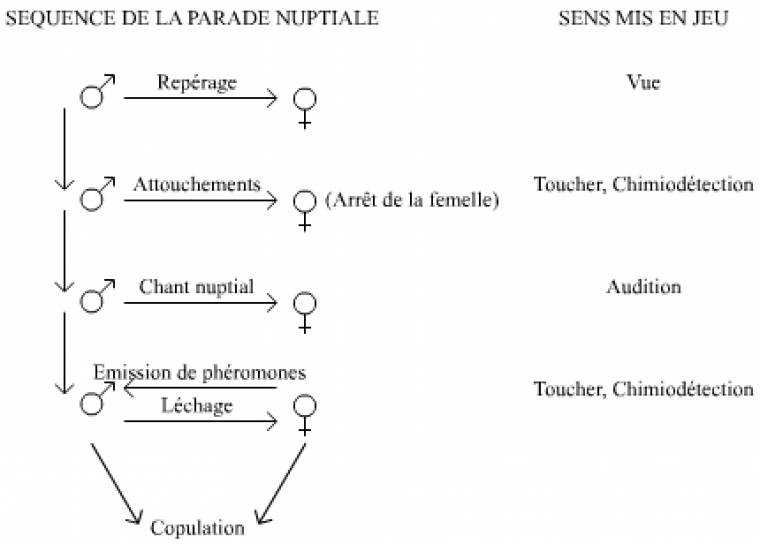
De nombreux sens interviennent dans le déroulement de ce comportement, qui sont autant de cibles potentielles de mutations perturbatrices (Figure 3).
Quant à la femelle :
- elle émet des substances odorantes aphrodisiaques (des phéromones) lorsqu’elle est réceptive ;
- elle baguenaude puis ralentit son activité locomotrice pour favoriser l’accouplement ;
- elle manipule et écarte ses plaques génitales au moment de l’accouplement.
Bien sûr, il faut mobiliser un grand nombre d’organes (organes olfactifs, organes auditifs, yeux, nerfs, muscles…) et mettre en jeu en amont énormément de gènes pour aboutir à cette parade, mais l’un d’entre eux, le gène fruitless (ou gène fru), joue un rôle maître dans ce comportement.
Les mutations du gène fru
Le gène fru est un gène autosomal découvert dans les années soixante par les effets que ses mutations peuvent provoquer sur la parade sexuelle des mâles :
- une cour qui continue d’être adressée indistinctement aux mâles et aux femelles ;
- un chant peu audible et déformé émis par une aile mal déployée ;
- une inaptitude à copuler ;
- une tendance à tourner en rond en se stimulant les uns les autres, à la queue leu leu, lorsqu’ils se trouvent ensemble dans une même boîte.
Comme on s’en doute, ces mâles n’ont rien de prolifique d’où le nom de fruitless (sans descendance) donné à ce gène, puisqu’un gène est souvent nommé d’après l’effet que produit sa mutation. Signalons que ce gène intervient dans d’autres mécanismes non liés à la sexualité (développement des disques imaginaux par exemple).
Les transcrits du gène fru, les protéines FruM et FruF
Ce gène a été cloné et séquencé : il est transcrit à partir de promoteurs multiples et dispose d’un vaste répertoire de sites d’épissages alternatifs.
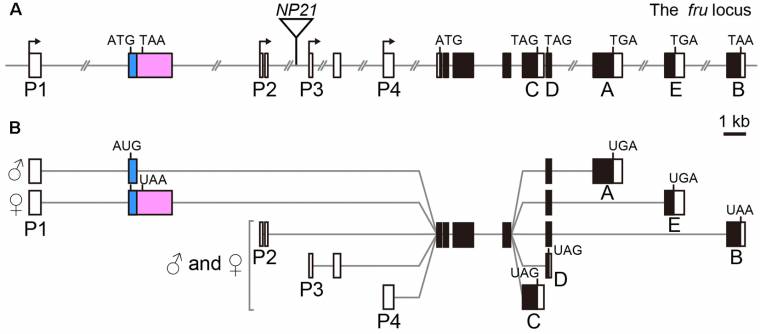
Les ARN prémessagers (ARNpm) spécifiques de la parade des mâles et des femelles sont formés à partir du promoteur le plus distal, le promoteur P1. Celui des mâles est ensuite le seul à subir un épissage partiel de son premier exon (Figure 4).
A: Structure du gène fru, comportant quatre promoteurs (P1–P4). Les exons sont représentés par des rectangles (noircis au niveau des séquences codantes), les introns par des traits. L’exon subissant un épissage alternatif dépendant du sexe est représenté en rose.
B: Différents transcrits obtenus à partir du gène fru. Un seul seul exon subit un épissage alternatif dépendants du sexe : l'exon S qui n'est transcrit qu'à partir du promoteur proximal P1.
Les autres produits de cet épissage alternatif sont retrouvés aussi bien chez les mâles que chez les femelles.
De ce fait, les protéines Fru finalement formées diffèrent par l’une de leurs extrémités, l’extrémité N terminale, donnant FruM chez les mâles et FruF chez les femelles. Elles contiennent chacune des portions en doigt de zinc typiques de nombreux facteurs de trancription. Elles s’expriment dans environ 2 % des neurones cérébraux.
La démonstration du rôle de l’épissage partiel alternatif de l’ARNpm fru
L’épissage alternatif du premier exon de l’ARNpm fru est-il à l’origine des différences de parade sexuelle entre mâles et femelles ? Pour le savoir, l’équipe de Barry Dickson à l’Institut de biotechnologie moléculaire de Vienne (référence 3) a construit des femelles chez lesquelles cet exon est partiellement ôté de leur ARNm fru comme chez les mâles, et des mâles chez lesquels, au contraire, il ne l’est jamais. Les femelles ainsi modifiées (c’est-à-dire « masculinisées » par la perte partielle d’un exon en amont de leur ARNm fru) s’orientent alors majoritairement vers les femelles ordinaires : elles les tapotent, leur chantent la sérénade, enroulent leur abdomen dans une manœuvre précopulatoire et s’arrêtent là… faute de pièces génitales adéquates. Un comportement de mâle presque complet dans un corps de femelle donc ! À l’inverse, les mâles chez lesquels l’exon n’est plus excisé ne se dirigent plus vers les femelles. Ils ne sont pas paralysés pour autant, puisqu’ils marchent, volent et se toilettent comme à l’ordinaire. Une absence de comportement mâle dans un corps de mâle donc !
Conclusion sur la drosophile
La preuve est donc apportée, chez la drosophile, que le transcrit d’un seul gène, selon qu’il est épissé suivant le mode mâle ou femelle, est nécessaire et suffisant pour gouverner à la fois une orientation sexuelle et la conduite presque entière d’une parade sexuelle élaborée et innée.
L’équipe de Barry Dickson est allée plus loin dans son travail en montrant que les protéines FruM sont présentes dans un circuit neuronal, comprenant des neurones olfactifs, qui jouent nécessairement un rôle dans la détection de phéromones sexuelles.
Il devient donc possible de commencer à comprendre comment un comportement inné et complexe est inscrit dans le système nerveux.
Conclusion générale
Chez les campagnols et la drosophile, deux comportements innés changent du tout au tout lorsqu’un seul de leur gène est modifié.
Les campagnols des prés polygames deviennent monogames quand on leur apporte la version du gène V1aR des campagols monogames. De leur côté, les drosophiles mâles et femelles adoptent la parade sexuelle de l’autre sexe quand on échange le mode d’épissage, dépendant du sexe, du premier exon de l’ARN prémessager de leur gène fru.
Comme est lointaine l’idée que l’étude d’un seul gène n’apporterait rien de significatif à l’étude d’un comportement. Et comme ces gènes font penser aux gènes du développement qui déclenchent le développement de structures anatomiques : yeux, membres, axe antéro-postérieur, axe dorso-ventral… Des gènes maîtres, des gènes interrupteurs, s’avèrent jouer également un rôle dans les comportements.
Vient alors à l’esprit la question suivante : quid de l’espèce humaine ? Si les homologues de fru n’ont pas été trouvés chez les mammifères, ceux de V1aR sont bien présents chez l’Homme. Ces homologues V1aR jouent-ils un rôle dans un comportement pathologique comme l’autisme, qui peut conduire à une anxiété intense et à un repliement prononcé sur soi ? Si la réponse n’est pas encore trouvée, l’équipe de Barry Dickson engage cette enquête et, sans les campagnols, la question n’aurait même pas pu être posée.
Bibliographie
- Hammock E.A.D. et Young L.J. (2002) « Variation in the vasopressin V1a receptor promoter and expression : implications for inter – and intraspecific variation in social behaviour. » Eur. J. Neurosci. 16(3) :399-402.
- Lim M.M., Wang Z., Olazabal D.E., Ren X., Terwilliger E.F. et Young L.J. (2004) « Enhanced partner preference in a promiscuous species by manipulating the expression of a single gene. » Nature 429(6993) :754-757.
- Demir E. et Dickson B.J. (2005) « fruitless splicing specifies male courtship behavior in Drosophila » Cell 121(5) :785-794.
- (2005) « Genes Exert Powerful Effect On Sexual Behavior » ScienceDaily.
- Stockinger P., Kvitsiani D., Rotkopf S., Tirian L. et Dickson B.J. (2005) « Neural circuitry that governs Drosophila male courtship » Science 121(5) :795-807.
Sur le même sujet
Pour la Science N°545, du 14 février 2023, « Campagnols : l’amour est dans le pré. », de Dev Manoli, Steve Phelps et Zoe Donaldson.
Les figures de cet article, publié en février 2006, ont été remplacées en mai 2026 par de nouvelles figures présentant des informations similaires, et ce afin de respecter le droit d’auteur.