Cet article présente les connaissances actuelles relatives à la réponse des végétaux au stimulus gravitationnel. Il s'appuie à la fois sur des expériences anciennes mais aussi de plus récentes, notamment obtenues dans l'espace, en apesanteur. Il précise le rôle de l'hormone végétale auxine dans la croissance asymétrique des racines et des tiges d'une plante soumise à une accélération.
Introduction
La gravité terrestre est un facteur constant de notre environnement. La force qui en résulte représente potentiellement un stimulus, appelé stimulus gravitropique, auquel les organismes peuvent répondre. En particulier, la croissance des végétaux peut être modulée par ce stimulus : on parlera alors de gravitropisme. Dans ce cas, l’influence d’un facteur de l’environnement, la gravité, modifie l’établissement du phénotype au travers de différents mécanismes cellulaires.
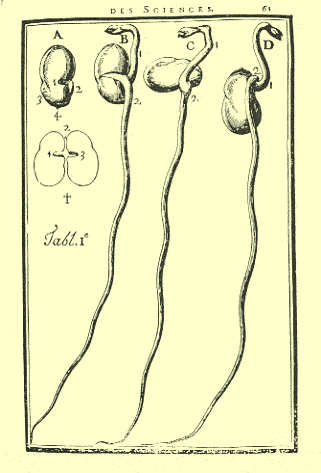
Figure extraite de l’article de D. Dodart, Sur l’affectation de la perpendiculaire, remarquable dans toutes les tiges, dans plusieurs racines, et autant qu’il est possible dans toutes les branches des plantes, Académie royale des sciences, 1703.
Mise en évidence expérimentale
Dès le début du XVIIIe siècle, Dodart et Astruc remarquent l’orientation verticale de bon nombre d’organes végétaux, et émettent l’hypothèse d’une relation avec la gravité. En effet, lorsqu’une racine, par exemple, croit initialement dans la direction du champ de gravité, puis est placée ensuite perpendiculairement à celle-ci, on observe au bout d’une vingtaine de minutes l’apparition d’une courbure qui tend à ramener la pointe de la racine dans la direction du champ de gravité (voir l'article Gravitropisme : réalisation d’expériences simples chez les végétaux).
À gauche : racine de lentille après 27 h de germination à la verticale
En haut, à droite : la racine est placée perpendiculairement au champ de gravité, g
En bas, à droite : courbure observée après 2 h
Ce n’est cependant qu’un siècle plus tard que la relation causale entre gravité et orientation des organes végétaux a été montrée expérimentalement.
Cette mise en évidence a été réalisée lors de l’expérience de Knight (1806). Celui-ci, en plaçant de jeunes plantules sur un tambour tournant autour d’un axe vertical, a observé que les tiges se courbaient en se rapprochant de l’axe de rotation du tambour, tandis qu’au contraire les racines se courbaient en s’éloignant de cet axe.
Dans ce dispositif expérimental, la rotation du tambour crée une accélération centrifuge (vecteur C), dont les propriétés physiques sont tout à fait semblables à celle de la gravité (vecteur G), si ce n’est que son orientation diffère. L’orientation observée pour les tiges et les racines des plantes correspond donc bien à une réponse à un facteur environnemental qui est le champ de gravité en milieu naturel, ou une accélération combinant accélération centrifuge et gravité (vecteur R) artificiellement créée dans l’expérience de Knight.
À la fin du XIXe siècle, Franck montre le premier que la réponse gravitropique est liée à la croissance des organes. En effet la courbure observée dans l’expérience de Knight, ou lorsqu’une racine ou une tige est placée à l’horizontale, correspond à une augmentation de la vitesse d’élongation au niveau de la zone de croissance, du côté extérieur à la courbure, tandis qu’au contraire la vitesse d’élongation est ralentie du côté intérieur à la courbure. Il introduit alors le terme de « géotropisme » qui a depuis été remplacé par celui de « gravitropisme ».
La vitesse d’élongation de la zone de croissance va varier selon sa position dans la racine (vers le haut ou vers le bas selon l’axe de la gravité), entraînant une courbure de l’organe.
Les racines s’orientent dans le sens du champ de gravité, c’est-à-dire « pointe vers le bas ». Il s’agit donc d’un gravitropisme positif, tandis qu’au contraire les coléoptiles et les tiges s’orientent dans le sens opposé au champ de gravité : il s’agit alors d’un gravitropisme négatif.
Depuis les travaux de Knight, des études ont permis de préciser les mécanismes mis en jeu dans la réaction gravitropique, même si des incertitudes demeurent encore à l’heure actuelle.
Enfin, récemment, la conquête spatiale a permis de réaliser des expériences en condition d’apesanteur (microgravité). Les résultats obtenus ont alors permis, entre autres, de confirmer le rôle important de la gravité sur la morphogenèse chez les végétaux.
En haut à gauche : Lentilles après 25 h de germination en gravité artificielle (mission spatiale). La force de gravitation, notée g sur la photo, est recréée grâce à une centrifugeuse. Les racines sont orientées dans la direction de la force de gravitation
En haut à droite : Lentilles après 4 h de germination supplémentaire en gravité artificielle. Les racines sont toujours orientées selon la direction de la force de gravitation. Les quelques déviations observées par rapport à cette direction sont dues aux mouvements de circumnutation (voir dossier BMédia sur la circumnutation). c : cotylédon, r : racine, s : support humide
En bas à gauche : Lentilles après 25 h de germination en microgravité (mission spatiale). Les racines ne s’orientent pas selon une direction particulière.
En bas à droite : Lentilles après 4 h de germination supplémentaire en microgravité. On remarque notamment que les racines des lentilles dont les cotylédons sont marqués par une étoile se sont totalement réorientées au cours de ces quatre heures.
Perception du stimulus
L’existence d’une réponse gravitropique chez les végétaux, qui correspond à une croissance dirigée de certains organes (tige, racine) selon le sens de la force de gravitation, suppose qu’il existe un ou des systèmes pouvant percevoir le stimulus gravitropique au sein de la plante. Nous considérerons plus particulièrement dans la suite de l’exposé le cas des racines.
Localisation des récepteurs du stimulus gravitropique dans la racine
C’est Darwin (1881) qui le premier a montré où sont localisés les récepteurs du stimulus gravitropique dans les racines des plantes.
Il réalise une expérience chez le maïs (Zea maïs), plante dont la coiffe racinaire se détache du reste de la racine sans entraîner de lésion des tissus du corps racinaire.
-
Chez une jeune racine primaire de maïs, placée à l’horizontale, on voit rapidement apparaître une courbure tendant à ramener la pointe racinaire dans l’axe vertical.
-
Au contraire, lorsque la coiffe a été supprimée, il n’y a aucune courbure alors même que la racine est placée à l’horizontale : la réponse gravitropique a disparu. Si on laisse la racine dans cette position pendant 18 à 24 h, la coiffe racinaire se reconstitue, et dès que la coiffe est reconstituée, on observe à nouveau une réaction de courbure.
Présence de cellules spécialisées dans la coiffe
Il apparaît donc que l’un des éléments contenus dans la coiffe racinaire intervient dans le gravitropisme. La force due à la gravité est susceptible de déformer ou de déplacer tous les éléments possédant une masse. Donc un dispositif biologique susceptible de percevoir ce stimulus devrait obligatoirement contenir un ou plusieurs éléments pouvant se déformer ou se déplacer et agir ainsi sur un récepteur cellulaire.
Des études cytologiques on permit de montrer que la coiffe racinaire était composée de différentes zones : une zone centrale, la columelle, entourée de cellules périphériques.
À gauche : Section longitudinale axiale dans une pointe racinaire de lentille (Lens culinaris). Coloration au bleu de toluidine.
À droite : Localisation de la columelle (C) contenant les statocytes et de la partie latérale de la coiffe (plc).
Les cellules de la columelle (statocytes) sont fortement différenciées. Les statocytes sont des cellules polarisées : si l’on considère une racine dont l’axe est orienté selon la direction de la gravité, le noyau est situé dans la moitié supérieure de la cellule, tandis que le réticulum endoplasmique se trouve au pôle opposé de la cellule. Ces cellules sont dépourvues de vacuole centrale. Elles contiennent par contre des amyloplastes volumineux, dont la densité est plus élevée que celle du cytoplasme. Dans une racine verticale, les amyloplastes sédimentent du côté opposé au noyau.
Micrographies de Lens culinaris, microscopie électronique.
À gauche, racine en position verticale : les amyloplastes ont sédimenté « en bas » de la cellule, sur le côté opposé au noyau.
a : amylopastes, N : noyau, mi : mitochondries, er : réticulum endoplasmique, g : direction de la gravité.
À droite, racine en position horizontale : les amyloplastes ont sédimenté « en bas » de la cellule, contre la longue paroi.
Cellules spécialisées permettant la perception de la gravité
Les amyloplastes volumineux contenus dans les statocytes pourraient donc, par leurs déplacements et leurs changements de position liés à la gravité, représenter la première étape du système de perception de la gravité chez les plantes. En relation avec ces propriétés, ils sont aussi appelés statolithes.
Plusieurs résultats expérimentaux appuient cette hypothèse :
-
L’ablation sélective, au laser, des statocytes, supprime la réponse gravitropique sans modifier la croissance, tandis que l’ablation des cellules latérales de la coiffe est sans effet sur le gravitropisme.
-
Les mutants dont les statocytes contiennent une quantité réduite d’amidon dans les amyloplastes ont une croissance tout à fait normale, mais sont moins sensibles au stimulus gravitropique que les plantes sauvages.
-
Le déplacement des amyloplastes au moyen de champs électro-magnétiques produit une courbure des racines.
Les statocytes, et plus particulièrement les statolithes qu’ils contiennent, jouent donc un rôle important dans la perception du stimulus gravitropique. On peut par ailleurs noter que chez certaines algues ( Charaphycées), des particules formées d’un complexe de protéines, de polysaccharides et de sulfate de baryum sédimentent dans la cellule de façon similaire à celle des amyloplastes des plantes supérieures et interviennent dans la perception de la gravité.
Des mécanismes discutés
Cependant, si l’hypothèse des statolithes est séduisante, certains résultats expérimentaux remettent en cause son unicité en tant que mécanisme de perception de la gravité.
En effet, des mutants d’Arabidopsis totalement dépourvus d’amidon ne s’orientent effectivement pas dans la direction du champ de gravité lorsqu’ils sont placés dans des conditions normales (champ de gravité terrestre = 1 g). Mais lorsqu’ils sont placés dans un champ de gravité plus intense (10 g, obtenu sur une centrifugeuse), ils s’orientent alors selon la direction du champ de gravité.
Il semble donc qu’un autre mécanisme de perception, certes moins sensible que celui lié à la sédimentation des amyloplastes, intervient lors de la réponse gravitropique.
Une hypothèse, dite de « pression du protoplaste », a été avancée. Selon cette hypothèse, la masse entière du cytoplasme participerait à la perception, par le biais d’un dispositif qui percevrait la tension et la compression existant entre la membrane plasmique et la paroi. Du fait du poids du protoplaste, cette tension et cette pression ne serait pas égale sur les différentes faces de la cellule, ce qui fournirait ainsi une information sur la direction du champ de gravité.
Étant donné que l’existence d’un gravitropisme de la racine et de la tige est indispensable à la survie de la plante lors de la germination, et que la gravité est un facteur environnemental constamment présent, il apparaît tout à fait possible que plusieurs voies de perception du stimulus gravitropique aient été sélectionnées au cours de l’évolution, aboutissant ainsi à l’existence de plusieurs systèmes de perception, au sein d’un même organisme.
Transduction du signal
Transformation d’un signal physique en un message biochimique
La sédimentation des amyloplastes dans les statocytes apparaît donc comme l’un des mécanismes majeurs de perception du signal gravitropique. Cependant, la réponse gravitropique, qui consiste en une courbure de la racine, suppose une modification des vitesses d’élongation de part et d’autre de l’axe de la racine. On peut dès lors s’interroger sur les mécanismes qui relient la sédimentation des amyloplastes à cette réponse physiologique. En tout premier lieu, il doit y avoir au niveau des statocytes transformation du signal physique « sédimentation des amyloplastes » en un message biochimique.
Expérimentalement, l’emploi d’inhibiteurs des canaux membranaires étirement-dépendants supprime le gravitropisme. On peut dès lors supposer que la sédimentation des amyloplastes, en agissant physiquement sur ces canaux, les active et permet des modifications de concentration de certaines substances, qui pourraient alors jouer le rôle de messagers biochimiques.
On peut dès lors se demander comment la sédimentation des amyloplastes est reliée à l’activation des canaux étirement-dépendant.
-
On peut supposer simplement que la chute des amyloplastes sur la membrane de la face inférieure du statocyte pourrait, en étirant cette membrane, activer les canaux qu’elle contient.
-
Une hypothèse complémentaire de la précédente suppose que les amyloplastes sont reliés au réseau de filaments d’actine (cytosquelette) existant dans le statocyte. Ces filaments d’actine seraient eux même reliés à la membrane de la cellule. Les mouvements des amyloplastes produiraient donc des tensions dans les filaments d’actine. Ces tensions se propageraient le long des filaments jusqu’à la membrane, produisant ainsi l’activation des canaux sensibles à la déformation.
Quoi qu’il en soit, le passage d’un signal physique (la sédimentation des amyloplastes) à un signal biochimique semble donc se faire par le biais de l’ouverture de canaux membranaires sensibles à la déformation.
Modification des flux d’auxine au sein de la racine après gravistimulation
L’auxine est une hormone végétale synthétisée dans l’apex de la tige, qui est ensuite transportée par les vaisseaux jusqu’à l’extrémité de la racine. Là, l’hormone est redistribuée vers les tissus périphériques puis transportée jusqu’à la zone d’élongation. Cette hormone végétale est susceptible d’intervenir sur la croissance et la division cellulaire. En ce qui concerne son intervention dans le gravitropisme, on dispose des données suivantes :
-
L’utilisation d’auxine marquée radioactivement a permis de montrer que la distribution de l’auxine au sein de la racine était modifiée après gravistimulation. Cette redistribution débute au niveau de la coiffe pour progressivement concerner toute l’extrémité de la racine, y compris la zone d’élongation.
-
On connaît des transporteurs de l’auxine : il s’agit de protéines membranaires pouvant, selon leur type, faire passer l’auxine de l’intérieur de la cellule vers l’extérieur, ou inversement. De proche en proche, ce système permet un transport de l’auxine au sein de l’organe. Des plantes présentant des mutations dans les gènes codants pour ces protéines ont une réponse altérée au stimulus gravitropique. L’utilisation d’inhibiteurs de ces transporteurs supprime totalement la réponse gravitropique.
Les variations de la concentration d’auxine au sein des différentes zones de la racine semblent donc jouer un rôle essentiel dans la mise en place de la réponse gravitropique. Cependant, le mécanisme exact de la redistribution de l’auxine suite à un stimulus gravitropique, ainsi que le lien avec ce qui se produit au niveau des statocytes n’est pas encore élucidé.
La réponse gravitropique : une croissance différentielle
Les phénomènes existant au niveau de la zone d’élongation distale
La réponse à une gravistimulation consiste en une courbure de la racine. Cette courbure se produit au niveau de la zone d’élongation distale (localisée à cheval sur le méristème et le début de la zone d’élongation maximale), qui est située à un ou deux millimètres de distance de la pointe racinaire.
À gauche : représentation schématique d'une racine avec localisation de la zone d'élongation.
À droite : représentation schématique de l’élongation différentielle des cellules, entre la face inférieure et la face supérieure de la racine, lors de la courbure apparaissant suite à une stimulation gravitropique.
Cette différence d’élongation des cellules induit donc une augmentation de la longueur de la partie supérieure de la racine par rapport à la partie inférieure, qui aboutit à la courbure.
Intervention d’un inhibiteur de l’élongation cellulaire
La différence d’élongation des cellules entre les parties supérieure et inférieure est très certainement due à l’intervention d’un facteur modifiant cette élongation. Les résultats expérimentaux suivants ont été obtenus :
À gauche, dispositif expérimental : la moitié de la coiffe de la racine est ôtée.
À droite, résultat observé après quelques heures : courbure de la racine du coté de la demi-coiffe restante
Si on ôte la moitié de la coiffe d’une racine verticale, on voit apparaître une courbure de la racine vers le côté où la coiffe n’a pas été enlevée. Donc les cellules situées au-dessus de la moitié de coiffe restante ont une élongation moindre que celles situées au-dessus de la partie dépourvue de coiffe. Il semble donc que la coiffe soit la source d’un facteur qui limite l’élongation cellulaire.
Ligne du haut : les protocoles expérimentaux, ligne du bas : les résultats observés au bout de quelques heures.
À gauche : on place une barrière physique (lame de mica) entre la coiffe et la zone d’élongation, de façon à couper les flux de substances dans la moitié d’une racine verticale, on voit apparaître une courbure vers le côté opposé à la barrière.
Au milieu : on place une barrière physique (lame de mica) au-dessus de la zone d’élongation, on ne voit apparaître aucune courbure.
À droite : après avoir retiré la coiffe, on place une barrière physique (lame de mica) entre la l'extrémité de la racine et la zone d’élongation, on ne voit apparaître aucune courbure.
Donc les facteurs régulant l’élongation des cellules circulent de façon longitudinale et basipète (de la pointe vers la base).
Si un inhibiteur provenant de la coiffe est responsable de la différence d’élongation des deux côtés de la racine, alors il faut qu’une asymétrie de la distribution de cet inhibiteur soit établie dans la racine.
Expérimentalement, on insère une lame de mica au milieu de la coiffe d’une racine horizontale, de façon à supprimer les flux latéraux de substances à l’intérieur de la coiffe. Alors, la réaction gravitropique observée est très amoindrie.
Ligne du haut : les dispositifs expérimentaux, ligne du bas : les résultats après quelques heures.
À gauche : une petite lame de mica est placée au milieu de la coiffe d'une racine positionnée horizontalement. On n'observe pas de courbure de la racine.
À droite : la racine est disposée horizontalement mais on ne place rien dans la coiffe, on observe quelques heures plus tard une courbure de la racine vers le bas.
Il semble donc que la distribution asymétrique de la substance responsable de la régulation de l’élongation cellulaire s’établisse par des transports latéraux au sein de la coiffe.
Bien évidemment ces résultats ne fournissent aucune indication quant à la nature de l’inhibiteur en question. Par contre, nous avons vu qu’un gradient d’auxine naissait dans la coiffe suite à une stimulation gravitropique et se propageait de façon basipète jusqu’à la zone d’élongation. Ces caractéristiques font donc de l’auxine un candidat potentiel pour le rôle de substance inhibitrice de l’élongation cellulaire.
Le rôle de l’auxine
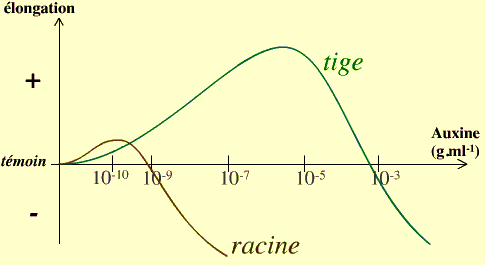
Parmi les effets connus de l’auxine chez les végétaux figure la régulation de la croissance des cellules. L’auxine active une pompe à protons membranaire, ATP-dépendante, ce qui provoque le rejet de protons du côté de la paroi, entraînant ainsi une plus grande extensibilité de celle-ci (voir document Bmédia sur le mécanisme d’action de l’Auxine). D’autre part, l’auxine provoque l’exocytose de composants de la paroi, ainsi que l’activation de certains gènes. L’auxine a un effet sur l’élongation cellulaire dont la courbe dose-réponse est globalement « en cloche », c’est-à-dire que l’auxine a un effet activateur de l’élongation cellulaire aux faibles doses et au contraire inhibiteur à des doses plus élevées. Dans la racine, les concentrations d’auxine rencontrées correspondent au domaine où se produit ce deuxième type d’effet : une augmentation de la concentration d’auxine entraîne une inhibition de l’élongation cellulaire.
Une stimulation gravitropique s’accompagne, nous l’avons vu, d’une redistribution de l’auxine au sein de la racine. Si la racine est placée horizontalement, la concentration d’auxine augmente dans la partie inférieure de celle-ci, tandis qu’au contraire, elle diminue dans la partie supérieure. Ces variations de concentration existent, entre autres, au niveau de la zone d’élongation. L’auxine pourrait donc être l’inhibiteur de l’extension cellulaire intervenant dans la réponse au stimulus gravitropique.
Lorsque la racine est verticale, schéma de gauche, la répartition de l’auxine se fait de façon homogène. Au contraire, lorsque la racine est horizontale (schéma de droite), il y a une redistribution latérale de l’auxine au niveau de la coiffe. La concentration d’auxine dans la partie inférieure de la racine augmente, ce qui inhibe l’élongation cellulaire.
La redistribution asymétrique de l’auxine suite à un stimulus gravitropique induirait donc une modulation de la vitesse de croissance de chacune des faces de la racine, aboutissant à la courbure. Cette hypothèse a été proposée simultanément par Cholodny et Went en 1926. Bien qu’aujourd’hui de nombreux faits expérimentaux soient compatibles avec cette hypothèse, il n’est cependant pas encore possible d’affirmer avec certitude qu’elle correspond bien à une réalité biologique.
Conclusion
Que se passe-t-il dans les tiges ?
Tout ce qui a été vu jusqu’ici concerne principalement le gravitropisme racinaire. Qu’en est-il du gravitropisme des tiges ?
Dans les tiges, il semble que le stimulus gravitropique soit perçu au niveau de cellules présentes dans l’endoderme de la zone d’élongation de la tige. Ces cellules, appelées statocytes, tout comme celles contenues dans la coiffe racinaire, contiennent de volumineux grains d’amidons qui sédimentent sous l’effet de la pesanteur, et qui sont donc aussi appelés statolithes.
Coloration au lugol.
P : parenchyme, C : cambium, Ph : phloème, M : moelle, v : vaisseau, S : statocyte, st : statolithes
Cette sédimentation déclencherait l’activation de transporteurs membranaires actifs de l’auxine. L’action de ces transporteurs créerait un gradient d’auxine entre les faces inférieure et supérieure de la tige. Les concentrations d’auxine présentes dans la tige correspondent, par opposition à ce qui existe dans la racine, à la zone où une augmentation de concentration d’auxine augmente l’élongation cellulaire.
La courbure se fait de la même façon que dans la racine, par une différence d’élongation des cellules entre les faces inférieure et supérieure de la tige. Le signal responsable de cette modulation de l’élongation cellulaire serait donc ici aussi l’apparition de gradients latéraux de la concentration d’auxine consécutive à la stimulation gravitropique.
Dans le cas des tiges, tout comme pour les racines, de nombreuses incertitudes demeurent quant aux voies de transduction et de transmission intervenant dans la réponse gravitropique.
Conclusion et perspectives
La gravité est, sur Terre, présente de façon constante. En cela, elle représente un facteur environnemental très important pour les espèces végétales. Ainsi, le gravitropisme est un phénomène présent chez quasiment toutes les plantes. Les mécanismes exacts qui interviennent dans sa réalisation sont aujourd’hui encore très mal connus. Cependant, les progrès réalisés au cours des dernières années en génétique permettront sans doute, à plus ou moins court terme, d’identifier les gènes intervenant dans le gravitropisme, et, partant de là, de mieux « décortiquer » les voies de transduction et de transmission du stimulus gravitropique. L’exploration de cette voie de recherche a d’ores et déjà débuté et fourni des résultats intéressants.
D’autre part, la réalisation d’expériences scientifiques au cours des missions spatiales, seul moyen de travailler dans un environnement où la gravité est négligeable, a permis et permettra d’intéressantes découvertes sur le gravitropisme végétal.
Il existe également des moyens de mimer l’absence de pesanteur, sur Terre, en laboratoire : la méthode du clinostat, par exemple, consiste à placer les échantillons végétaux sur un tambour en rotation lente, de telle sorte que les forces dues à l’action de la gravité s’annulent pour un tour complet du système. Cependant, les résultats obtenus avec cette méthode ne sont pas toujours exactement les mêmes que ceux obtenus en véritables conditions d’apesanteur…
Voici une liste d’ouvrages ou d’articles contenant des informations plus approfondies sur le gravitropisme des végétaux.
- Advanced plant physiology , 1984, edited by Malcolm B. Wilkins. Pitman, 514 p.
- Perception de la gravité par les plantes et expérimentation spatiale , 1994, G. Perbal et D. Driss-École. Compte rendus de l’académie des sciences, série générale, 11(3) : 163-176.
- Gravitropism in higher plants , 1999, R Chen, E. Rozen et P.H. Masson. Plant physiology, 120 : 343-350.
- Root gravitropism, a complex response to a simple stimulus ? , 1999, E. Rozen, R. Chen et P.H. Masson. Trends in Plant Science, 4(10) : 407-412.
- Mechanisms of the early phases of plant gravitropism , 2000, J.Z. Kiss. Critical Reviews in Plant Science, 19(6) : 551-573
- Amyloplast sedimentation dynamics in maize columella cells support a new model for the gravity-sensing apparatus of roots, 2001, T.L. Yoder, H-q Zheng, P. Todd, L.A. Staehelin. Plant Physiology, 125:1045-1060.
Remerciements
Je remercie le laboratoire Cytologie expérimentale et morphogenèse végétale de l’université Paris 6, et en particulier D. Driss-École et G. Perbal pour les conseils et les illustrations qu’ils ont fournies.
L’animation Flash a été réalisée par Gilles Furelaud (Vie – La biologie au lycée). Les schémas de la roue de Knight sont de Roger Prat (Laboratoire Biologie et Multimédia – Université Paris 6).