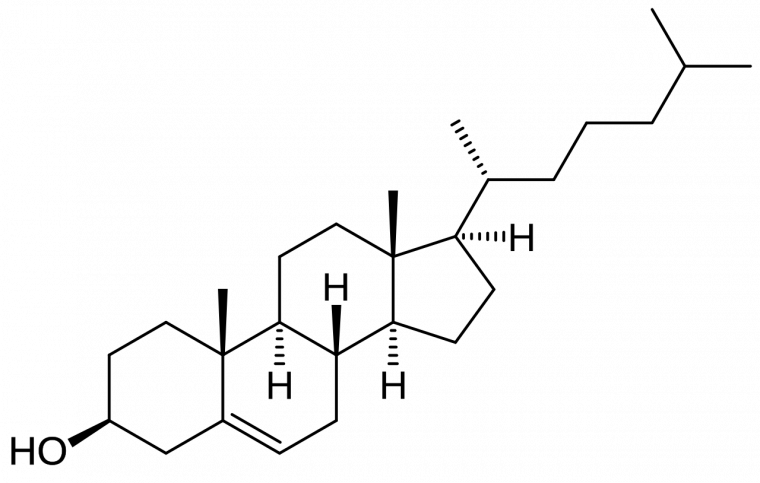Qu’appelle-t-on « bon » et « mauvais » cholestérol ? Après avoir rappelé la structure moléculaire du cholestérol, cet article présente ses deux types de fonction; structurelle et métabolique. Il détaille les différentes molécules assurant le transport du cholestérol et explique leur dénomination de « bon » et « mauvais » cholestérol.
Introduction
Lorsqu’on évoque les problèmes liés à des déséquilibres alimentaires, il est de coutume de parler de « bon » et de « mauvais » cholestérol. Pourtant, à priori le cholestérol est une molécule dont la structure, unique, est bien définie. Alors quelle est la différence entre le « bon » et le « mauvais » cholestérol ?
La structure du cholestérol
Les lipides constituent une famille très hétérogène d’un point de vue structural, mais possédant une caractéristique commune : une solubilité dans l’eau faible, voire inexistante, et inversement une solubilité forte à très forte dans les solvants organiques non polaires.
Le cholestérol pour sa part est un lipide de la famille des stérols. La molécule de cholestérol est basé sur un noyau stéroïde polycyclique issu de la condensation de quatre cycles et possédant un alcool secondaire.
Cette molécule est composée de quatre cycles et possède un groupe hydroxyle OH qui peut réagir avec des acides gras pour donner des esters de cholestérol.
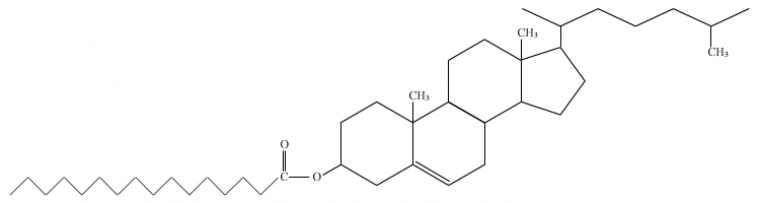
L’alcool secondaire peut réagir avec l’acide carboxylique d’un acide gras pour donner un ester de cholestérol, formant la famille des stérides.
Un stéride est composé d'une molécule de cholestérol reliée par une liaison ester (liaison entre une fonction alcool et une fonction acide carboxylique) à un acide gras. Selon l'acide gras lié, on obtient différents types de stérides.
Dans le cas de la molécule prise ici pour exemple, l'acide gras est l'acide palmitique ou palmitate puisqu'il est saturé et composé de 16 atomes de carbones.
Le palmitate est l'acide gras synthétisé en premier par l'acide gras synthétase (enzyme de synthèse des acides gras), tous les autres acides gras susceptibles d'être produits par nos cellules proviennent de modifications de celui-ci.
Quelques rôles du cholestérol
Le cholestérol est essentiellement retrouvé chez les animaux et les champignons. Chez les végétaux on trouve des molécules assez proches : les phytostérols. Par contre on ne retrouve pas de cholestérol chez les procaryotes (bactéries et archées).
Il s’agit d’un des constituant important des membranes biologiques (jusqu’à 50 % des lipides membranaires en nombre) dont il augmente l’imperméabilité vis à vis des molécules hydrophiles, et dont il participe à la régulation de la viscosité. On parle de rôle tampon car il a tendance à fluidifier les membranes à basse température et à limiter l’augmentation de la fluidité membranaire à haute température (membrane ni trop rigide, ni trop désorganisée).
Mais son rôle est loin de se limiter à un rôle structural, aussi important soit-il.
C’est également un précurseur de nombreuses molécules biologiques importantes telles que les hormones stéroïdiennes (testostérone, œstrogène, etc.), les acides biliaires (impliqués dans la digestion, ils permettent d’émulsionner les acides gras en vue de leur digestion) et certaines vitamines (vitamine D).
Un autre rôle important est son implication dans le transport des lipides dans l’organisme.
Le transport du cholestérol dans l’organisme
Les besoins en cholestérol d’un organisme sont d’environ 1 g par jour. Il existe deux sources : l’alimentation et la biosynthèse de novo.
Deux organes sont particulièrement importants dans le métabolisme du cholestérol : le foie et l’intestin. Tous les deux sont des organes producteurs (le foie en étant le principal), l’intestin assurant en plus l’absorption des lipides alimentaires, et tous les deux ont un rôle central dans le mécanisme de transport du cholestérol et des lipides en général dans l’organisme.
En effet, les lipides étant hydrophobes, il doivent être solubilisés pour que le sang puisse les véhiculer dans l’organisme. Cette solubilisation est obtenue par la formation de particules lipoprotéiques contenant du cholestérol, des triacylglycérols et des protéines appellées apoprotéines.
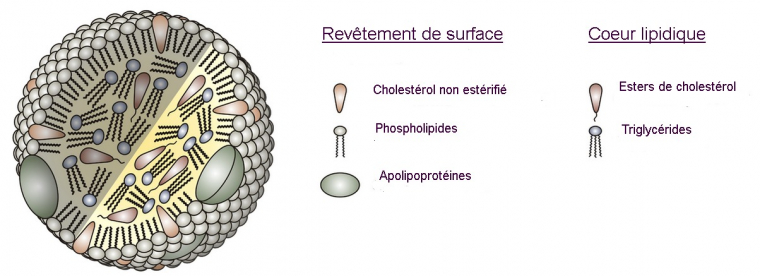
Les lipides les plus hydrophobes (les triacylglycérol et les esters de cholostérol) sont au centre de ces particules. A la périphérie, on trouve des molécules moins hydrophobes, amphiphiles (avec une partie hydrophobe tournée vers le cœur et une partie hydrophile tournée vers l’extérieur) : les apoprotéines et certains lipides comme le cholestérol non estérifié (la fonction alcool étant polaire, il possède une partie hydrophile).
Outre leur rôle dans la solubilisation des lipides, les protéines ont également un rôle d’adressage de ces particules aux différentes cellules de l’organisme.
Les différents types de lipoprotéines
Les particules de lipoprotéines sont composées d'un coeur lipidique contenant des esters de cholestérol et des triglycérides, et d'un revêtement de surface comprenant des phospholipides, du cholestérol non estérifié et des apolipoprotéines.
On distingue plusieurs type de lipoprotéines, classées en fonction de leur densité :
-
Les chylomicron (densité inférieure à 0,94 g.cm3) et les lipoprotéines de très faible densité (VLDL pour Very Low Density Lipoprotein, densité inférieure à 1,006 g.cm3).
Les chylomicrons sont formés au niveau de l’intestin, essentiellement à partir des acides gras et du cholestérol provenant de l’alimentation. Rappelons que les acides gras alimentaires sont principalement trouvés sous forme de triglycérides et que pour être absorbés par la muqueuse intestinale, ils doivent être clivés en acides gras plus monoacylglycérol par des lipases pancréatiques, après solubilisation par les sels biliaires qui permettent d’augmenter la surface de contact. Une fois absorbés, acides gras et monoacylglycérol reforment des triacylglycérols dans les cellules intestinales. Ils serviront à fabriquer les chylomicrons qui seront libérés dans le système lymphatique avant de gagner le système sanguin.
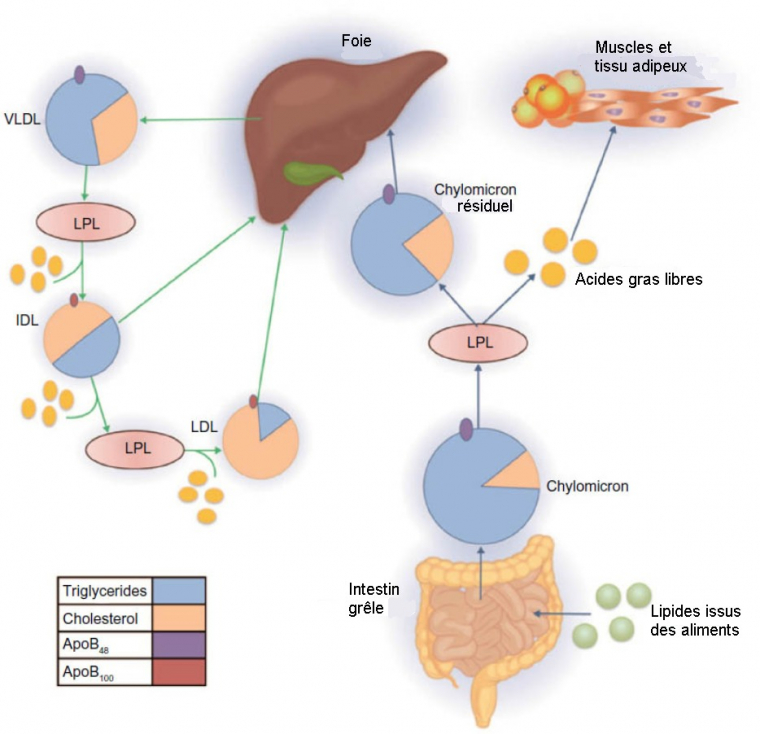
Les chylomicrons sont de grosses particules (180 à 500 nm de diamètre) très riches en triacylglycérol (environ 99 %) dont la solubilité est assurée par l’apoprotéine B-48 qui forme la couche externe hydrophile. Ils apportent surtout des acides gras aux cellules. Ceux-ci sont libérés par l’action d’une lipoprotéine lipase membranaire que l’on retrouve dans les cellules bordant les vaisseaux sanguins qui traversent les organes consommateurs (essentiellement les muscles qui les utilisent comme source d’énergie et le tissus adipeux pour une mise en réserve). Les chylomicrons perdent donc une partie de leurs triacylglycérols et vont devenir des résidus de chylomicron, proportionnellement plus riches en esters de cholestérol, qui vont être captés par le foie. -
Les VLDL, pour leur part, sont des particules ayant un rôle analogue aux chylomicrons, mais ils sont formés au niveau du foie à partir des triacylglycérol et du cholestérol néosynthétisés par celui-ci. La couche externe est formée par deux apoprotéines, l’apo B-100 et l’apo E.
-
Lipoprotéines de densité intermédiaire (IDL pour Intermediate Density Lipoprotein, densité comprise entre 1,006 et 1,019 g.cm3).
Ils correspondent aux résidus de VLDL dont une partie des triacylglycérols ont été captés par des cellules utilisatrices. Une partie des IDL est recaptée par le foie, comme les résidus de chylomicrons, mais une autre partie continue d’évoluer en perdant toujours plus de triacylglycérols jusqu’à devenir des LDL riches en cholestérol. -
Lipoprotéine de faible densité (LDL pour Low Density Lipoprotein, densité comprise entre 1,019 et 1,063 g.cm3).
Les LDL sont les particules assurant l’essentiel de la fourniture du cholestérol aux cellules.
La particule de LDL a un diamètre de 22 nm et elle est composée d’un cœur d’environ 1500 molécules d’esters de cholestérol fortement hydrophobe, entouré d’une molécule de l’apoprotéine apo B-100 et de cholestérol non estérifié.
L’utilisation des LDL par les cellules qui ont besoin de cholestérol est très bien documentée, et son étude est à la base de la connaissance que nous avons de l’endocytose médiée par des récepteurs. En cas de besoin en cholestérol, une cellule active la transcription du gène codant pour un récepteur membranaire au LDL (R-LDL). Une fois ce récepteur exprimé à la surface cellulaire au niveau de zones appelées puits recouverts (coated pits), les LDL vont se lier à lui via leur apoprotéine apo B-100. Cette liaison va entraîner la formation d’une vésicule d’endocytose par assemblage d’un manteau de clathrine. Après détachement du manteau de clathrine, la vésicule rejoint l’endosome précoce qui est un compartiment acide (présence de pompes à protons abaissant le pH aux environs de 5). Cette acidification entraîne la dissociation entre les LDL et les R-LDL. Les récepteurs sont recyclés à la membrane cytoplasmique par exocytose, les LDL étant acheminées vers les lysosomes via les endosomes tardifs. Dans les lysosomes, les LDL sont dégradées et leurs constituants, au premier rang desquels se trouve le cholestérol, libérés pour utilisation par la cellule. Lorsque la cellule n’a pas ou plus besoin de cholestérol, le gène codant pour le R-LDL subit une régulation négative et le R-LDL cesse d’être produit. Ce qui détermine l’activation ou non du gène est le taux de LDL interne à la cellule. -
Lipoprotéine de haute densité (HDL pour High Density Lipoprotein, densité comprise entre 1,063 et 1,21 g.cm3).
Les HDL sont des particules riches en esters de cholestérol et comportant l’apoportéine apo-A1. Elles ont pour fonction de capter les molécules de lipides et surtout de cholestérol libre des tissus périphériques.
En effet, initialement, le foie produit une particule comportant l’apo-A1 et peu de lipides avec. Une fois dans le plasma, cette particule initiale va s’enrichir en cholestérol pour devenir une HDL. Pour cela une acétyltransférase présente au niveau des HDL, la LCAT (Lecithin Cholesterol Acyl Transferase), va estérifier le cholestérol libre en provenance des membranes cellulaires et des parois des vaisseaux sanguins. La formation des HDL peut donc se faire à partir du cholestérol présent dans les plaques d’athérome. Les HDL peuvent ensuite transmettre directement leur cholestérol aux LDL et aux VLDL grâce à l’action d’une molécule de transfert, la Cholesterol Ester Transfer Protein (CETP), mais ils peuvent aussi être captés par le foie.
Apo :apolipoprotein ; IDL :intermediate-density lipoprotein ; LDL :low-density lipoprotein ; LPL :lipoprotein lipase ; VLDL :very low-density lipoprotein.
« Bon » et « mauvais » cholestérol
Concernant le cholestérol, les deux particules plus spécialement chargées de son transport sont donc les LDL et les HDL. Leur rôle est différent : les LDL apportent le cholestérol aux cellules, les HDL récupèrent le cholestérol périphérique et peuvent le ramener au foie.
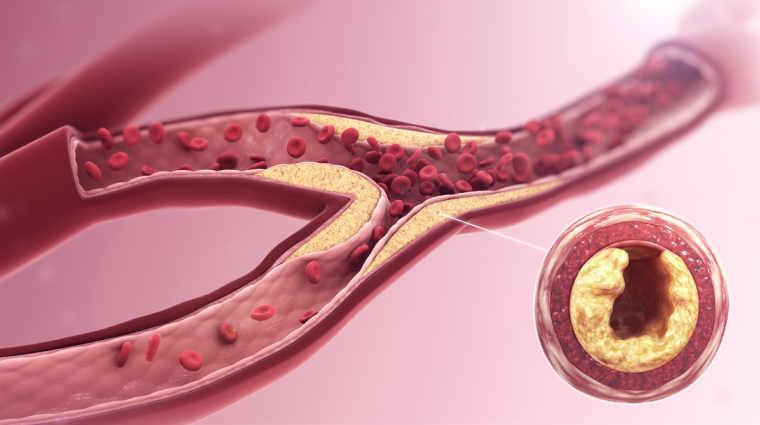
Une quantité trop élevée de LDL aura des conséquences négatives. En effet, s’il y a plus de cholestérol transporté par les LDL que les cellules n’en ont besoin, ces LDL ne seront pas utilisées par les cellules et resteront dans le sang (puisqu’elles ne sont plus internalisées par endocytose). Elles vont alors se déposer sur les parois des vaisseaux sanguins, formant des plaques d’athéromes qui diminuent le diamètre des vaisseaux. Cette diminution de diamètre des vaisseaux augmente le risque d'accident vasculaire. C’est pourquoi les LDL sont appelées « mauvais cholestérol ». Il ne s’agit donc pas d’une molécule de cholestérol particulière, mais d’une particule de transport du cholestérol particulière.
Quand la plaque d'athérome (composée de calcium, de débris cellulaires, de cholestérol et lipides) se dépose dans une artère, elle la durcit et en réduit le débit, on parle d'athérosclérose.
Si la plaque vient à boucher le vaisseau, les conséquences dépendent de sa localisation. Elle provoquera, par exemple, un infarctus, si elle se situe dans une artère coronaire et un AVC (accident vasculaire cérébral) si elle se situe dans une carotide.
Au contraire, les HDL assurent le captage du cholestérol excédentaire de l’organisme et son élimination en l’apportant au foie. Elles ont donc une action de « nettoyage » des vaisseaux sanguins à l’opposé de l’action des LDL. C’est pourquoi les HDL sont appelées « bon cholestérol ».
Conclusion
Les maladies cardiovasculaires sont la première cause de mortalité en France avec 180 000 décès annuels. On dénombre pas moins de 120 000 infarctus du myocarde et 130 000 accidents vasculaires cérébraux chaque année.
Les causes sont multiples mais on peut mettre en avant une alimentation déséquilibrée (trop de graisse saturée) et le manque d’exercice physique.
Mais il existe d’autres facteurs pouvant générer ou aggraver le phénomène (prédispositions génétiques, diabète, etc.). Dans ce cadre, le taux de « bon » et de « mauvais » cholestérol est un indicateur important du risque cardiovasculaire. Dans l’idéal, il est conseillé d’avoir un rapport LDL/HDL inférieur à 4,5 pour des personnes ne présentant pas de risques particuliers, avec un taux de LDL ne dépassant pas 1,5 g/l et un taux de HDL au moins égal à 0,5 g/l.
Lorsque ce rapport est dépassé, le meilleur moyen de le faire descendre est de modifier ses habitudes alimentaires.
Contrairement à ce que l’on pourrait penser, le plus important n’est pas de diminuer la quantité de cholestérol absorbé (la majorité est synthétisée par l’organisme), mais plutôt la quantité d’acides gras saturés absorbés, présents en grande quantité dans le beurre ou de nombreuses viandes animales par exemple.
Pratiquer des exercices physiques est également recommandé.
Il est à noter qu’il ne faut pas confondre modification des habitudes alimentaires visant à faire baisser le rapport LDL/HDL et régime amaigrissant. Dans le premier cas, il s’agit plus d’une modification qualitative (même si réduire sa consommation de lipides entraîne souvent une perte de poids), alors que dans le second cas il faut diminuer l’apport énergétique global.
Il est préférable que les traitements médicamenteux, qui sont efficaces mais peuvent avoir certains effets secondaires, soient réservés en seconde intention si des mesures d’hygiènes de vie ne suffisent pas. Il existe différentes catégories de molécules :
-
Les résines, qui empêchent la réabsorption des sels biliaires au niveau intestinal (pour rappel, les sels biliaires sont des dérivés du cholestérol) ;
-
Les statines qui inhibent la synthèse endogène du cholestérol en inhibant l’enzyme clef de sa voie de biosynthèse (la HMG-CoA réductase) ;
-
Les fibrates, qui inhibent également la synthèse endogène du cholestérol ;
-
La niacine (vitamine B3) qui diminue la production de LDL et de triacyglycérol.
Le choix d’un traitement plutôt qu’un autre doit être fait en fonction des caractéristiques individuelles (taux de LDL, de DHL, de triglycérides, facteurs de risques, etc.). En effet, chaque molécule a un effet spécifique (action variable sur les taux de LDL, de HDL de triacylglycérol, etc.) et peut être indiquée ou non selon la situation. Un suivi est d’ailleurs généralement nécessaire pour ajuster le traitement si besoin.