Cet article se veut être une introduction pour les biologistes aux bases physiques et chimiques de la lumière et de la couleur chez les Animaux. Nous ne rentrerons donc pas dans tous les détails mécanistiques à l’origine de ces deux phénomènes, mais ceux-ci seront suffisamment explicités à chaque fois que nécessaire pour comprendre la réalité biologique.
La lumière est un phénomène physique double
La lumière est un phénomène physique double, ayant à la fois une nature ondulatoire (onde électromagnétique) et corpusculaire (photons). Nous utiliserons alternativement l’une ou l’autre définition pour comprendre les phénomènes décrits ci-dessous.
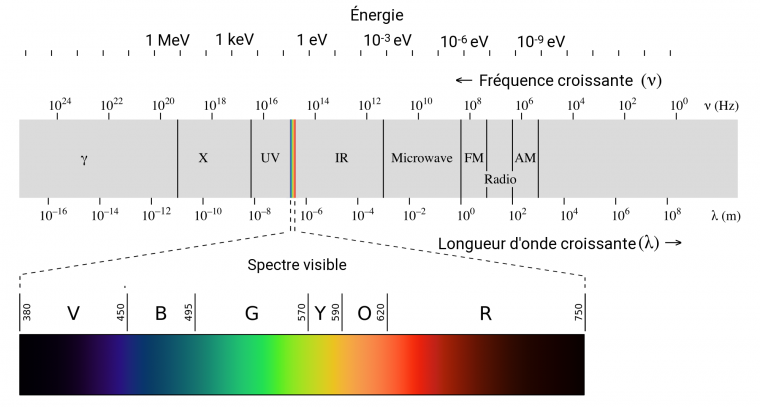
Le spectre électromagnétique correspond à l’ensemble des longueurs d’onde des rayonnements électromagnétiques, depuis les rayons gammas (λ < 10−12 m) jusqu’aux ondes radio (λ > 1 m). Une partie de ce spectre, entre 400 et 800 nm de longueur d’onde, correspond à la lumière dite visible car elle perceptible par notre œil d’humain.
L’énergie d’une onde lumineuse est inversement proportionnelle à sa longueur d’onde. Ainsi, les ultraviolets (longueur d’onde entre 10 et 400 nm) sont plus énergétiques que les infrarouges (entre 800 nm et 3 mm), eux-mêmes plus énergétiques que les micro-ondes (de 3 mm à 30 cm). Du fait de leurs différences d’énergie, les ondes lumineuses n’interagissent pas toutes de la même manière avec la matière. En particulier, les UV et le visible peuvent exciter les électrons alors que les infrarouges font vibrer les liaisons chimiques des molécules.
La couleur a une définition sensorielle, propre à chaque individu
La couleur est la façon dont chacun de nous perçoit un objet en fonction des longueurs d’onde (du visible pour les humains) qu’il nous envoie. La couleur est donc une perception d’un signal environnemental. Elle est alors propre à chaque individu : tous les êtres humains voient les couleurs différemment.
La lumière visible est définie par la gamme d’ondes lumineuses capables d’être captées par l’œil humain et pouvant induire une réponse du cerveau. Les espèces qui ont des capacités visuelles différentes peuvent voir d’autres plages de longueurs d’onde. Par exemple, les abeilles sont bien connues pour voir des signaux dans l’ultraviolet proche. De l’autre côté du spectre visible, certains serpents peuvent détecter une partie du rayonnement infrarouge, bien que l’organe sensoriel impliqué ne soit pas l’œil (Gracheva et al., 2010).
Les êtres vivants ne produisent généralement pas la lumière qu’ils émettent
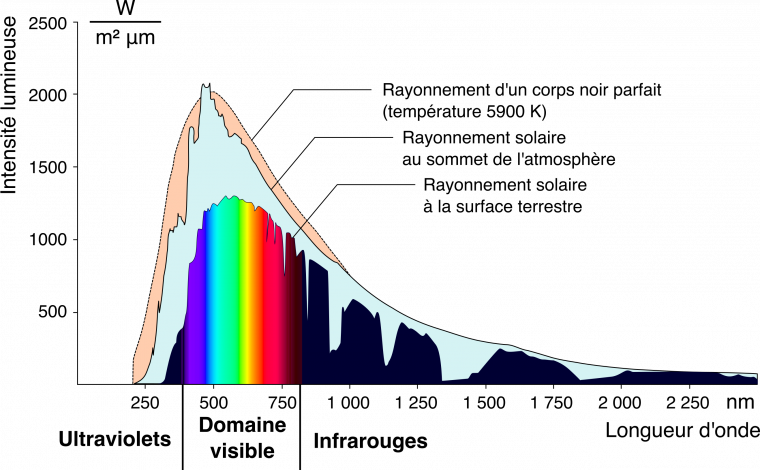
La couleur résulte donc de l’interaction entre un phénomène optique, la lumière, et un système sensoriel (généralement visuel). Pour qu’un objet, biologique ou non, nous apparaisse coloré, il faut donc qu’il émette de la lumière. Sauf dans le cas de la bioluminescence, où les organismes eux-mêmes émettent un nouveau photon par une réaction enzymatique (que nous ne détaillerons pas ici), tout objet biologique ne produit pas réellement de la lumière. La couleur d’un objet est due à des phénomènes d’absorption et de diffusion des rayons lumineux provenant du Soleil en milieu naturel. La couleur d’un objet vu par réflexion correspond alors aux longueurs d’onde qu’il n’absorbe pas et qu’il renvoie. Le Soleil émet un spectre de longueurs d’onde allant des ultraviolets aux infrarouges, avec un pic à 504 nm (vert). Pourquoi cette gamme de longueurs d’ondes en particulier ? Pourquoi le Soleil n’émettrait-il pas à des longueurs d’ondes inférieures ou supérieures ? La raison physique est que tout corps émet des radiations ; la loi de Wien postule ainsi que la longueur d’onde de ces radiations dépend de la température de l’objet. Les humains avec une température de 37 °C émettent principalement dans l’infrarouge (à 9 350 nm). Le Soleil, ayant une température de surface de plus de 5 000 °C, émet des longueurs d’onde plus faibles (c’est-à-dire avec des énergies plus élevées) ayant un pic très large autour de 500 nm.
Sur Terre, les êtres vivants seraient ainsi adaptés à détecter les signaux électromagnétiques de longueurs d’ondes solaires. Si seuls les Animaux disposent d’un système nerveux spécialisé dans le traitement des informations visuelles, de nombreux autres êtres vivants sont capables de percevoir et de réagir à des stimulations lumineuses (p. ex. phototropisme des Angiospermes ou phototactisme des Euglènes). Certains Champignons disposent de photorécepteurs qui captent des longueurs d’ondes du visible ou du proche ultraviolet (Tisch and Schmoll, 2010).
En conclusion, une feuille, un papillon ou un poisson, pourtant colorés, ne sont pas eux-mêmes source de leur lumière et ne renvoient qu’une partie de la lumière (solaire) qu’ils reçoivent. Ce qui les rend visibles est le résultat de leur interaction avec la lumière incidente du Soleil.
Les couleurs d’origine chimique : l’absorption par un pigment
Transparence et pigmentation
Considérons un organisme qui reçoit de la lumière solaire constituée de toutes les longueurs d’onde visibles (lumière dite blanche). Nous nous situons derrière l’organisme et sur le trajet des rayons lumineux. Si la lumière traverse totalement cet organisme de part en part, alors les longueurs d’onde que nous percevons sont inchangées. Rien dans cet organisme ne le rend différent de l’environnement dans lequel il est et notre œil ne peut pas le distinguer, ce qui le rend transparent ; c’est le cas de certains Cnidaires et de la plupart des cellules.
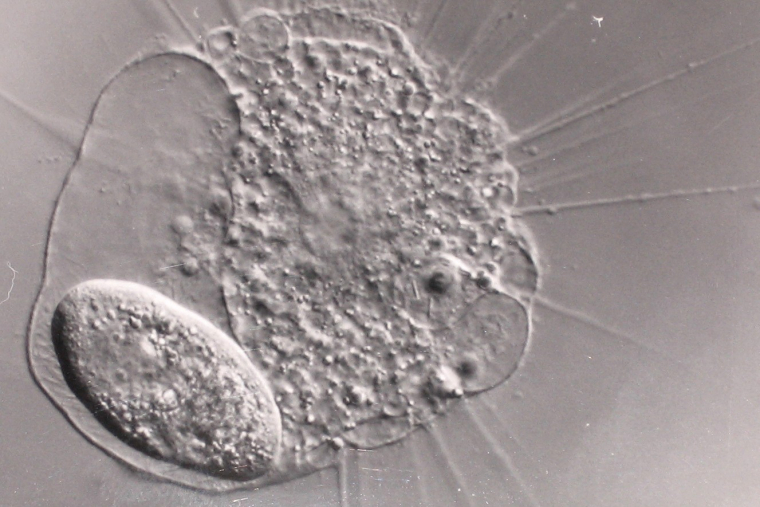
Cette observation d’une paramécie (en bas à gauche) phagocytée par un héliozoaire aux nombreux exopodes n’a été possible que grâce à une technique de microscopie spéciale, la microscopie à contraste interférentielle. Celle-ci permet notamment de souligner les différences de densité entre compartiments, leur contenu étant transparent à la lumière visible quelle que soit la cellule.
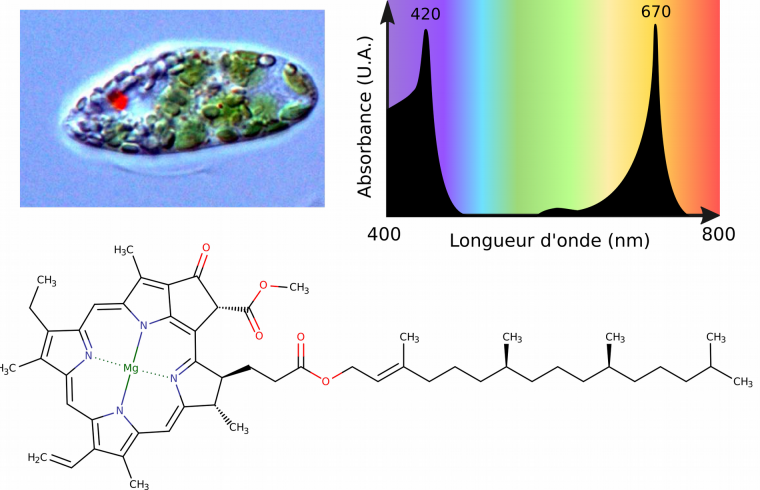
Supposons maintenant qu’au sein de l’organisme soit présente une molécule, qui, par sa structure, peut absorber une partie du spectre visible de la lumière incidente. Cette molécule s’appelle alors un pigment. Une partie de la lumière incidente qui traverse cet organisme est absorbée par ce pigment et nous ne percevons que l’autre partie du spectre, celle transmise à travers le tissu pigmenté. Nous avons alors une impression de couleur. Par exemple, la chlorophylle des Euglènes absorbe majoritairement le violet, le bleu et le rouge. Les longueurs d’ondes transmises correspondent à l’orange, au jaune et surtout au vert, ce qui explique que ce pigment nous paraisse vert. On note donc que la couleur d’un pigment est définie par les longueurs d’onde qu’il transmet, pas par celles qu’il absorbe.
| Longueur d’onde absorbée | Violet | Bleu | Bleu-vert | Vert-bleu | Vert | Jaune | Orange | Rouge |
|---|---|---|---|---|---|---|---|---|
| Couleur du pigment | Vert-jaune | Jaune | Orange | Rouge | Violet | Bleu | Bleu-vert | Vert-bleu |
Ce phénomène cache pourtant une subtilité. Pendant la traversée du tissu, l’absorption fait diminuer l’intensité totale de la lumière. Ainsi, un organisme chlorophyllien épais ne devrait pas nous paraître vert mais noir ! Pour qu’un organisme épais apparaisse coloré et non pas noir, il faut qu’une surface réfléchissant la lumière incidente soit présente sous la couche pigmentée. Chez les Animaux, l’ensemble des tissus conjonctifs sont réfléchissants. Cela explique notamment pourquoi les individus albinos ne sont pas transparents mais blancs : dépourvus de pigment, seul leur tissu conjonctif est visible et de couleur blanche car il réfléchit toutes les longueurs d’onde visibles de la lumière incidente. De même, chez les Oiseaux, la structure des plumes est constituée d’un mélange kératine/air qui réfléchit la lumière visible. Ainsi, bien qu’une plume isolée et dépigmentée soit fine, elle paraît blanche et non transparente.
Bases physico-chimiques de l’absorption de la lumière par les pigments
Les bases physiques de l’absorption de la lumière par un pigment sont directement reliées à sa structure chimique. Toute molécule interagit avec la lumière mais toutes ne sont pas capables d’absorber des longueurs d’onde du spectre visible de la lumière. Pour expliquer ce phénomène, il faut comprendre comment se fait l’absorption d’un photon par une molécule, plus particulièrement lorsque ce photon a une énergie correspondant aux longueurs d’onde dans l’UV et dans le visible.
Comme nous l’avons vu précédemment, ce type de photons a une énergie suffisante pour interagir avec les électrons d’un atome ou d’une molécule. Les électrons possèdent un niveau d’énergie de base (le plus bas) et ils peuvent accéder à un nombre fini de niveaux de plus haute énergie qui sont dits excités. Un niveau excité possède une énergie bien définie et un électron ne peut l’atteindre que s’il reçoit une énergie exactement égale à la différence d’énergie entre son état de base et cet état excité. Or les photons ont eux aussi une énergie bien définie (inversement proportionnelle à la longueur d’onde). Ainsi, tous les photons (et donc toutes les longueurs d’onde) ne peuvent pas exciter un électron donné ; seuls les photons ayant la bonne énergie le peuvent, ce sont les seuls à être absorbés.
Dans le cas d’une molécule, les électrons sont partagés entre les atomes ; on dit qu’ils sont délocalisés. L’importance de cette délocalisation dépend du type d’atome (plus ou moins électronégatifs), du type de liaison (simple, double, cyclique, etc.), de leur nombre et de l’environnement direct de la molécule (solvant, interaction avec d’autres molécules, etc.). La délocalisation affecte directement les niveaux d’énergie des électrons et donc les longueurs d’onde qu’ils peuvent absorber. Généralement, plus les électrons sont délocalisés, plus les niveaux excités sont proches du niveau de base. Il faut donc peu d’énergie pour exciter des électrons très délocalisés, ce qui correspond à des longueurs d’onde relativement élevées.
Par exemple, une molécule organique composée d’atomes d’hydrogène, de carbone et d’oxygène avec des liaisons simples possède des électrons peu délocalisés ; chaque électron reste centré autour des atomes et de la liaison où il est impliqué. Ces molécules absorbent dans les UV lointains (très énergétiques) mais pas dans le visible (peu énergétiques), elles apparaissent donc transparentes ; c’est le cas du glucose en solution. À l’inverse, une molécule composée d’atomes d’hydrogène, de carbone, d’oxygène et d’azote avec des liaisons doubles alternées (conjuguées) et/ou des cycles aromatiques possède des électrons fortement délocalisées autour de toutes ces liaisons. Les électrons impliqués sont facilement excitables, ils peuvent absorber des électrons de faible énergie dans le domaine du visible. Cette région de la molécule absorbant spécifiquement les longueurs d’onde du visible s’appelle le chromophore. Le noyau tétrapyrrolique de la chlorophylle en est un exemple. Sa délocalisation électronique très prononcée permet d’absorber des longueurs d’onde dans le bleu (450 nm) et dans le rouge (> 600 nm), d’où la couleur verte de la chlorophylle.
Chez les Euglènes, la chlorophylle est contenue dans les chloroplastes. Sa structure chimique montre de nombreuses doubles liaisons, des hétérocycles aromatiques et la présence d’un atome de magnésium qui permettent d’absorber des longueurs d’onde peu énergétiques, telles que celles dans le visible. Cette région de la molécule fait office de chromophore grâce à la délocalisation très importante de ses électrons. U.A. : unité arbitraire. Photographie d'euglène par Ellis O'Neill, Wikimedia.
Une fois qu’un électron a été excité, il y a plusieurs issues possibles. Nous ne les détaillerons pas toutes ici car cela dépasse le cadre de cet article. L’électron peut revenir à son niveau de base par de nombreux petits paliers ce qui transforme l’énergie correspondante en chaleur. L’électron peut aussi perdre son énergie par petits paliers puis par un plus gros saut d’énergie jusqu’à son niveau de base. Si ce saut énergétique est d’amplitude suffisante, un photon de longueur d’onde dans le visible est émis : c’est le phénomène de fluorescence. La fluorescence produit donc nécessairement de la lumière à plus haute longueur d’onde (moins énergétique) que la lumière absorbée. L’électron excité peut aussi transmettre son énergie à l’électron d’une molécule voisine de quelques nanomètres. C’est le phénomène de transfert d’énergie par résonance mis en œuvre dans les antennes collectrices lors de la photosynthèse et dans la technique du FRET (Förster resonance energy transfer). Finalement, l’énergie de l’électron excité peut être utilisée dans une réaction chimique. Puisque la lumière en est à l’origine, on parle de réaction photochimique. Un exemple est le photoblanchiment, lors duquel le chromophore est dégradé chimiquement après l’absorption d’un photon, ou encore la photoisomérisation du 11-cis-rétinal en all-trans-rétinal qui est à la base du mécanisme de la vision.
Les couleurs pigmentaires chez les Animaux
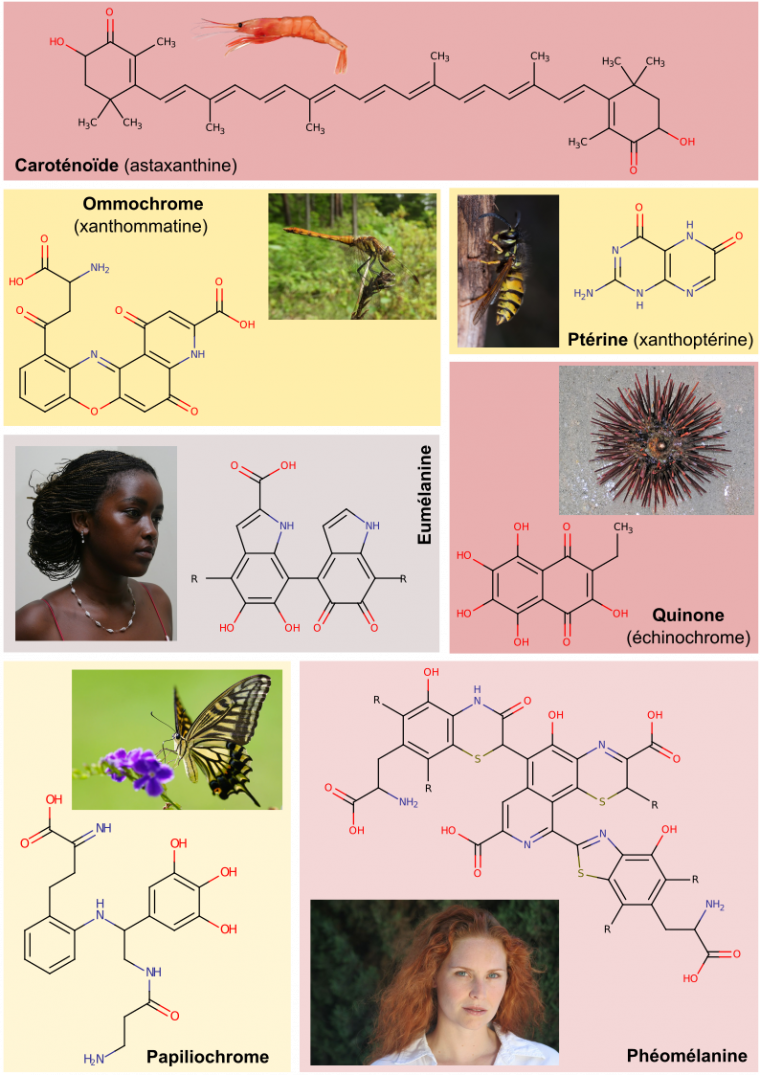
Chez les Animaux, on dénombre près d’une dizaine de familles de chromophores et donc autant de types de pigments. Des variations existent autour de la structure chimique de ces chromophores ce qui augmente encore la diversité de couleurs que les animaux peuvent produire. Il est à noter que nous n’avons pas représenté sur la figure 6 la classe des bilines, pourtant largement répandue, car elle est basée sur un chromophore présenté plus haut : le noyau tétrapyrrolique (figure 5). Les bilines sont formées par l’ouverture du cycle tétrapyrrolique et sont associées à des protéines, appelées alors chromoprotéines. La couleur normale des bilines est le bleu-vert mais elles sont généralement associées à des pigments jaunes ce qui donne la couleur verte caractéristique des Sauterelles, des Mantes, etc.
L’eumélanine et la phéomélanine, les deux principales formes de mélanine, sont des pigments hautement polymérisés. Nous n’avons représenté ici que des dimères et des trimères mais les combinaisons de polymérisation sont nombreuses et peuvent en particulier se faire au niveau des liaisons – R.
Source des photographies : Pandalus borealis : NOAA FishWatch/Wikimedia domaine public ; Vespula vulgaris : Jeroen Ruël/Wikimedia CC BY-SA ; couleur de la peau humaine : peter klashorst/Wikimedia CC BY ; femme rousse : dusdin on flickr/Wikimedia CC BY ; Papilio xuthus : Peellden/Wikimedia CC BY-SA ; Arbacia punctulata : James St. John/Wikimedia CC BY ; Sympetrum darwinianum : R78G addz/Wikimedia CC0.
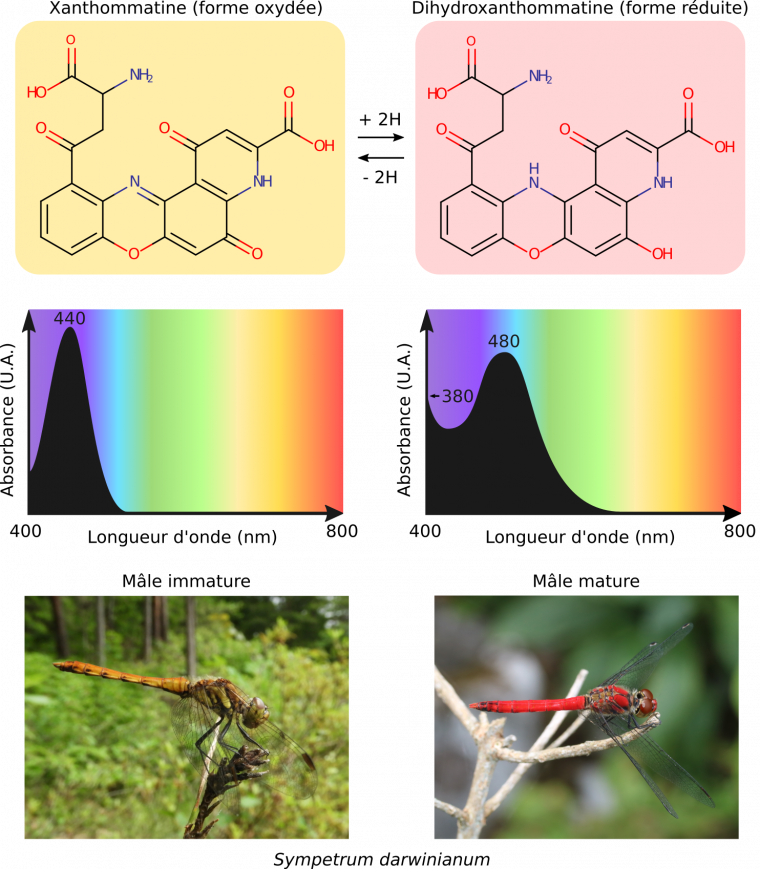
Comme exemple de variation nette de couleur à partir d’un même chromophore, citons les ommochromes des Arthropodes qui possèdent un chromophore de type phénoxazinone. Lorsque celui-ci est à l’état oxydé, l’ommochrome est jaune car il absorbe les longueurs d’onde dans le violet et le bleu (440 nm). Lorsque le chromophore est à l’état réduit, l’ommochrome devient rouge en absorbant les longueurs d’onde dans le bleu et le vert (480 nm). Cet effet, appelé bathochrome car il va vers les longueurs d’onde d’énergies plus faibles, s’explique notamment par de nouvelles formes de résonance du chromophore (Linzen, 1974). Les électrons y sont plus délocalisés qu’à l’état oxydé, ils sont donc plus facilement excitables et ils absorbent alors dans le bleu-vert. L’effet bathochrome des ommochromes est notamment visible chez les mâles des Libellules des genres Crocothemis et Sympetrum dont le corps passe du jaune au rouge lors de la maturation sexuelle (Futahashi et al., 2012).
Les couleurs d’origine structurelle : la diffusion par un tissu
Dans ce qui précède, la couleur était due à une molécule, appelée pigment, qui absorbait la lumière. Toutefois, il existe d’autres processus physiques permettant de modifier la lumière incidente blanche en lumière émise avec une certaine teinte. Ces processus ne sont pas liés à l’absorption de la lumière par une molécule mais à sa diffusion par les tissus. En rencontrant un tissu, la lumière interagit avec sa structure ; les longueurs d’onde peuvent alors ne pas être toutes diffusées de la même manière (diffusion différentielle). Ces couleurs d’origine structurelle, sont, à l’instar des couleurs d’origine pigmentaire, des couleurs qui ne sont pas dues à l’émission de lumière par les tissus : les tissus sont « passifs » vis-à-vis de la lumière puisqu’ils n’en produisent pas directement. On distingue deux mécanismes physiques en fonction de la structure du tissu.
Les couleurs dues à la diffusion incohérente
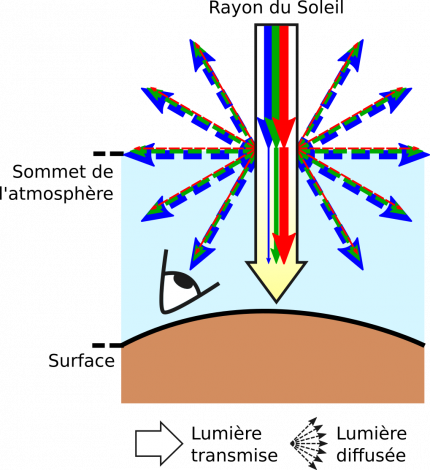
Avant d’arriver au sommet de l’atmosphère, les rayons du Soleil sont composés de toutes les longueurs d’onde dans le visible ; ils sont blancs. Lorsque ces rayons atteignent l’atmosphère, ils interagissent avec les particules qui la composent. Une partie des longueurs d’onde du rayon solaire est alors diffusée de manière incohérente dans toutes les directions. Du fait de la taille des particules, l’intensité de diffusion est plus importante pour les longueurs d’onde dans le bleu que celles dans le vert et dans le rouge. Or, lorsque nous regardons le ciel sans observer le Soleil directement en face, nous voyons la lumière diffusée et non pas transmise. Cette lumière diffusée étant plus riche en longueurs d’onde dans le bleu que dans le reste du spectre, le ciel nous apparaît bleu. À l’inverse, la lumière transmise à travers l’atmosphère est appauvrie en longueurs d’onde dans le bleu par rapport au reste du spectre électromagnétique. Le Soleil nous apparaît donc jaune. Il est à noter que la diffusion se fait dans tout le volume de l’atmosphère et pas seulement à son sommet, et que les rayons diffusés sont à leur tour diffusés par les particules qu’ils rencontrent dans l’atmosphère, ce qui accentue les couleurs respectives du ciel et du Soleil.
Une structure non-ordonnée et dont les éléments ont une taille comparable à la valeur des longueurs d’onde de la lumière visible (quelques centaines de nanomètres) produit une diffusion différentielle en fonction des longueurs d’onde : c’est la diffusion incohérente. Le bleu du ciel est par exemple largement dû à la diffusion plus importante des longueurs d’ondes autour de 500 nm par les particules de l’atmosphère alors que les autres longueurs d’onde sont transmises sans être (trop) diffusées. Ainsi, la lumière provenant du ciel et arrivant au sol, donc à nos yeux, est majoritairement constituée de longueurs d’onde dans le bleu. À l’inverse, la lumière provenant directement du Soleil et qui est transmise à travers l’atmosphère s’appauvrit en bleu ; elle paraît jaune (Figure 2 et 8).
Les couleurs dues à la diffusion cohérente
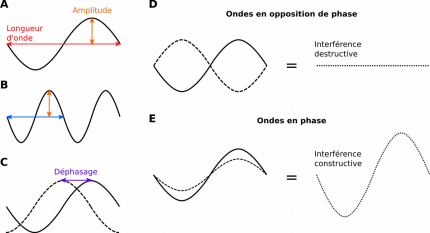
En A et B sont représentées deux ondes ayant la même amplitude mais des longueurs d’onde différentes. La longueur d’onde en B vaut la moitié de celle en A. En C, lorsque deux ondes de même longueur d’onde (peu importe l’amplitude) sont en décalage l’une par rapport à l’autre, on parle de déphasage. En D, deux ondes déphasées d’une demie longueur d’onde sont en opposition de phase, l’interférence correspondant à la somme des deux courbes en tout point est alors destructive : l’onde résultante a une amplitude nulle. En E, deux ondes déphasées d’une longueur d’onde sont en phase, l’interférence est constructive et leurs amplitudes s’additionnent.
Une structure ordonnée, comme un cristal, un réseau de cavités ou une superposition de couches minces réfléchissantes, diffuse les longueurs d’onde en modifiant leur phase. Les ondes diffusées déphasées interagissent et interfèrent : c’est la diffusion cohérente. Certaines longueurs d’onde diffusées sont en opposition de phase, menant à des interférences destructives et donc à la disparition de ces longueurs d’onde. À l’inverse, d’autres longueurs d’onde sont en phase et deviennent prédominantes. La lumière diffusée apparaît alors colorée. Ces phénomènes d’interférence peuvent dépendre de l’angle de vision et produisent alors des couleurs iridescentes, comme à la surface d’une bulle de savon.
Les couleurs d’origine structurelle chez les Animaux
Chez les Animaux, ces deux mécanismes de diffusion de la lumière incidente sont largement mis en jeu dans la production de la couleur bleue. Le principal mécanisme structurel dans le vivant reste la diffusion cohérente. Parmi les exemples les mieux compris, citons la structure en réseau du collagène de la peau des Mandrills (Prum and Torres, 2004), le réseau de cavités des plumes des Aras (Yin et al., 2012), l’agglomération de protéines appelées réflectines chez les Céphalopodes (Cai et al., 2019) ou encore les nanosphères du tégument des Zygoptères (Demoiselles) du genre Coenagrion (Prum et al., 2004). Il n’y aurait que chez certaines grenouilles que le bleu serait dû à de la diffusion incohérente (Bagnara et al., 2007). Cette dernière est par contre largement mise en œuvre dans la production de blancs vifs et purs, notamment chez les Céphalopodes (Mäthger et al., 2013) et les Coléoptères (Burresi et al., 2015). Les cas de couleurs iridescentes chez les Animaux sont nombreux et bien documentés. Nous pouvons citer ici les magnifiques ailes des papillons du genre Morpho (Prum et al., 2006) et des Colibris (Greenewalt et al., 1960), ou encore les écailles des élytres chatoyantes de certains Coléoptères (Seago et al., 2009), pour lesquels une iridescence a été préservée dans des fossiles vieux de 50 millions d’années ! (Parker et McKenzie, 2003). L’iridescence est également produite par les cristaux de guanine de certains copépodes du genre Sapphirina qui paraissent totalement bleus ou totalement transparents selon l’angle. On note que les couleurs d’origine structurelle peuvent s’ajouter à celles générées chimiquement par les pigments. Chez les Aras par exemple, le vert de certaines plumes provient de l’absorption par un pigment jaune et de la diffusion cohérente du bleu par les barbes.
Les diffusions cohérente et incohérente de la lumière incidente peuvent produire du bleu, du blanc ou de l’iridescence (dont des effets métallisés).
Sources des images : Mandrill : Rolf Dietrich Brecher/Wikimedia CC BY-SA ; Ara : Jay Warburton/Wikimedia CC BY ; Pieuvre : Jens Petersen/Wikimedia CC BY ; Demoiselle : Gilles San Martin/Wikimedia CC BY-SA ; Seiche : Amada44/Wikimedia CC BY-SA ; Hanneton : Josve05a/Wikimedia CC BY-SA ; Morpho : Didier Descouens/Muséum de Toulouse/Wikimedia CC BY-SA ; Colibri : Sharp Photography/Wikimedia CC BY-SA ; Carabe : Michael K. Oliver/Wikimedia CC BY-SA
Conclusion : la coloration diffère de la pigmentation, elle provient d’une interaction entre pigment et structure du tissu
La coloration d’un organisme définit donc l’ensemble des facteurs physiques et chimiques qui produisent une couleur avec (i) l’arrivée de certaines longueurs d’ondes sur un tissu, (ii) le renvoi par celui-ci de tout ou partie de ces longueurs d’onde vers l’œil suite à des processus structuraux et/ou pigmentaires ; et (iii) la transformation, par l’œil puis par le cerveau, d’un signal physique en une perception de couleur, propre à chacun.
La pigmentation (ou coloration chimique) est un terme plus spécifique qui caractérise le rôle joué par les pigments dans l’obtention d’une couleur. On note que celle-ci n’est pas générée par les pigments seuls, mais que ces derniers agissent de concert avec la structure des tissus : le rendu d’une couleur vive requiert leur interaction physique proche avec un tissu sous-jacent qui est lui, réfléchissant. À l’échelle de l’organisme, le terme de pigmentation est donc généralement impropre puisqu’il y a quasiment toujours l’intervention physique (par réflexion) du tissu sous-jacent. De plus, la couleur perçue peut être due à une interaction entre ces pigments chimiques et des processus purement physiques dus à à la structure des tissus. Par exemple, dans les plumes oranges de certains Oiseaux, la couleur résulte de pigments absorbant la lumière (les caroténoïdes) et de la structure de la plume qui réfléchit la lumière et la rend plus vive (Shawkey and Hill 2005). Enfin, certaines cellules d’abord décrites comme pigmentaires se sont en fait révélées contenir des molécules qui induisent une couleur d’origine physique, c’est-à-dire sans absorption de la lumière par un pigment : c’est le cas des cristaux de purines au sein de cellules spécialisées de certains Vertébrés, les iridophores.
Dans les faits, la distinction entre couleurs d’origine chimique (pigmentaire) et physique (structurelle) est généralement impossible à faire chez les organismes vivants. Les deux processus agissent de concert pour produire la couleur d’un organisme, bien que l’un puisse être prédominant par rapport à l’autre. Nous verrons ainsi que la coloration des Mammifères met généralement en œuvre des pigments : le terme de pigmentation est donc souvent employé comme un synonyme de coloration. Dans d’autres lignées, comme chez les Oiseaux ou chez les Insectes, s’ajoutent aux pigments des structures tissulaires très diverses produisant de la diffusion (à l’origine du bleu, de l’iridescence, etc.) : l’emploi du terme coloration est donc plus indiqué (McGraw and Hill, 2006 ; D’Alba et al., 2012).
Les couleurs d’origine chimique sont en réalité dues à une interaction physico-chimique : l’absorption par les pigments et la réflexion par le tissu sous-jacent. Les couleurs d’origine physique sont dues à la diffusion différentielle des longueurs d’onde de la lumière incidente par la structure des tissus.

Références
- Bagnara, J. T., Fernandez, P. J. & Fujii, R. On the blue coloration of vertebrates. Pigment Cell Research 20, 14–26 (2007).
- Burresi, M. et al. Bright-White Beetle Scales Optimise Multiple Scattering of Light. Scientific Reports 4, (2015).
- Cai, T. et al. Reconstruction of Dynamic and Reversible Color Change using Reflectin Protein. Scientific Reports 9, (2019).
- D’Alba, L., Kieffer, L., & Shawkey, M. D. Relative contributions of pigments and biophotonic nanostructures to natural color production: a case study in budgerigar (Melopsittacus undulatus) feathers. Journal of Experimental Biology 215, 1272-1277 (2012).
- Futahashi, R., Kurita, R., Mano, H. & Fukatsu, T. Redox alters yellow dragonflies into red. Proceedings of the National Academy of Sciences 109, 12626–12631 (2012).
- Gracheva, E., Ingolia, N., Kelly, Y. et al. Molecular basis of infrared detection by snakes. Nature 464, 1006–1011 (2010).
- Greenewalt, C. H., Brandt, W. & Friel, D. D. Iridescent Colors of Hummingbird Feathers. Journal of the Optical Society of America 50, 1005 (1960).
- Linzen, B. The Tryptophan → Ommochrome Pathway in Insects. in Advances in Insect Physiology (eds. Treherne, J. E., Berridge, M. J. & Wigglesworth, V. B.) vol. 10 117–246 (Elsevier, 1974).
- Mäthger, L. M. et al. Bright White Scattering from Protein Spheres in Color Changing, Flexible Cuttlefish Skin. Advanced Functional Materials 23, 3980–3989 (2013).
- McGRAW, K. J., & Hill, G. E. Mechanics of carotenoid-based coloration. Bird coloration 1, 177-242 (2006).
- Needham, A. E. The significance of zoochromes. vol. 3 (Springer-Verlag, 1974).
- Parker, A. R. & McKenzie, D. R. The cause of 50 million-year-old colour. Proceedings of the Royal Society of London. Series B: Biological Sciences 270, (2003).
- Prum, R. O. & Torres, R. Structural colouration of mammalian skin: convergent evolution of coherently scattering dermal collagen arrays. Journal of Experimental Biology 207, 2157–2172 (2004).
- Prum, R. O., Cole, J. A. & Torres, R. H. Blue integumentary structural colours in dragonflies (Odonata) are not produced by incoherent Tyndall scattering. Journal of Experimental Biology 207, 3999–4009 (2004).
- Prum, R. O., Quinn, T. & Torres, R. Anatomically diverse butterfly scales all produce structural colours by coherent scattering. Journal of Experimental Biology 209, 748–765 (2006).
- Seago, A. E., Brady, P., Vigneron, J.-P. & Schultz, T. D. Gold bugs and beyond: a review of iridescence and structural colour mechanisms in beetles (Coleoptera). Journal of The Royal Society Interface 6, (2009).
- Tisch, D., & Schmoll, M. Light regulation of metabolic pathways in fungi. Applied microbiology and biotechnology 85, 1259-1277 (2010).
- Shawkey, M. D., & Hill, G. E. Carotenoids need structural colours to shine. Biology Letters 1, 121-124 (2005).
- Yin, H. et al. Amorphous diamond-structured photonic crystal in the feather barbs of the scarlet macaw. Proceedings of the National Academy of Sciences 109, 10798–10801 (2012).