Il n’existe actuellement aucun traitement curatif pour les diabètes. Les recherches sur le sujet sont très actives et de nombreux espoirs reposent sur un phénomène connu depuis quelques années : la capacité du pancréas à générer de nouvelles cellules β, productrices d’insuline. Récemment, une équipe du centre de recherche Saint-Antoine à Paris a réussi à identifier des facteurs circulants responsables de la mise en place de ces cellules β, ce qui ouvre la voie au développement d’une thérapie régénératrice.
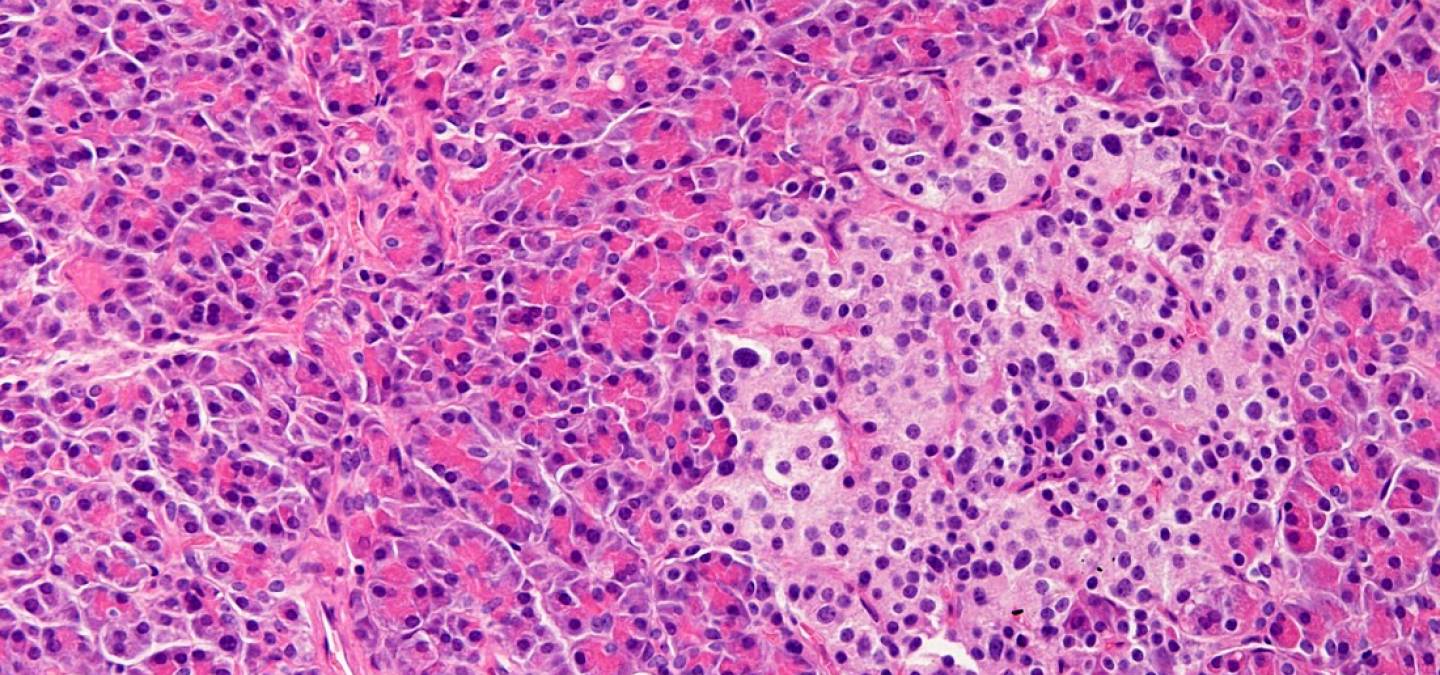
La régulation de la glycémie est notamment assurée par des hormones sécrétées par le pancréas. Ces molécules sont synthétisées par des cellules spécialisées contenues dans les îlots de Langerhans. Les cellules α, situées en périphérie, sécrètent du glucagon, une hormone hyperglycémiante, tandis que les cellules β, situées au centre des îlots, sécrètent de l’insuline, une hormone hypoglycémiante. Lorsque la glycémie s’élève, les cellules β libèrent de l’insuline qui agit sur des cellules cibles, principalement situées dans les muscles squelettiques, le foie et le tissu adipeux. L’insuline y favorise le stockage ou l’utilisation du glucose. Ce mécanisme permet un retour à une glycémie comprise entre 0,7 et 1,1 g/L.
La régulation de la glycémie est altérée chez les personnes vivant avec un diabète : elles présentent, en l’absence de traitement, un état d’hyperglycémie chronique. Le diabète de type 1 est causé par une perte des cellules β, tandis que celui de type 2 s’explique par une insulinorésistance, c’est-à-dire une résistance des cellules cibles à l’insuline. Dans les débuts du diabète de type 2, l’insulinorésistance est compensée par la sécrétion accrue d’insuline par le pancréas. L’imagerie en deux dimensions a montré que cette adaptation est liée à une prolifération des cellules β.
Récemment, ce phénomène a pu être confirmé par une équipe du centre de recherche Saint-Antoine grâce à l’utilisation de l’imagerie en trois dimensions qui permet d’analyser le pancréas dans sa totalité et de palier aux limites, principalement liées aux biais d’échantillonnage, de l’observation en deux dimensions 1.
Chez des souris insulinorésistantes, la clarification du pancréas et l’immunomarquage de l’insuline ont permis de confirmer l’existence d’un lien entre développement d’une insulinorésistance et adaptation pancréatique : une insulinorésistance légère s’accompagne d’abord d’une augmentation de la sécrétion d’insuline par les cellules β des îlots de Langerhans (Figure 1). Une insulinorésistance plus importante provoque ensuite une augmentation de la masse des cellules β du fait de leur prolifération ainsi qu’une augmentation de la densité d’îlots de Langerhans. Des expériences complémentaires ont mis en évidence que ce phénomène se produit aussi bien chez des souris jeunes que chez des souris âgées.
A. La concentration en insuline dans le sérum de souris présentant une insulinorésistance croissante suite à un traitement aux glucocorticoïdes est bien plus élevée que chez les souris témoin.
B-D. La masse de cellules β, leur abondance par rapport aux autres types cellulaires, ainsi que la densité des îlots de Langerhans sont toutes les trois plus élevées chez des souris présentant une insulinorésistance modérée (++) à sévère (+++) que chez des souris témoins.
Une légère insulinorésistance (+) provoque une augmentation de la sécrétion d’insuline, sans modification de la masse ou du pourcentage des cellules β, ni augmentation de la densité des îlots.
Graphique produit d'après les données de 1.
De précédents travaux avaient montré que la prolifération des cellules β s’effectue sous l’action de facteurs circulants présents dans le sérum de souris insulinorésistantes. Sachant que les muscles squelettiques sont très sensibles à l’insuline et qu’ils possèdent des fonctions endocrine et paracrine, les chercheurs ont supposé qu’ils pouvaient être à l’origine de la sécrétion de ces facteurs. Des expériences ont alors été menées in vitro afin de vérifier si des cellules musculaires insulinorésistantes étaient capables de déclencher une adaptation pancréatique. Les résultats ont montré que lorsqu’un milieu de culture provenant de myotubes ayant développé une insulinorésistance est mis en contact avec des bourgeons pancréatiques, la quantité de cellules β dans ces bourgeons augmente, de même que l’expression de gènes impliqués dans la différenciation de ces cellules, confirmant l’hypothèse formulée.
Afin d’identifier les molécules assurant la communication entre les cellules musculaires et pancréatiques, les transcriptomes de myotubes et de tissus musculaires squelettiques rendus insulinorésistants ont été analysés et comparés au transcriptome de témoins. Cela a permis de constater la surexpression de quatre gènes codant des myokines : Mstn, codant la myostatine, et BMP6, codant la protéine morphogénétique osseuse (Bone Morphogenetic Protein 6), surexprimés dans les myotubes et les tissus musculaires squelettiques, le gène AREG, codant l’amphiréguline, surexprimé dans le tissu musculaire squelettique et enfin EREG, codant l’épiréguline, surexprimé uniquement dans les myotubes.
Des bourgeons pancréatiques sont exposés aux protéines BMP6, MSTN, AREG ou EREG ou à aucune protéine dans le témoin (CTL). Le pourcentage de cellules pancréatiques exprimant de l’insuline est ensuite mesuré après 7 et 14 jours. Seules les protéines MSTN, AREG et EREG provoquent une différenciation des cellules β dans le pancréas.
La recherche des voies de signalisation suractivées dans les canaux pancréatiques ainsi que l’utilisation de protéines MSTN, BMP6, AREG et EREG recombinantes ont permis de conclure que la myostatine et l’épiréguline stimulent la différenciation des cellules β tandis que AREG favorisent d’abord la prolifération et ensuite la différenciation de ces cellules (Figure 2). Ces protéines sont ainsi, au moins en partie, responsables de l’adaptation pancréatique.
Ces résultats obtenus in vitro sur des cellules murines doivent maintenant être confirmées sur des cellules humaines ainsi qu’in vivo. La découverte de protéines sécrétées provoquant la mise en place de cellules β sécrétrices d’insuline constitue un réel espoir dans la mise en place d’une thérapie régénératrice qui permettrait de faire face au manque d’insuline et de mieux gérer le diabète et ses conséquences.