Les télomères sont des régions hautement répétitives de l'ADN, située à l'extrémité de chaque chromosome. Après l'historique de leur découverte, l'article décrit leur structure moléculaire particulière, permettant à la cellule de les différencier de simples cassures d'ADN double brin. Il montre comment leur réplication entraîne leur diminution de longueur à chaque division et en quoi la télomérase s'oppose à ce processus de raccourcissement. L'article montre ensuite, chez les pluricellulaires, en quoi l'absence d'activité télomérasique entraîne la sénescence et termine en expliquant pourquoi il n'est pas envisageable d'utiliser la télomérase comme molécule anti-vieillissement.
Introduction
La cellule, unité fonctionnelle minimale du vivant, est un système complexe de mécanismes qui interagissent pour mener à bien l’ensemble des fonctions cellulaires. Au cœur de la cellule, les chromosomes forment l’encyclopédie contenant toutes les informations nécessaires. Ils portent une information précieuse qui doit à la fois être lue et utilisée par la cellule, mais aussi protégée pour être transmise à l’identique à la descendance. Pourtant, l’ADN portant cette information est en permanence soumis à des stress, sources de dommages de nature variée sur l’ADN, notamment des cassures.
De nombreux mécanismes existent dans les cellules afin de réparer le plus fidèlement possible ces dommages et ainsi conserver intacte l’information génétique. Il est alors surprenant d’observer chez les organismes Eucaryotes, ainsi que certains Procaryotes, l’existence de structures naturelles qui s’apparentent au premier abord à des cassures dans l’ADN. En effet, les chromosomes linéaires, de par leur linéarité même, possèdent des extrémités d’ADN. Ces régions, appelées télomères, sont spécialisées afin de ne pas être reconnues ni réparées comme des dommages à l’ADN. Elles permettent ainsi de protéger les chromosomes linéaires contre des fusions par leurs extrémités et d’empêcher la dégradation des séquences internes. Cependant, bien qu’ils soient distincts d’une cassure, de nombreux mécanismes impliqués dans la reconnaissance et le traitement des dommages à l’ADN sont aussi présents aux télomères.
De par leur structure particulière, les télomères requièrent d’être maintenus par une transcriptase inverse cellulaire spécifique appelée télomérase. En absence de télomérase, les télomères raccourcissent progressivement, jusqu’à atteindre une taille critique qui entraîne un arrêt des divisions cellulaires : c’est la sénescence réplicative. Au cours du processus menant à l’arrêt des divisions, les télomères subissent de nombreux changements, notamment vis-à-vis des mécanismes de réponse aux dommages. Ainsi, les télomères forment une structure essentielle dans le contrôle de la viabilité cellulaire. Ils permettent de maintenir l’équilibre entre le vieillissement cellulaire et le risque de prolifération cellulaire incontrôlée associée aux cancers.
Découverte des télomères
Les dommages à l’ADN sont des évènements fréquents dans la vie d’une cellule, et de nombreux mécanismes spécialisés sont mis en place afin de tolérer et réparer fidèlement ces dommages. Pourtant, alors que les cassures double-brin, qui créent des extrémités nouvelles, sont très délétères pour la cellule et sont corrigées efficacement, certaines bactéries (Borrelia, A. tumefaciens), certains phages (T7, λ) et tous les Eucaryotes investigués possèdent des chromosomes linéaires. Ces chromosomes linéaires présentent deux extrémités naturelles, qui ne sont pas traitées comme des cassures.
La nécessité d’une extrémité spécifique
C’est dans les années 1930, alors même que la nature ADN des chromosomes n’est pas encore connue, que Hermann Muller et Barbara McClintock apportent les premières informations sur l’existence d’extrémités particulières aux chromosomes. En 1939, par des études cytologiques, McClintock montre qu’une extrémité issue de la cassure d’un chromosome, à l’inverse des extrémités « naturelles », est instable et subit de multiples cycles de réparation et cassure avant d’être stabilisée. En 1938, Muller observe, chez les mouches, que les extrémités naturelles des chromosomes ne se lient pas entre elles ou avec des extrémités issues de cassures, contrairement à ces extrémités issues de cassures qui peuvent se lier entre elles. Ainsi, il existe une structure particulière au niveau des extrémités naturelles des chromosomes qui permet à ces extrémités d’être reconnues différemment d’une cassure. Muller nomme cette structure «télomère», du grec τέλος, télos («fin») et μέρος, meros («partie») (Blackburn, 2006 ; McClintock, 1939).
En plus de cet effet de protection des extrémités, la compréhension du mécanisme de réplication de l’ADN a permis à James Watson, en 1972, et Alekseï Olovnikov, en 1973, de mettre en évidence l’existence d’un problème de réplication des extrémités, suggérant que la réplication est incomplète aux extrémités du fait de la nécessité d’une matrice ARN et de la structure de la polymérase (Blackburn, 2006 ; Olovnikov, 1973 ; Watson, 1972).
L’identification des télomères
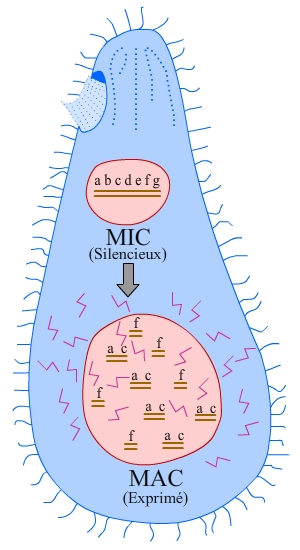
L'état végétatif du protozoaire cilié Tetrahymena présente un macronoyau très actif (MAC).
Ce macronoyau contient environ 50 copies de chacun des innombrables minichromosomes qui dérivent de la conjugaison sexuelle, par réarrangements et amplification de séquences provenant du micronoyau silencieux (MIC).
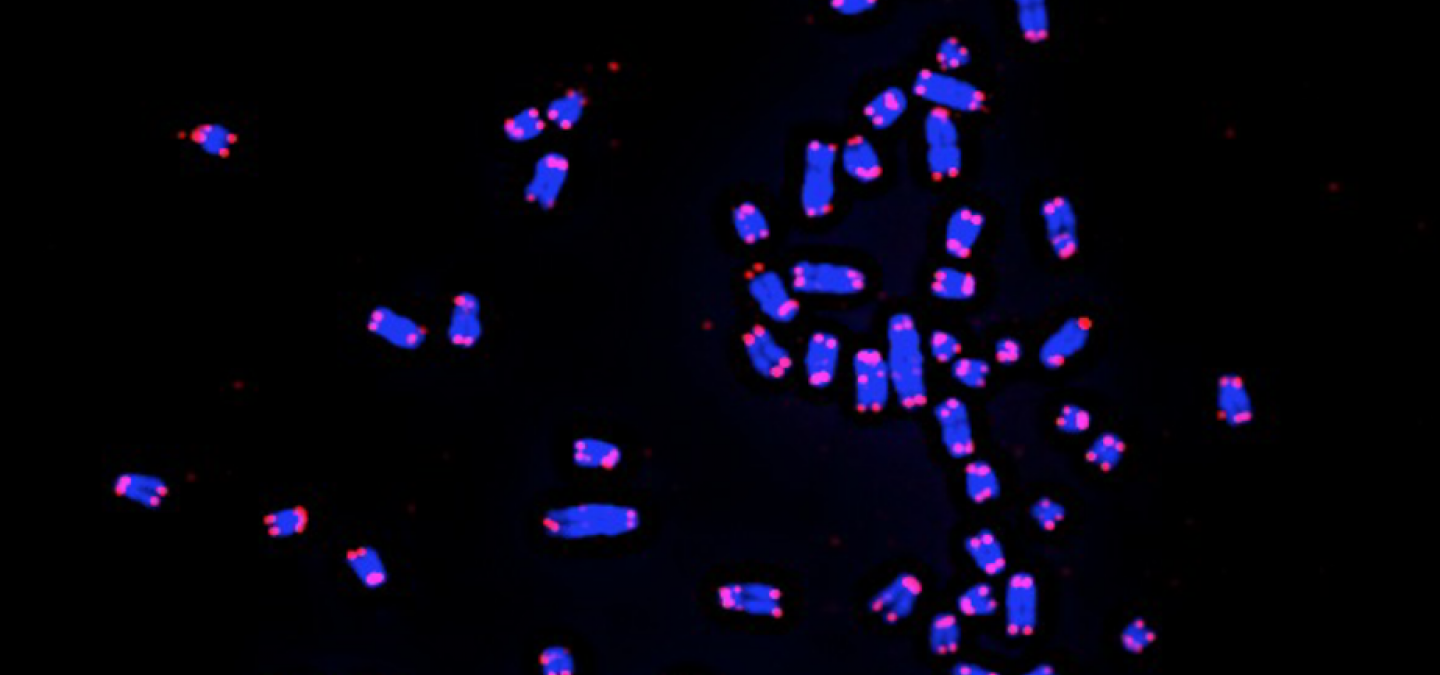
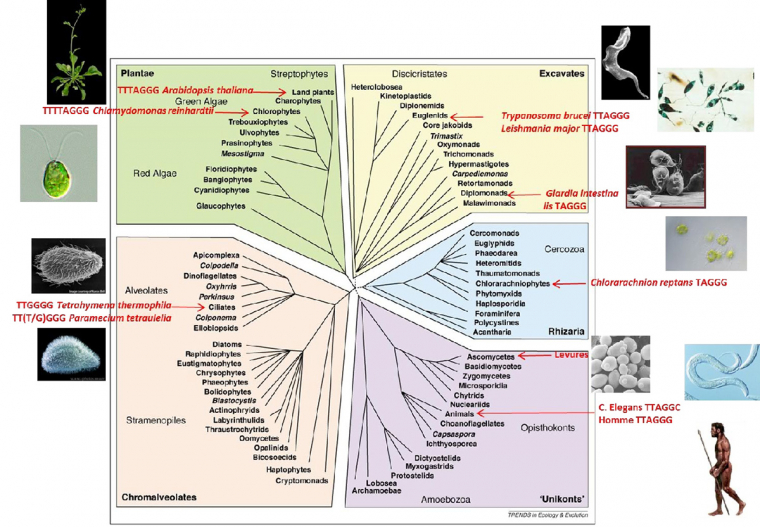
Face à ces deux problèmes concomitants de protection et de réplication des extrémités, de nombreuses structures possibles des télomères ont été proposées, notamment l’existence d’une structure terminale en épingle. En 1978, face à cette interrogation, Liz Blackburn a cherché à déterminer la séquence des télomères. Pour cela, elle a utilisé un protozoaire cilié, Tetrahymena thermophila, qui présente la particularité de posséder plusieurs milliers de molécules linéaires d’ADN ribosomique (Fig. 1), dont elle a pu isoler et séquencer les extrémités. Elle a ainsi montré que leurs extrémités contiennent entre 20 et 70 répétitions GGGGTT sur le brin se terminant par l’extrémité 3’-OH et présentent des régions simple brin (Blackburn & Gall, 1978). Ces séquences, insérées aux extrémités d’un plasmide linéaire, permettent la stabilisation de celui-ci chez Saccharomyces cerevisiae, ce qui montre une grande conservation de séquence des télomères entre espèces. La décennie suivante permit l’identification des séquences télomériques dans de nombreux autres organismes (Fig. 2, Fig. 3 et Fig. 4), à commencer par la levure S. cerevisiae, qui possède des répétitions TG1-3 dégénérées (un T suivi de 1 à 3 G) et aussi des régions simple brin.
Dès le début, il est observé que le nombre de répétitions télomériques est variable. Shampay et Blackburn montrent en 1988 que cette hétérogénéité de taille au niveau d’un télomère unique augmente avec le nombre de réplications (Shampay & Blackburn, 1988). Ce résultat leur permet de proposer le modèle d’un équilibre entre des activités de raccourcissement et d’élongation à chaque télomère, aboutissant progressivement à une augmentation de l’hétérogénéité de taille. En effet, S. cerevisiae peut perdre l’activité d’élongation des télomères, ce qui conduit à un raccourcissement progressif de ceux-ci jusqu’à un arrêt des divisions cellulaires, et le même phénomène est observé dans des fibroblastes humains normaux.
Ainsi, les télomères sont les extrémités des chromosomes linéaires, qui résolvent les problèmes de protection et de réplication des extrémités, grâce à leur structure et à leur maintenance spécifique.
Des régions spécifiques et spécialisées
Les extrémités des chromosomes sont ainsi des régions bien particulières qui présentent des séquences d’ADN qui leur sont propres. Elles sont également associées à des protéines spécifiques. Il est important de comprendre l’ensemble de ces caractéristiques pour mieux appréhender la distinction entre télomère et cassure double brin.
Une séquence nucléique particulière
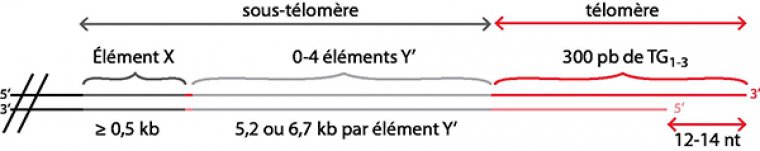
Étonnamment, n’étant pas une région codante, la séquence nucléique et la structure des télomères sont très conservées chez les Eucaryotes (Fig. 2). En effet, les télomères sont le plus souvent constitués de petites répétitions riches en G sur le brin d’ADN se terminant par une extrémité 3’ simple brin, mais de longueurs pouvant varier de quelques dizaines de nucléotides à plusieurs dizaines de milliers de nucléotides selon l’organisme (voir Fig. 3). Au sein d’une population cellulaire, la taille d’un télomère présente une hétérogénéité liée à son mode d’élongation (voir ci-après). Chez S. cerevisiae, les télomères ont la particularité d’être constitués d’environ 300 nucléotides de répétitions dégénérées, sous forme d’une thymine suivie d’une à trois guanines. Ils se terminent par un simple brin 3’ sortant de 12 à 14 nucléotides, qui peut augmenter jusqu’à plusieurs dizaines de nucléotides au cours de la phase S (Fig. 2).
Organisation des séquences ADN des télomères et régions sous-télomériques de S. cerevisiae
D'après Gilson & Geli, 2007 ; Wellinger & Zakian, 2012.
| Type de télomère | Nature des répétitions | Longueur du télomère | |
| Saccharomyces cerevisiae (levure de bière) |
Répétitions riches en G | TG1-3 | 300 à 400 pb |
| Schizosaccharomyces pombe (levure) |
Répétitions riches en G | TTAC(A)(C)G2-8 | 300 pb |
| Caenorhabiditis elegans | Répétitions riches en G | TTAGGC | 4-9 kb |
| Danio rerio (poisson zèbre) |
Répétitions riches en G | TTAGGG | Adulte, deux populations: 6 et 16 kb |
| Mus musculus (souris grise) |
Répétitions riches en G | TTAGGG | Jusqu'à 150 kb |
| Homo sapiens (Homme) |
Répétitions riches en G | TTAGGG | A la naissance: 10 kb |
| Arabidopsis thaliana | Répétitions riches en G | TTTAGGG | 2-9 kb |
| Chlamydomonas reinhardtii | Répétitions riches en G | TTTTAGGG | ND |
| Tetrahymena thermophila | Répétitions riches en G | GGGGTT | macronoyau: 250 à 350pb, micronoyau: 2 à 3,4 kb |
| Drosophila melanogaster (mouche du vinaigre) |
Rétrotransposons | Het-A et TART | 20 kb |
| Borrelia burgdorferi | Boucle en épingle terminale | ||
| La nature et la longueur des télomères dans différents organismes sont indiquées. ND : non déterminé. D’après de Lange et al, 2006; Henriques et al, 2013; Wicky et al, 1996. |
|||
Les séquences télomériques de quelques espèces sont présentées sur un arbre phylogénétique.
Du fait de leur richesse en guanine, les répétitions télomériques sont capables, in vitro, de former des structures secondaires au simple brin, appelées G-quadruplex. Cependant, ces structures n’ont été observées in vivo que dans le macronoyau du cilié Stylonychia lemnae, à l’aide d’un anticorps ciblant les G-quadruplex, et leur rôle n’est pas connu.
En amont des télomères, les chromosomes possèdent une région appelée sous-télomère, constituée de séquences répétées plus longues, hétérogènes et variables selon le télomère. Chez S. cerevisiae, tous les sous-télomères possèdent un élément X, suivi de 0 à 4 répétitions d’un élément Y’ (Fig. 2). Ces éléments Y’ sont présents sur plus de la moitié des sous-télomères. Bien qu’ils soient présents à tous les télomères, les sous-télomères ne sont pas essentiels pour la viabilité des cellules. Ces régions contiennent des origines de réplication potentielles ainsi que de petites répétitions TTAGGG, ce qui correspond à la séquence télomérique chez les Vertébrés. Les éléments Y’ codent aussi pour une hélicase, Y’-Help1. De plus, chez S. cerevisiae comme chez S. pombe et l’humain, les télomères peuvent être transcrits à partir du sous-télomère. La fonction de ces ARN télomériques, appelés TERRA, est encore peu connue. D’autre part, les télomères sont localisés de préférence à la périphérie du noyau.
Cette structure des télomères n’est cependant pas universelle (voir Fig. 3 et Fig. 4). Ainsi, Arabidopsis thaliana possède des télomères avec un simple brin sortant, mais aussi des télomères se terminant par une extrémité franche. Chez la drosophile, les télomères sont constitués de séquences alternées de rétrotransposons non-LTR HeT-A et TART. Chez la plupart des bactéries, le problème des extrémités d’ADN est évité grâce à leur chromosome circulaire, mais certaines ont des chromosomes linéaires, avec des télomères très différents de ceux des Eucaryotes. Ainsi, Borrelia burgdorferi, qui cause la maladie de Lyme, possède de petites répétitions imparfaites inversées au niveau de ses télomères, qui forment des boucles en épingles liées de manière covalente.
Une séquence particulière associée à des protéines spécifiques.
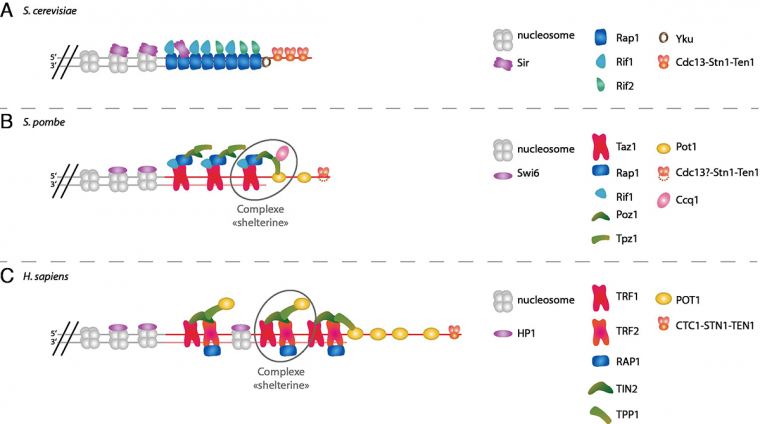
Un télomère n’est pourtant pas seulement une séquence d’ADN particulière. Comme le reste du chromosome, cet ADN est associé à des protéines spécialisées dont la perte entraîne une instabilité télomérique. Ces protéines télomériques présentent une grande diversité entre les organismes (Fig. 5). Certaines de ces protéines sont associées à la région double brin du télomère, d’autres à la région simple brin, et leur interaction forme un complexe appelé « shelterine » chez l’Homme, essentiel pour la protection et la maintenance des extrémités télomériques.
Principales protéines associées aux télomères chez deux espèces de levure et l'homme :
(A) S. cerevisiae, (B) S. pombe, et (C) H. sapiens.
Les couleurs similaires indiquent les protéines dont la séquence primaire est conservée entre espèces.
Protéines du double brin télomérique
Chez la levure S. cerevisiae, les télomères sont exempts de nucléosomes. Initialement identifiée comme un régulateur de l’expression génique, Rap1 y est la principale protéine liée aux répétitions télomériques double brin. Rap1 est capable de se lier à des sites spécifiques d’ADN double brin, avec une grande affinité pour ses sites télomériques. On estime qu’une molécule de Rap1 est liée à environ 18 pb, soit 15 à 20 Rap1 pour un télomère de taille moyenne. Rap1 est aussi associée aux promoteurs d’environ 5 % des gènes. Cette protéine essentielle est impliquée à la fois dans le contrôle de la taille des télomères et dans l’effet de position télomérique via ses partenaires, tout en étant un facteur de transcription de nombreux gènes.
Rif1 et Rif2 s’associent à Rap1 et permettent le contrôle de la longueur des télomères. Alors que la liaison de Rap1 sur chaque site télomérique se fait indépendamment des sites voisins, l’analyse structurale de ces protéines montre que l’interaction de Rif1 et Rif2 avec Rap1 forme un velcro moléculaire qui associe entre elles les protéines du double brin d’un même télomère.
L’effet de position télomérique est un mécanisme de répression transcriptionnelle par l’hétérochromatine des gènes situés dans les régions sous-télomériques. Cet effet dépend de la liaison sur Rap1 d’autres protéines que Rif1 et Rif2. Ainsi, le complexe Sir2/Sir3/Sir4 permet la propagation de l’hétérochromatine dans les sous-télomères. Rif1 et Rif2 inhibent de manière additive cet effet de position télomérique, probablement parce qu’ils partagent le même site de liaison à Rap1 que Sir3. Le complexe Yku est, lui aussi, associé aux télomères et requis pour leur équilibre fonctionnel.
Rap1 est retrouvée dans d’autres organismes, mais sa fonction de liaison à l’ADN n’est pas conservée. Au contraire, elle interagit avec les protéines télomériques de ces organismes, tel Taz1 chez S. pombe. TRF1 et TRF2, les orthologues de Taz1 chez les Mammifères, forment un complexe de protection des télomères, le complexe « shelterine », en interagissant avec les 4 autres protéines télomériques, dont Rap1. Ces télomères, beaucoup plus longs, sont aussi couverts par des nucléosomes.
Protéines du simple brin télomérique
Chez S. cerevisiae, l’ADN simple brin 3’ sortant terminal du télomère est lié par la protéine Cdc13. Cette protéine, capable de se lier spécifiquement à l’ADN simple brin avec un site de liaison de 11 nt de long, est impliquée à la fois dans la protection des extrémités et dans le contrôle de l’élongation des télomères. Son association avec les télomères varie au cours du cycle, et elle est maximale en fin de phase S, au moment où la quantité de simple brin est maximale. Cette protéine est essentielle, mais le mutant ponctuel de perte de fonction cdc13-1 accumule très rapidement plusieurs kilobases d’ADN simple brin 3’ terminal, jusque dans les régions sous-télomériques, ce qui montre le rôle essentiel de cette protéine dans la protection des extrémités contre la dégradation.
Les protéines Stn1 et Ten1 sont importantes pour la protection des télomères dans la voie Cdc13, en formant un complexe avec cette dernière. Stn1 et Ten1 sont aussi capables de se lier elles-mêmes à l’ADN simple brin télomérique, et leur surexpression permet de sauver la perte de Cdc13.
Chez les Mammifères et les plantes, STN1, TEN1 et CTC1, l’orthologue de Cdc13, n’ont été impliquées dans la protection des télomères que récemment. Contrairement à Cdc13, CTC1/AAF, initialement identifiée comme un facteur accessoire de la Pol alpha-primase (une primase est une enzyme responsable de la synthèse de l’amorce ARN nécessaire à l’initiation de la réplication), favorise la réplication aux télomères avec l’aide de STN1 et TEN1, mais aussi dans le reste du génome. S. pombe possède aussi Stn1 et Ten1, qui sont associées aux télomères, mais aucun homologue de Cdc13 ou CTC1 n’ayant été identifié, elles y sont peut-être recrutées par un mécanisme différent.
Chez S. pombe et les Mammifères, c’est une autre protéine, POT1, qui est principalement impliquée dans la protection du simple brin télomérique, et a longtemps été considérée comme l’homologue fonctionnel de Cdc13. POT1 fait partie du complexe shelterine et est associée à l’ADN simple brin. Les interactions entre les différentes protéines de ce complexe permettent de créer un pont entre l’ADN simple et double brin télomérique.
Protéines des régions sous-télomériques
Au contraire des télomères, les régions sous-télomériques de S. cerevisiae sont couvertes par les nucléosomes, dont les histones peuvent être modifiées. Les protéines Sir, responsables de l’effet de position télomérique par formation d’hétérochromatine, sont retrouvées jusqu’à plusieurs kilobases en amont des télomères. Il est intéressant de noter que certains organismes utilisent cet effet de position télomérique pour réguler l’expression de certains gènes. C’est le cas de Plasmodium falciparum, un agent du paludisme, qui contrôle ainsi l’expression des gènes impliqués dans la variation antigénique.
D’après Gilson & Geli, 2007 ; Giraud-Panis et al, 2010 ; Moser & Nakamura, 2009.
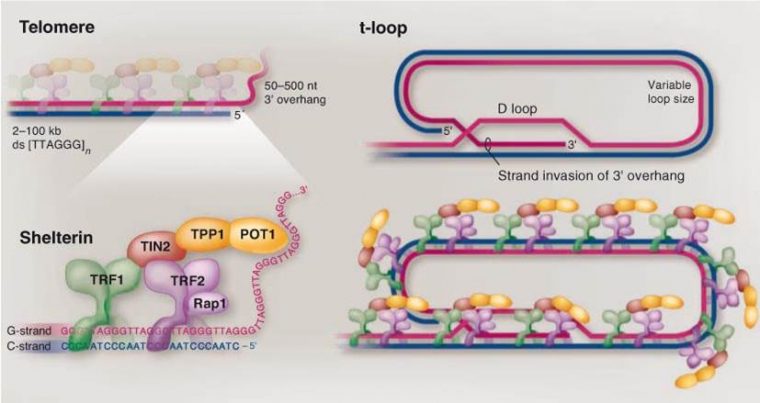
Chez les Mammifères, la région simple brin télomérique est capable d’envahir les régions double brin du même télomère par une boucle en D favorisée par les protéines shelterines (Fig. 6). Cette structure, qui a été observée par microscopie électronique, est appelée « t-loop » et est proposée comme un mode supplémentaire de protection des télomères.
D'après Titia de Lange, Science, 2009.
Il existe donc un réseau complexe de protéines télomériques, plus ou moins spécifiques des extrémités, associées à des séquences nucléiques spécialisées. Ce complexe nucléoprotéique définit l’identité unique des extrémités naturelles d’ADN.
Un télomère n’est pas une cassure double brin
Une identité télomérique
L’identité définie par le système nucléoprotéique télomérique permet à la cellule de différencier un télomère d’une cassure double brin. En effet, la perte d’un unique télomère par coupure double brin expérimentale (par une endonucléase dite HO), sur un chromosome non-essentiel, entraîne un arrêt du cycle cellulaire et une forte perte de la viabilité des cellules. Cependant, si des répétitions télomériques sont placées artificiellement au niveau de ce site de coupure HO, elles permettent de restaurer la viabilité des cellules. Cet effet est en accord avec les observations initiales de Barbara McClintock qui montraient l’existence de deux types d’extrémités, stables ou instables, qui correspondent respectivement aux télomères et aux cassures double brin (McClintock, 1939).
Ainsi, la présence de séquences télomériques au niveau d’une extrémité permet la mise en place de sa reconnaissance comme une extrémité naturelle et non délétère pour la cellule.
Des protéines qui protègent le télomère
L’une des fonctions majeures nécessitant l’existence des télomères est donc la protection des extrémités naturelles, fonction qui est déclenchée par la présence de séquences répétées spécifiques.
Les protéines télomériques, recrutées sur ces régions, sont cruciales pour l’accomplissement de ce rôle. Elles sont aussi capables d’empêcher l’activation de la voie de signalisation des dommages aux télomères à plusieurs niveaux, et bien que certaines protéines de réponse aux dommages, comme Tel1, soient présentes aux télomères, les protéines télomériques coopèrent pour empêcher la reconnaissance, la signalisation et la réparation du télomère comme une cassure double brin.
Maintenance des télomères
La réplication de ces régions répétées
Comme nous venons de le voir, les télomères sont des structures nucléoprotéiques très spécialisées, qui permettent de protéger les extrémités des chromosomes. Pourtant, leurs spécificités, si importantes pour la protection, rendent ces régions difficiles à répliquer.
Les spécificités de la réplication télomérique
Les télomères sont des régions très répétées, riches en GC, ce qui rend le double brin très stable (les bases G et C sont reliées par 3 liaisons hydrogène, alors que les bases A et T ne sont reliées que par 2 liaisons hydrogène), et ils possèdent le potentiel de former des G-quadruplex, structures secondaires impliquant au moins huit G et un cation, sources de difficultés de réplication et d’instabilité génétique. De plus, au sein du chromosome, si la réplication est bloquée au niveau d’une fourche de réplication, elle peut être sauvée par l’arrivée d’une seconde fourche provenant de la direction opposée, ce qui n’est pas possible aux télomères après la dernière origine de réplication.
Les régions télomériques font donc partie des régions du génome difficiles à répliquer, mais les cellules sont capables de gérer ces difficultés. Un problème se pose pourtant toujours lorsque la fourche de réplication atteint l’extrémité du télomère.
Le(s) problème(s) de réplication des extrémités
Ce problème de réplication des extrémités est dû à la fois à la structure télomérique et à la nature même de la réplication. Il conduit au raccourcissement progressif des télomères avec chaque réplication, et donc à chaque division cellulaire.
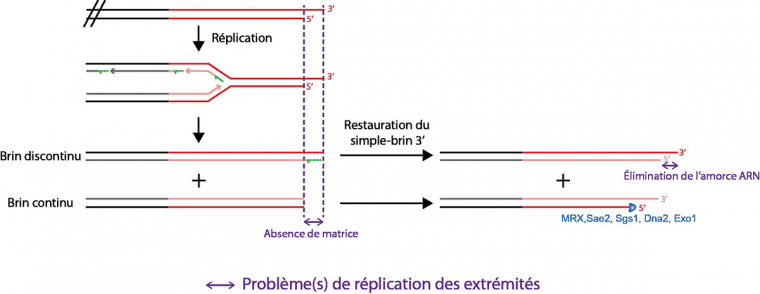
À chaque réplication, la présence d’un ADN simple brin 3’ sortant ainsi que l’élimination de la dernière amorce ARN entraînent la perte d’une petite séquence terminale des télomères. La synthèse du brin continu (qui utilise comme matrice le brin ayant son extrémité 5' au niveau de la fin du chromosome) peut se faire jusqu’à l’extrémité du brin matrice, mais il manque alors une extrémité 3' simple brin. Cette extrémité simple brin peut être restaurée en raccourcissant l’extrémité 5', au prix d’une diminution de la taille du télomère. Ce problème de réplication des extrémités est donc à l’origine du raccourcissement progressif des télomères.
La compréhension du mécanisme de réplication amène Alekseï Olovnikov à proposer, en 1973, une théorie de la « marginotomie », qu’il définit comme « la formation de répliques plus courtes que la matrice ». Il propose, d’une part, que la distance qui existe entre les extrémités d’une polymérase et sa région catalytique a pour résultat la présence aux extrémités d’ADN d’une région de l’ADN matrice non copiée par la polymérase, et d’autre part, que l’initiation de la réplication, qui nécessite l’utilisation d’une petite amorce ARN qui est ensuite dégradée, laisse une région non copiée (Olovnikov, 1973). Ces deux phénomènes ont lieu aux extrémités d’ADN, et sont donc source d’un raccourcissement des télomères lors de la réplication (Fig. 7).
À la même période, James Watson définit le problème de complétion (c’est-à-dire l’achèvement jusqu’au bout) de la réplication des extrémités sur l’ADN linéaire du phage T7, dû à la formation d’une queue d’ADN 3’ sortant, après l’élimination de la dernière amorce ARN. Il propose que cette formation de simple brin aux extrémités de l’ADN T7 expose des régions redondantes, qui peuvent s’associer entre elles et ainsi permettre la concaténation de plusieurs molécules de l’ADN T7, ce qui compense alors le problème de réplication des extrémités (Watson, 1972).
Aux extrémités, le problème de réplication est donc théoriquement lié au placement de la dernière amorce ARN au brin discontinu. Pourtant, la présence d’un simple brin télomérique 3’ sortant est la structure physiologique du télomère. L’élimination de la dernière amorce ARN permet le ré-établissement de la queue 3’ sortante au brin discontinu, et donc de la structure naturelle de ce télomère (Fig. 7). Par contre, le brin 5’ initial est plus court que le brin 3’, à cause de cette région simple brin. Le télomère issu de la réplication continue de ce brin 5’ est donc plus court que le télomère initial (il manque la partie 3' simple brin qui, n’ayant pas eu de matrice, n’a pas pu être synthétisée). Ainsi, le problème de réplication des télomères est révélé au niveau du brin continu, et résulte en un raccourcissement progressif des télomères avec chaque réplication (Fig. 7).
De par son mode de réplication, et à condition que les polymérases soient capables de copier une matrice ADN jusqu’à son extrémité, ce brin continu devrait posséder une extrémité franche. In vitro, la réplication d’un ADN linéaire à l’aide d’un extrait cellulaire humain semble confirmer que le brin continu est copié jusqu’à son extrémité. Il est donc nécessaire de rétablir le simple brin 3’ sortant au niveau du télomère issu de ce brin continu, ce qui renouvelle le même problème de réplication pour la duplication suivante (Fig. 7).
Le problème de réplication des extrémités télomériques provient donc à la fois de l’absence de matrice terminale sur le brin continu, ce qui conduit à une perte de séquence sur la chromatide-fille, et de la reconstitution après chaque réplication du simple brin terminal à l’origine de cette absence de matrice. Ce problème est alors recréé et transmis de génération en génération.
Une séquence simple brin à maintenir
Afin de rétablir la structure télomérique normale, qui définit le problème de réplication des extrémités télomériques, le simple brin télomérique 3’ doit donc être recréé après la réplication.
Chez S. cerevisiae, la formation de simple brin télomérique étendu observée en fin de phase S, qui contribue probablement à la restauration de cette structure, nécessite que la réplication ait eu lieu aux télomères. Les protéines impliquées dans la résection (digestion progressive de l’un des deux brins d’une molécule d’ADN) des cassures double brin semblent toutes impliquées dans la résection 5’-3’ des télomères, mais avec un mécanisme légèrement différent.
Pourtant, le problème de réplication du brin discontinu lié à l’existence d’une amorce ARN propose que le brin discontinu possède déjà une région simple brin 3’ après élimination de cette amorce, d’une taille compatible avec la longueur de la queue 3’ sortante observée aux télomères si cette amorce est placée à la fin de la séquence d’ADN. Le mécanisme d’élimination de cette amorce ARN n’est pas connu. Ceci suggère que l’extrémité franche du brin continu est le substrat principal de la résection télomérique.
En conclusion, la compréhension de la formation du simple brin télomérique met en évidence de nouvelles similarités de traitement entre une cassure double brin et un télomère, qui sont pourtant deux structures bien différenciées.
La ré-élongation des télomères par la télomérase
Les particularités de la structure des télomères, notamment leur extrémité simple brin maintenue, les rendent sujets à un problème de réplication qui les conduit à un raccourcissement graduel. En réponse à cette perte progressive de séquences télomériques, il existe un mécanisme spécifique permettant de rallonger les télomères.
La télomérase, une transcriptase inverse cellulaire
Très tôt après la caractérisation moléculaire des télomères, il a été montré que des extrémités télomériques de Tetrahymena insérées sur un plasmide linéaire chez S. cerevisiae sont allongées par des séquences télomériques de cette levure. Ceci implique l’existence d’une activité capable de rallonger spécifiquement les télomères. C. Greider et E. Blackburn mettent en évidence peu après, dans des extraits cellulaires de Tetrahymena, une activité de type « transférase terminale » capable d’ajouter des répétitions télomériques de Tetrahymena sur des petites amorces riches en T et G, qu’elles désignent sous le nom de télomérase (Greider & Blackburn, 1985 ; Greider & Blackburn, 1987). Cette activité dépend de la présence d’un ARN associé à la télomérase, qui contient une petite séquence complémentaire aux répétitions télomériques (Greider & Blackburn, 1987 ; Greider & Blackburn, 1989).
À la même période, V. Lundblad décrit chez S. cerevisiae un gène dont les mutants possèdent des télomères qui raccourcissent au fur et à mesure des divisions cellulaires, qu’elle nomme EST1, pour son phénotype « Ever Shorter Telomeres ». Ceci reflète le problème de réplication des extrémités et indique l’existence d’une activité nécessaire à la maintenance des télomères pour leur conserver une taille constante.
Trois autres mutants ont ensuite été caractérisés par leur phénotype similaire à celui de est1, et leur implication dans la même voie a été montrée par épistasie. Un crible génétique indépendant ayant pour but l’identification de gènes impliqués dans la répression transcriptionnelle aux télomères a permis d’identifier TLC1, qui code pour l’ARN de la télomérase chez S. cerevisiae, et dont le mutant possède le même phénotype de raccourcissement des télomères que est1. Cet ARN d’1,3 kilobases possède une séquence de 16 nucléotides complémentaire aux répétitions télomériques. L’ensemble de ces observations a pu être intégré dans une vue d’ensemble par l’identification de la sous-unité catalytique de la télomérase chez le cilié Euplotes aediculatus, qui est l’homologue de Est2. Ces deux protéines sont des transcriptases inverses, dont l’activité est nécessaire à la maintenance des télomères. Est2 et son activité transcriptase inverse sont nécessaires à l’activité de la télomérase in vitro, mais pas Est1, ni Est3, ni Cdc13. Les trois protéines Est1, Est2 et Est3, qui sont peu abondantes, forment avec TLC1 in vivo un complexe stable, qui possède l’activité télomérase.
La caractérisation de l’activité de la télomérase suggère que l’ARN de la télomérase s’associe par complémentarité avec l’extrémité 3’ du simple brin télomérique (le brin G), puis est utilisé comme matrice pour allonger ce brin (Fig. 8). La longueur de séquence ajoutée est très variable et l’action de la télomérase est régulée.
| Un fragment d'ARN appartenant à la polymérase sert de matrice pour permettre à l'activité catalytique de cette télomérase d'allonger le brin 3' sortant. La télomérase a donc une activité de transcriptase inverse. Ultérieurement, le brin 5' pourra être allongé à son tour par une ADN-polymérase en utilisant le brin 3' comme matrice. |
L’activité de la télomérase allonge uniquement le brin G (brin qui se termine au niveau du télomère par une extrémité 3' simple brin, voir Fig. 8), mais elle est couplée avec l’activité des polymérases alpha et delta qui vont allonger le brin C (brin qui se termine au niveau du télomère par une extrémité 5'), ce qui synchronise l’élongation des brins G et C. En revanche, l’ADN simple brin télomérique existe même en absence de télomérase, ce qui indique que la formation du simple brin télomérique est indépendante de l’élongation par la télomérase.
Une activité régulée
L’activité de la télomérase permet l’élongation des télomères, il est donc possible qu’elle agisse de manière différentielle selon la longueur des télomères. De fait, les études expérimentales ont montré que la télomérase allonge de préférence les télomères courts (Fig. 9). En effet, plus un télomère est court, plus sa vitesse d’élongation au cours des divisions est élevée. Ceci est dû à une augmentation de la fréquence d’action de la télomérase lorsque les télomères raccourcissent.
Le raccourcissement progressif des télomères, causé par le problème de réplication des extrémités, est contré par la télomérase qui rallonge préférentiellement les télomères les plus courts. En son absence, les télomères courts sont à l'origine de la sénescence réplicative.
Chez S. cerevisiae, plusieurs systèmes ont été développés pour obtenir des télomères artificiellement courts afin de répondre à cette question (Fig. 10). Un nombre variable de répétitions télomériques peut être placé au niveau d’un site de coupure HO, de façon à créer un télomère court ou de taille sauvage lors de l’induction de la coupure. Alternativement, un nombre variable de répétitions télomériques est placé avec un marqueur entre deux séquences FRT (séquence qui encadre une région soumise à une recombinaison), juste avant le télomère, ce qui fait varier la longueur des répétitions télomériques terminales. L’induction de la flipase (enzyme qui réalise la recombinaison) entraîne l’excision du cercle contenant ces séquences télomériques internes, et laisse un télomère plus court à l’extrémité.
Un nouveau télomère court peut être obtenu par insertion de séquences télomériques au niveau d'une coupure HO (A) ou par élimination de répétitions TG1-3 sous-télomériques (B). Les triangles représentent les répétitions télomériques.
Noir = télomère naturel, Rouge = télomère court artificiel, Vert = répétitions télomériques internes
D’après Diede & Gottschling, 1999 ; Marcand et al, 1999.
De plus, Est1 et Est2 sont recrutées préférentiellement à des télomères raccourcis artificiellement. Ce recrutement dépend de la présence et du recrutement au télomère de Tel1. Tel1 est ainsi recrutée préférentiellement aux télomères courts, en présence et en absence de télomérase. Ce recrutement dépend de son interaction avec le complexe MRX, qui est lui aussi aux télomères courts, et de Rif2. À l’inverse, la surexpression de Tel1 entraîne l’association de Tel1 avec tous les télomères, ce qui résulte en une augmentation de la taille moyenne des télomères. Par contre, le second point de contrôle cellulaire, Mec1, n’est pas requis pour le recrutement de la télomérase.
L’élongation d’un télomère raccourci artificiellement a lieu en fin de phase S et nécessite plusieurs cycles cellulaires avant qu’une longueur normale soit atteinte. Au niveau d’un télomère créé de novo au niveau d’une coupure HO, l’élongation dépend de la télomérase et peut avoir lieu en phase G2/M, mais pas en phase G1. En effet, l’association de la télomérase avec les télomères se fait préférentiellement en phase S. Ce recrutement est anticipé dans la phase S lorsque les télomères sont courts, en accord avec la réplication précoce de ces télomères. Par conséquent, l’élongation des télomères semble coordonnée avec leur réplication semi-conservative.
Le recrutement de la télomérase aux télomères est dépendant à la fois des protéines télomériques et des sous-unités de la télomérase. En effet un jeu complexe d’interactions entre les protéines télomériques et les sous-unités de la télomérase permettent son recrutement et son activation contrôlée.
En conclusion, l’activité de la télomérase est régulée de façon à coordonner son activité avec le moment de la perte de séquence aux télomères par la réplication et à favoriser l’élongation des télomères les plus courts, ce qui permet de maintenir l’ensemble de la population télomérique d’une cellule à une taille convenable.
L’importance de la taille
Une taille variée
Étonnamment, les télomères au sein d’une cellule et d’une population n’ont pas une taille identique bien définie, ils sont hétérogènes. Ceci peut s’expliquer par l’action conjuguée des mécanismes de raccourcissement et d’élongation des télomères. Alors que le problème de réplication des extrémités fait que l’ensemble des télomères raccourcit de 3 à 4 pb par division en moyenne chez S. cerevisiae, la télomérase n’agit que sur une faible proportion des télomères, et elle ajoute un nombre variable de répétitions lorsqu’elle agit. Il en résulte un équilibre dynamique, qui centre la taille des télomères autour d’une moyenne mais ne fixe pas une taille identique pour tous les télomères. Les télomères très courts ou très longs peuvent donc exister, mais sont moins fréquents que des télomères de taille moyenne. La plupart des télomères sont donc dans un état natif dit non-extensible, mais peuvent passer à un état extensible en devenant courts, ce qui les rend substrats potentiels de la télomérase.
Les mutants de nombreuses protéines, télomériques ou non, affectent la longueur des télomères. Ceci peut notamment être dû à un effet de ces protéines sur la télomérase. De plus, les télomères de levure sont aussi sensibles aux stress environnementaux : en présence d’éthanol, les télomères sont plus longs, alors qu’ils raccourcissent en réponse à une élévation de température ou à la caféine.
Des télomères courts qui changent d’identité
Ainsi, il est normal pour la cellule que certains de ses télomères soient plus courts que les autres. Cependant, ces télomères courts présentent des spécificités qui les différencient des autres télomères. Tout d’abord, le recrutement préférentiel de la télomérase aux télomères courts est permis par l’association des protéines MRX et Tel1 aux télomères courts.
Si un télomère court se différencie des télomères plus longs par sa composition protéique, il reste néanmoins distinct d’une cassure : une cellule reste capable de distinguer une coupure double brin d’un télomère, même en présence de répétitions télomériques. Par exemple, si la présence d’un unique télomère court dans la cellule peut activer la signalisation par phosphorylation de Rad53, la durée du cycle cellulaire n’est pas affectée par sa présence.
Par ailleurs, la réplication est aussi affectée par la taille des télomères. Ceux-ci sont ainsi répliqués de manière plus précoce quand ils sont courts, et la pause de réplication observée aux télomères n’a pas lieu lorsqu’ils sont courts, impliquant que la réplication est peut-être plus facile lorsque le nombre de répétitions diminue.
Les extrémités télomériques des chromosomes sont donc des structures nucléoprotéiques particulières, très organisées, et leur identité évolue lorsqu’ils deviennent courts. La maintenance de leur taille et de leur structure est garante de la protection des chromosomes et est donc essentielle à la viabilité cellulaire.
Télomères, vieillissement et cancers
Vieillissement et sénescence réplicative
Une limite à la viabilité cellulaire
À l’origine, les premières expériences de mise en culture de cellules de Vertébrés semblaient montrer l’immortalité des cellules. Pourtant, les études menées par Leonard Hayflick dans les années 1960 sont venues défier ce dogme. Elles ont montré en effet que le nombre de divisions que peuvent effectuer des cellules issues de différents tissus de fœtus humains est limité (Hayflick & Moorhead, 1961). Ce phénomène de barrière au nombre de divisions cellulaires a été nommé, par la suite, « limite de Hayflick ». Après la description moléculaire des télomères, il sera montré qu’en absence de télomérase, les télomères raccourcissent progressivement avant cet arrêt des divisions cellulaires.
Si dans les organismes unicellulaires tels que S. cerevisiae, la télomérase est active de manière constitutive et les télomères sont maintenus à une taille constante, ce n’est pas le cas dans les organismes pluricellulaires. En effet, chez l’Homme, la télomérase est active dans les tissus de la lignée germinale, mais pas dans les tissus somatiques normaux. Ainsi, la taille des télomères diminue quand l’âge de l’individu augmente, et on observe un raccourcissement progressif de la taille des télomères dans des cultures primaires de fibroblastes (Harley et al, 1990 ; Hastie et al, 1990). La ré-introduction de la télomérase s’oppose à ce raccourcissement, ce qui rétablit la capacité proliférative des cellules (Bodnar et al, 1998 ; Harley et al, 1990).
Cet arrêt des divisions cellulaires dû au raccourcissement des télomères en absence de télomérase est appelé « sénescence réplicative » (Figure 11 A et B). C’est un phénomène similaire qui a été observé lors de l’identification des sous-unités de la télomérase chez S. cerevisiae.
(A) Comportement théorique d'une population de cellules humaines d'après les observations de Harley et al, 1990 ; Hayflick, 1965 ; Hayflick & Moorhead, 1961.
(B) Effet de la ré-activation de la télomérase, d'après Bodnar et al, 1998.
(C) Comportement typique d'une population de S. cerevisiae en culture liquide après perte de la télomérase, d'après Lundblad & Blackburn, 1993 ; Lundblad & Szostak, 1989.
Ainsi, la sénescence réplicative est un arrêt irréversible du cycle cellulaire dans des cellules qui restent métaboliquement actives, dû au raccourcissement excessif des télomères. Chez les Mammifères, cet arrêt a lieu le plus souvent en phase G1 et est associé à de nombreux changements dans l’expression des gènes. Une forme prématurée de sénescence cellulaire peut aussi être induite par de nombreux stress, tels que le stress oxydatif, les lésions à l’ADN ou l’activation d’oncogènes. En particulier, les télomères peuvent être le lieu d’accumulation de dommages irréparables à l’ADN, source de sénescence.
Cependant, ce mécanisme a un coût, celui du vieillissement cellulaire. Même si le lien entre sénescence et vieillissement de l’organisme reste à prouver, de nombreuses données vont dans ce sens. Ainsi, les primates âgés accumulent progressivement des fibroblastes sénescents, en corrélation avec une accumulation de télomères dysfonctionnels. De plus, les télomères raccourcissent avec l’âge de l’individu, et la longueur des télomères est capable de prédire la mortalité à court terme chez une population sauvage de rousserolles des Seychelles.
Néanmoins, la viabilité d’un organisme reste contrôlée par l’élongation des télomères par la télomérase. Chez l’Homme, des mutations dans les gènes des sous-unités de la télomérase ou des protéines télomériques sont à l’origine de syndromes de vieillissement prématuré accompagné d’un raccourcissement des télomères, et la taille des télomères est un indicateur de la sévérité de la maladie.
C’est le cas notamment des patients atteints de dyskératose congénitale, qui présentent des mutations dans les gènes codants pour la télomérase ou les protéines télomériques. Ces patients peuvent montrer, entre autre, un vieillissement prématuré de la peau, une anémie, une maladie pulmonaire et une prédisposition aux cancers.
Alors que la souris est le modèle expérimental le plus utilisé, son comportement en réponse à la perte de la télomérase est différent de celui de l’Homme. En effet, la première génération de souris sans télomérase ne présente pas de défauts phénotypiques visibles, et ressemble donc à des souris « sauvages ». Ainsi, bien que la souris soit le modèle expérimental le plus utilisé, elle n’est peut-être pas le modèle le plus adapté pour l’étude du vieillissement lié à des défauts télomèriques.
À l’inverse, chez le poisson zèbre, comme chez l’Homme, la perte de la télomérase entraîne un phénomène de dégénérescence prématurée de nombreux tissus et une diminution de la durée de vie, associés au raccourcissement des télomères. C’est pourquoi certaines équipes de recherche explorent d’autres organismes modèles, tel que le poisson-zèbre.
Ainsi, la maintenance initiale des télomères par la télomérase est essentielle à la vie des organismes pluricellulaires, et le raccourcissement des télomères peut être source de vieillissement prématuré s’il est mal contrôlé.
S. cerevisiae comme modèle de sénescence
Chez S. cerevisiae, organisme unicellulaire, la sénescence réplicative n’est pas un évènement physiologique et est observée lors de la suppression expérimentale de l’un des gènes de la télomérase. Elle correspond à un arrêt du cycle cellulaire en phase G2/M, observé 60 à 80 doublements de populations après la perte de la télomérase, après raccourcissement des télomères. La vitesse de division de la population de cellules diminue progressivement par accumulation de cellules en phase G2/M (Fig. 11C). Les cellules arrêtées augmentent en taille, mais peu de ces cellules meurent immédiatement. Cette sénescence est aussi accompagnée par des changements d’expression de nombreux gènes et par une augmentation de l’instabilité génomique.
Remarquablement, dans une population de levure S. cerevisiae sans télomérase, une petite sous-population est capable d’échapper à la sénescence en mettant en place des mécanismes alternatifs de maintenance des télomères. Ces cellules survivantes envahissent alors la population et restaurent sa viabilité.
Il est donc possible de distinguer trois étapes successives dans la réponse d’une population de S. cerevisiae à la perte de la télomérase. Initialement, la culture perd progressivement en viabilité et la taille des télomères raccourcit. Cette étape correspond à la mise en place des réponses cellulaires à l’absence de télomérase, et donc à la mise en place de la sénescence, et a été désignée comme une phase de « pré-sénescence ». La culture atteint alors le pic de sénescence, qui correspond au moment où toutes les cellules arrêtent de se diviser, avant d’être envahie par les descendants des quelques cellules ayant été capables de trouver un mode de survie alternatif (Fig. 11C).
Les évènements cellulaires lors de la phase de pré-sénescence présentent encore de nombreuses zones d’ombre, notamment à cause de la limitation temporelle de cette étape. C’est pourtant probablement l’état majoritaire des cellules somatiques dans les tissus prolifératifs chez les Mammifères, notamment l’Homme, puisque la majorité des tissus somatiques ne présentent pas d’activité de la télomérase. Bien que pré-sénescence et sénescence semblent des évènements bien distincts au niveau d’une culture cellulaire, cette distinction est moins comprise à l’échelle cellulaire. Il est probable qu’une culture « pré-sénescente » à un instant donné soit constituée de cellules en division et de cellules déjà arrêtées en sénescence.
Le rôle des télomères dans le contrôle de la sénescence
Après la perte de la télomérase, les télomères raccourcissent donc progressivement jusqu’à mettre en place l’arrêt des divisions (Fig. 9 et 11). Les télomères sont ainsi au cœur du contrôle de la sénescence, et il est important de comprendre comment ils sont reconnus et maintenus au cours de ce processus.
Raccourcissement des télomères et sénescence
Nous avons vu précédemment que la taille des télomères est hétérogène et que les télomères courts présentent des spécificités par rapport aux autres télomères. Il est donc légitime de s’interroger sur la nature du moteur de la sénescence parmi les télomères, car si la sénescence est mise en place lorsque l’ensemble des télomères est court, il est possible que ce soit les télomères les plus courts parmi ces télomères courts qui induisent l’arrêt.
Chez la souris, ce sont les télomères les plus courts, et non la taille moyenne des télomères, qui importent dans la définition de l’« âge » d’un organisme. En accord avec cette idée, cinq télomères dysfonctionnels sont suffisants pour observer la sénescence dans des cellules humaines en culture. De plus, les fibroblastes sénescents de babouins âgés ne montrent qu’un seul foyer de protéines de dommage, ce qui souligne que seul un petit nombre de télomères est dysfonctionnel en sénescence. Chez S. cerevisiae, un seul télomère très court dans la cellule suffit à accélérer la sénescence. Les protéines télomériques sont de même impliquées dans le contrôle de la sénescence.
Ainsi, le raccourcissement des télomères, et en particulier la taille des télomères les plus courts, est le moteur de la mise en place de la sénescence. Celle-ci résulte notamment de l’instauration d’une signalisation en présence de ces télomères courts.
Autres voies de contrôle de la sénescence par les télomères
L’arrêt en G2/M peut être expliqué par la voie de signalisation des dommages à l’ADN qui conduit à la mise en place de l’arrêt des divisions cellulaires en réponse à la perte de la télomérase. Ce phénomène est conservé, puisque la voie de signalisation des dommages est aussi activée en sénescence dans des cellules humaines, et est nécessaire à l’arrêt du cycle cellulaire. Par contre, le substrat de l’activation de cette voie n’est pas encore clair.
Les ressemblances déjà observées entre un télomère et une coupure double brin, ainsi que l’implication de la voie de signalisation des dommages dans le contrôle de la sénescence, suggèrent que les voies de traitement d’une coupure double brin pourraient être impliquées aux télomères en sénescence, et éventuellement mener à la sénescence.
Ces résultats, dans leur ensemble, suggèrent que l’identité des télomères évolue lors de la mise en place de la sénescence après la perte de la télomérase, vers un état leur permettant d’être reconnus par la machinerie de réponse aux cassures double brin.
Complexité de la sénescence
Il est néanmoins difficile de simplifier la sénescence à ces quelques voies. En effet, les télomères en absence de télomérase sont sensibles aux perturbations de nombreuses autres voies cellulaires et de nombreux autres mécanismes ont été impliqués dans le contrôle de la sénescence, de manière plus ou moins détaillée, notamment grâce à un crible génétique.
Conjointement, l’implication de ces nombreuses voies montre que la maintenance de la protection des télomères devient essentielle en absence de télomérase pour soutenir la viabilité cellulaire à court terme.
Phénomènes d’évasion de la sénescence et cancers
Remarquablement, dans des cultures liquides de levure sans télomérase, on observe une reprise de la viabilité après la sénescence. Ceci est dû à la mise en place de mécanismes d’échappement à la sénescence par un petit nombre de cellules, grâce à des mécanismes alternatifs de maintenance des télomères (Fig. 11C). La capacité proliférative de ces cellules, appelées survivants, est rétablie et elles retrouvent une taille similaire à des cellules sauvages.
Chez S. cerevisiae, deux types principaux de survivants peuvent apparaître, avec des dépendances génétiques différentes. L’apparition de ces survivants requiert absolument les protéines Rad52 et Pol32, ce qui indique un mode de maintenance par la recombinaison, impliquant éventuellement la voie de réplication induite par les cassures.
Les survivants de type I sont obtenus par amplification du nombre de copies des éléments Y’ sur l’ensemble des chromosomes. Ils ne conservent qu’une courte région de répétitions télomériques terminales.
Au contraire, les survivants de type II se caractérisent par une élongation soudaine de la taille des télomères. Leurs répétitions TG1-3 télomériques sont très longues, de plusieurs kilobases, mais aussi très hétérogènes en taille. Elles raccourcissent progressivement avec les divisions cellulaires et subissent des évènements d’élongation ponctuels. Leur formation semble favorisée lorsque les télomères sont plus longs au moment de la sénescence.
Les survivants de type I représentent 90 % des survivants en absence de TLC1, et donc apparaissent plus fréquemment que ceux de type II. Cependant, ils ont une vitesse de croissance plus lente, ce qui explique que les survivants de type II finissent par envahir les cultures liquides.
Dans ces deux types de survivants, la réintroduction de la télomérase permet de rétablir un équilibre normal au télomère. Des molécules circulaires d’ADN Y’ ont été détectées dans les survivants de type I, et des molécules circulaires contenant uniquement des répétitions télomériques, parfois simple brin, dans les survivants de type II. Il est donc proposé que les télomères des survivants soient maintenus par un mécanisme de recombinaison en cercle roulant, moins favorisé que l’action de la télomérase.
De nombreuses autres espèces possèdent des mécanismes d’échappement de la sénescence, dont la nature peut varier. Les chromosomes de la levure S. pombe sont capables de fusionner sur eux-mêmes, probablement du fait de leur petit nombre. Ce phénomène est le mécanisme de survie principal chez S. pombe, plus fréquent que la survie par recombinaison télomérique.
Chez l’Homme, la télomérase est active dans les cellules de la lignée germinale et les cellules souches, mais son expression est faible ou absente dans les tissus somatiques « normaux ». Par contre, elle est réactivée dans la majorité des cancers (Kim et al, 1994 ; Wright et al, 1996). Il est proposé que cette réactivation n’est pas nécessaire à l’initiation de la tumorigenèse, mais qu’elle est nécessaire à la mise en place de l’immortalité dans ces cellules, et donc favorise la progression de tumeurs déjà établies. Dans les tumeurs où la télomérase n’est pas réactivée, les télomères, très longs et hétérogènes, sont maintenus par un mécanisme dit d’« élongation alternative des télomères » (ALT), dépendant d’évènements de recombinaison inter-télomériques encore mal compris.
Ainsi, la sénescence est un phénomène important dans l’équilibre d’un organisme pluricellulaire. En effet, elle permet de limiter la tumorigenèse en empêchant les divisions cellulaires. Néanmoins, cette fonction protectrice contre les cancers n’est pas sans conséquence, puisqu’elle est aussi source de vieillissement cellulaire. Les télomères et la télomérase sont aujourd’hui une cible privilégiée de la recherche sur le vieillissement. Alors que des souris chez qui la télomérase est absente depuis 4 générations montrent un vieillissement prématuré, la réactivation de la télomérase chez ces souris inverse la dégénérescence tissulaire. Pourtant, le risque potentiel de cancers lorsque la télomérase est active rend difficiles les modifications de ce mécanisme de vieillissement.
Conclusion
La télomérase et les télomères sont un des moteurs principaux du contrôle de la viabilité cellulaire. Les télomères protègent les chromosomes et la télomérase protège les télomères.
La perte de l’une entraîne la perte progressive des autres, jusqu’à un arrêt des divisions des cellules, qui peuvent rarement s’adapter et survivre. Étonnamment, ce phénomène de sénescence, apparemment commun à l’ensemble des Eucaryotes, est utilisé par les organismes pluricellulaires pour contrôler la viabilité des cellules somatiques.
Références
Remerciements à Maria Teresa Teixeira, responsable du groupe Biologie des télomères au laboratoire de biologie moléculaire et cellulaire des Eucaryotes (UMR8226 CNRS/UPMC)
- Blackburn EH (2006) A History of Telomere Biology. In Telomeres – Second Edition, Press CSHL (ed).
- Blackburn EH, Gall JG (1978) A tandemly repeated sequence at the termini of the extrachromosomal ribosomal RNA genes in Tetrahymena . J Mol Biol 120 : 33-53.
- Bodnar AG, Ouellette M, Frolkis M, Holt SE, Chiu CP, Morin GB, Harley CB, Shay JW, Lichtsteiner S, Wright WE (1998) Extension of life-span by introduction of telomerase into normal human cells. Science 279 : 349-352.
- de Lange T, Lundblad V, Blackburn EH (2006) Telomeres – Second Edition : Cold Spring Harbor Laboratory Press.
- Gilson E, Geli V (2007) How telomeres are replicated. Nat Rev Mol Cell Biol 8 : 825-838.
- Giraud-Panis MJ, Teixeira MT, Geli V, Gilson E (2010) CST meets shelterin to keep telomeres in check. Mol Cell 39 : 665-676.
- Greider CW, Blackburn EH (1985) Identification of a specific telomere terminal transferase activity in Tetrahymena extracts. Cell 43 : 405-413.
- Greider CW, Blackburn EH (1987) The telomere terminal transferase of Tetrahymena is a ribonucleoprotein enzyme with two kinds of primer specificity. Cell 51 : 887-898.
- Greider CW, Blackburn EH (1989) A telomeric sequence in the RNA of Tetrahymena telomerase required for telomere repeat synthesis . Nature 337 : 331-337.
- Harley CB, Futcher AB, Greider CW (1990) Telomeres shorten during ageing of human fibroblasts . Nature 345 : 458-460.
- Hastie ND, Dempster M, Dunlop MG, Thompson AM, Green DK, Allshire RC (1990) Telomere reduction in human colorectal carcinoma and with ageing . Nature 346 : 866-868.
- Hayflick L (1965) The Limited in Vitro Lifetime of Human Diploid Cell Strains . Exp Cell Res 37 : 614-636.
- Hayflick L, Moorhead PS (1961) The serial cultivation of human diploid cell strains . Exp Cell Res 25 : 585-621.
- Henriques CM, Carneiro MC, Tenente IM, Jacinto A, Ferreira MG (2013) Telomerase is required for zebrafish lifespan. PLoS Genet 9 : e1003214.
- Kim NW, Piatyszek MA, Prowse KR, Harley CB, West MD, Ho PL, Coviello GM, Wright WE, Weinrich SL, Shay JW (1994) Specific association of human telomerase activity with immortal cells and cancer. Science 266 : 2011-2015.
- Lundblad V, Blackburn EH (1993) An alternative pathway for yeast telomere maintenance rescues est1- senescence. Cell 73 : 347-360.
- Lundblad V, Szostak JW (1989) A mutant with a defect in telomere elongation leads to senescence in yeast. Cell 57 : 633-643.
- McClintock B (1939) The Behavior in Successive Nuclear Divisions of a Chromosome Broken at Meiosis . Proc Natl Acad Sci U S A 25 : 405-416.
- Moser BA, Nakamura TM (2009) Protection and replication of telomeres in fission yeast. Biochem Cell Biol 87 : 747-758.
- Olovnikov AM (1973) A theory of marginotomy. The incomplete copying of template margin in enzymic synthesis of polynucleotides and biological significance of the phenomenon . J Theor Biol 41 : 181-190.
- Watson JD (1972) Origin of concatemeric T7 DNA . Nat New Biol 239 : 197-201.
- Wicky C, Villeneuve AM, Lauper N, Codourey L, Tobler H, Muller F (1996) Telomeric repeats (TTAGGC)n are sufficient for chromosome capping function in Caenorhabditis elegans. Proc Natl Acad Sci U S A 93 : 8983-8988.
- Wright WE, Piatyszek MA, Rainey WE, Byrd W, Shay JW (1996) Telomerase activity in human germline and embryonic tissues and cells. Dev Genet 18 : 173-179.