Informations sur le virus du sida : structure, cycle viral, variabilité du virus... Phases de la maladie et pistes de traitement.
Cet article est ancien (2002). Pour un contenu plus récent, voir l'article VIH et sida.
Généralités
Introduction
Un virus est un parasite intracellulaire obligatoire ne pouvant se multiplier qu’à l’intérieur d’une cellule hôte et en utilisant sa machinerie cellulaire. Il contient une information génétique (sous forme d’ADN ou d’ARN) protégée par une structure compacte, souvent protéique, la capside. Il existe de nombreux types différents de virus, parmi lesquels on trouve les rétrovirus.
Les rétrovirus sont des virus d’un diamètre de 110 à 125 nanomètres, très répandus dans le monde animal. Ils sont la cause de différentes formes de cancers, d’immunodéficiences, dont le sida, et de dégénérescences du système nerveux central. Leur génome s’intègre sous forme d’ADN dans celui de la cellule hôte, pour ensuite s’exprimer pendant toute la vie active de la cellule. Les lentivirus (ou Lentivirinae) font partie de cette famille : ces virus sont responsables de pathologies à évolution lente.
L’exemple le plus connu de tels virus est le virus du sida : le HIV. Ce document s’attache à étudier quelques points de la biologie de ce virus.
Le virus du sida
Le virus du sida fait partie de la famille des lentivirus. Il s’agit d’un virus possédant un génome sous forme d’ARN, contenu dans une capside protéique, elle-même entourée par une enveloppe formée d’une membrane lipidique. Son nom correspond à son effet pathologique : VIH = Virus de l’Immunodéficience Humaine. La maladie qu’il cause chez l’Homme est le sida : Syndrome d’ImmunoDéficience Acquise.
Deux types de VIH
On distingue actuellement deux types de VIH : le VIH-1 et le VIH-2. Ces deux virus sont très proches (42 % d’homologie au niveau de leur génome). Le VIH-1 est le plus répandu : ce dossier traite essentiellement de ce virus (quelques distinctions entre ces deux virus seront toutefois dégagées).
Mode de transmission du virus
Le virus du sida peut être transmis de diverses manières, qui impliquent différents fluides corporels : le sang ou les sécrétions génitales (voir Les modes de transmission du virus du sida).
| Transmission par voie sexuelle | Transmission par le sang | Transmission materno-foetale |
|
Le virus est présent dans les sécrétions génitales, et peut donc être transmis lors d’un rapport sexuel, qu’il soit homosexuel ou hétérosexuel (la majorité des sidéens africains sont ainsi contaminés lors de rapports hétérosexuels). |
Le virus étant présent dans le sang, il peut être transmis lors de tout « don » de sang d’un individu à un autre : lors de pratiques toxicomanes (échanges de seringues), de manière accidentelle, ou lors de transfusions. |
Le virus est capable de traverser la barrière hémato-placentaire, et ainsi de contaminer, in utero, un fœtus. |
Répartition dans le monde
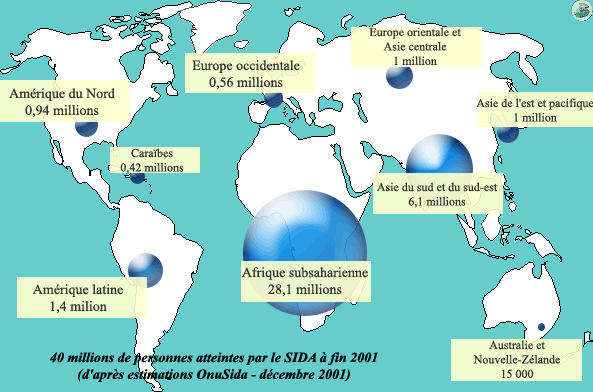
Selon les dernières estimations disponibles (OnuSida, rapport de décembre 2001), le nombre de personnes contaminées par le virus du Sida atteindrait les 40 millions dans le monde. L’Afrique représente la plus grande part, avec 28,1 millions d’individus pour la seule Afrique subsaharienne.
Le bilan de l’année 2001 est donc le suivant : 5 millions de nouveaux cas (dont 800 000 enfants de moins de 15 ans) ; 3 millions de décès dus au sida (dont 580 000 enfants de moins de 15 ans).
Structure du VIH et de son génome
Structure du VIH-1
Le virus du sida se compose d’un matériel génétique (ARN) accompagné de quelques protéines, le tout contenu dans deux « coques » protéiques (les capsides), elles-mêmes entourées d’une membrane portant des protéines spécifiques (cette membrane et ces protéines forment l’enveloppe du virus).
Vous pouvez télécharger cette animation sur la structure du virus du sida, pour une lecture ultérieure hors-connexion. Choisissez pour cela une des 4 versions proposées ci-dessous. La version « seule » correspond à une page HTML comportant l’animation : elle nécessite un ordinateur ayant un navigateur internet avec le plug-in Flash. Après décompaction, un dossier est créé (« VIH-1 »), comprenant plusieurs fichiers : un fichier HTML et un ou plusieurs fichier(s) SWF ; cliquez sur le fichier HTML (visualisable avec un navigateur internet) pour voir l’animation. La version « + lecteur » peut être lue sur un ordinateur ne possédant pas le plug-in Flash. Tous les fichiers sont compactés et auto-extractibles : après le téléchargement, il vous suffit de cliquer dessus pour les décompresser.
- Windows, animation seule : VIH-1win.exe
- Windows, animation + lecteur : VIH-1pwin.exe
- Mac OS, animation seule : VIH-1mac.sea
- Mac OS, animation + lecteur : VIH-1pmac.sea
Structure du génome viral
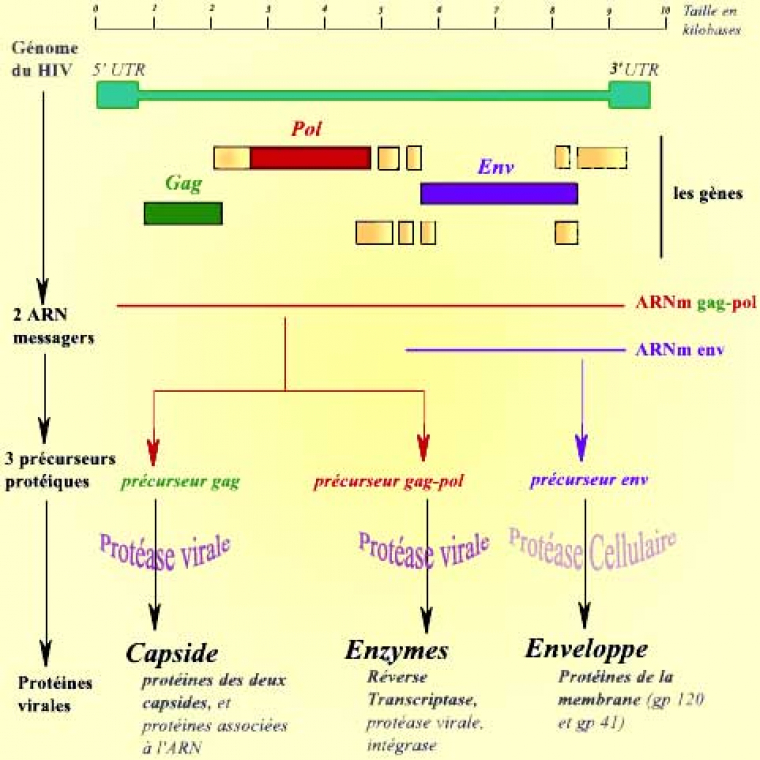
Le génome du virus du sida se compose d’un ARN simple brin de 9 181 nucléotides. Il comporte trois gènes principaux (Gag, Pol et Env), ainsi que quelques gènes de régulation, de petite taille. Il comporte, de plus, des séquences spécifiques situées à ses extrémités 5'UTR et 3'UTR (UTR = région non transcrite « UnTranscribed Region »).
Une fois rétrotranscrit sous la forme d’un ADN double brin (voir cycle), le génome du virus s’exprime par le biais de deux ARN messagers, qui aboutissent à la synthèse de trois protéines. Ces protéines sont ensuite clivées par des protéases, pour aboutir aux différentes protéines virales :
Vous pouvez télécharger cette animation pour une lecture ultérieure hors-connexion. Choisissez pour cela une des 4 versions proposées ci-dessous. La version « seule » correspond à une page HTML comportant l’animation : elle nécessite un ordinateur ayant un navigateur internet avec le plug-in Flash. Après décompaction, un dossier est créé (« VIH-1 »), comprenant plusieurs fichiers : un fichier HTML et un ou plusieurs fichier SWF ; cliquez sur le fichier HTML (visualisable avec un navigateur internet) pour voir l’animation. La version « + lecteur » peut être lue sur un ordinateur ne possédant pas le plug-in Flash. Tous les fichiers sont compactés et auto-extractibles : après le téléchargement, il vous suffit de cliquer dessus pour les décompresser.
- Windows, animation seule : cyclewin.exe
- Windows, animation + lecteur : cyclepwin.exe
- Mac OS, animation seule : cyclemac.sea
- Mac OS, animation + lecteur : cyclepmac.sea
Remarque : En plus des trois gènes « de structure » (Gag, Pol et Env), le virus du sida possède six gènes codant pour des protéines régulatrices. Ces protéines sont particulièrement importantes dans l’accomplissement de la réplication, de la transcription, de l’export des ARN viraux du noyau, etc. Leur expression est complexe. Ces six gènes sont caractéristiques de la famille des lentivirus, à laquelle appartient le VIH. Par souci de simplicité, ces gènes régulateurs sont omis dans l’ensemble de ce document.
Cycle du VIH
Le virus du sida présent dans le sang est capable de se fixer à des cellules particulières du système immunitaire : les lymphocytes T CD4 (ainsi nommés car ils portent la protéine transmembranaire CD4). La fixation du virus à ces cellules fait intervenir CD4 (reconnu par la protéine gp120 du virus), ainsi que d’autres protéines membranaires ; les co-récepteurs (voir plus loin :entrée du virus). Suite à cette fixation, le matériel génétique du VIH peut pénétrer dans le lymphocyte.
Il est à noter que le VIH peut, en fait, infecter de nombreux types cellulaires différents. Nous nous limiterons ici à l’exemple des lymphocytes T CD4.
Une fois dans le cytoplasme, l’ARN du virus est rétrotranscrit en ADNc (ADN complémentaire) double brin. Cet ADNc pénètre dans le noyau, et s’intègre au génome de la cellule hôte. L’expression des gènes du virus permet alors la fabrication des protéines du virus. Une fois assemblées, ces protéines permettent la formation de nouveaux virions, qui bourgeonnent de la cellule en s’entourant au passage d’une membrane (héritée de la cellule infectée). Ceci permet la libération de nouveaux virus dans le sang de l’organisme infecté.
Il est à noter que l’expression du génome viral se réalise grâce à la machinerie de transcription (puis de traduction) de la cellule infectée.
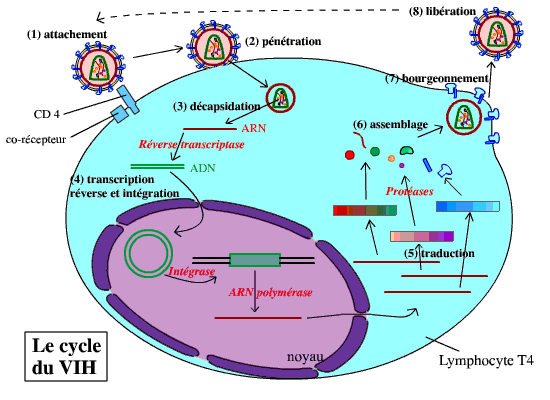
Le schéma résume le cycle du VIH. Pour une animation voir ci-dessous.
Légendes :
(1) Attachement : Le virus se fixe sur le lymphocyte T CD4, par reconnaissance entre la protéine virale gp120 et la protéine CD4 du lymphocyte (ainsi qu’un co-récepteur).
(2) Pénétration : Les deux membranes (du virus et du lymphocyte) fusionnent, ce qui permet la pénétration de la nucléocapside (les deux capsides + le matériel génétique, etc.) dans le cytoplasme.
(3) Décapsidation : Les deux capsides se dissocient, libérant l’ARN viral dans le cytoplasme.
(4) Transcription inverse et intégration : Grâce à la transcriptase inverse virale, l’ARN viral est rétrotranscrit en ADN double brin. Cet ADN pénètre dans le noyau, où il s’intègre au génome du lymphocyte. Il est ensuite transcrit en ARN.
(5) Traduction : Après avoir été transcrits par l’ARN polymérase de la cellule, les ARN messagers viraux sont traduits en trois précurseurs protéiques. Ces précurseurs sont clivés par des protéases, pour donner les différentes protéines du virus.
(6) Assemblage : Les protéines virales et l’ARN viral (transcrit par ailleurs) sont associés pour reformer des virus (sans la membrane). Les protéines virales membranaires sont intégrées à la membrane du lymphocyte.
(7) Bourgeonnement : Le virus bourgeonne, emportant un fragment de la membrane plasmique du lymphocyte (qui contient uniquement les protéines membranaires virales).
(8) Libération : Les nouveaux virus sont libérés dans le milieu intérieur. Ils peuvent infecter de nouveaux lymphocytes T CD4.
Mécanisme d’entrée du VIH dans les cellules
Protéines virales et CD4
Le virus du sida utilise, pour rentrer dans ses cellules hôtes, les protéines présentes au niveau de sa membrane et de celle de la cellule hôte. La protéine virale gp120 possède en effet un domaine de liaison à la protéine CD4. Le virus du sida est ainsi capable de se fixer spécifiquement aux lymphocytes porteurs de cette protéine, les T CD4. Cette fixation de gp120 à CD4 conditionne l’ensemble des étapes suivantes, permettant la pénétration de la nucléocapside virale dans le lymphocyte.
La fixation de gp120 à CD4 permet de démasquer une autre protéine membranaire virale : gp41. Celle-ci s’insère alors dans la membrane du lymphocyte, permettant la fusion des deux membranes, et ainsi l’entrée du virus dans la cellule :
Co-récepteurs du VIH
En réalité, le récepteur CD4 seul est insuffisant pour une pénétration du VIH dans la cellule. Des co-récepteurs sont nécessaires. Parmi ceux-ci, on peut citer deux protéines transmembranaires : CXCR-4 et CCR-5. Ces co-récepteurs ne sont pas des protéines spécifiques des lymphocytes T CD4 : de nombreuses autres cellules les possèdent.
Toutes les souches de VIH n’utilisent pas le même co-récepteur. D'autres co-récepteurs sont possibles…
Il est à noter que certaines personnes possédant un allèle particulier du co-récepteur CCR5 (délétion de 32 paires de bases dans le gène) semblent résistantes à l’infection par le VIH. Ces individus représenteraient 1 % de la population.
Mécanismes d’entrée du VIH dans les cellules
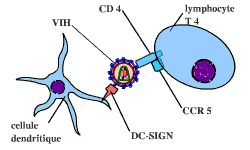
En plus de CD4 et d’un co-récepteur (par exemple, ici, CCR-5), un troisième type de récepteur serait également présent : un transporteur.
Ce transporteur serait la protéine DC-SIGN, qui est portée par les cellules dendritiques présentatrices d’antigènes, localisées sur l’épithélium muqueux. En se fixant sur cette protéine, le virus du sida deviendrait plus résistant vis-à-vis du système immunitaire. De plus, les cellules dendritiques migrent vers les ganglions, où se trouvent de nombreux lymphocytes T CD4…
Un exemple de variabilité du VIH : le VIH-1
Neuf sous-types de VIH-1
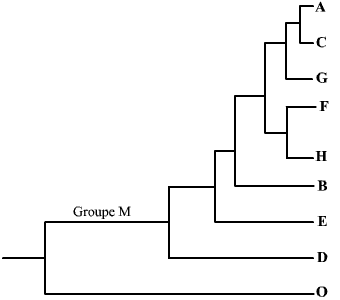
On distingue deux types de VIH : le VIH-1 et le VIH-2.
Le sous-type O est très différent des 8 autres : on peut le considérer comme une espèce différente de VIH.
Pour chaque type, il est possible de dégager un certain nombre de sous-types, sur la base de comparaison de séquences. Ainsi, pour le VIH-1, on ne compte pas moins de 9 sous-types (ci-contre).
Ces différents sous-types (ou souches) peuvent être corrélés à des zones géographiques. Par exemple, la souche B est essentiellement présente en Amérique du Nord et en Europe. Néanmoins, il est à noter que l’on trouve différentes souches au sein d’une même zone géographique, et même au sein d’un même individu infecté…
La variabilité du VIH est très forte.
Origine de la variabilité du VIH
Deux mécanismes rentrent en jeu pour expliquer une telle variabilité du VIH :
-
la transcriptase inverse a un taux d’erreur très élevé, de l’ordre de 10-3 à 10-4. Ceci correspond à une à deux mutation(s) par cycle de réplication ;
-
le taux de renouvellement du virus est très élevé (demi-vie de 48 h), ce qui donne de 108 à 109 virions synthétisés par jour.
Une telle variabilité rend difficile l’élaboration d’un vaccin. Ainsi, lorsque le système immunitaire est encore fort, on observe un grand nombre de variants, dus aux mutations : le virus déborde ainsi le système immunitaire, qui est alors détruit. La variabilité se réduit alors, le variant le plus efficace prenant le dessus.
Évolution du virus et diagnostic
Évolution de l’infection virale
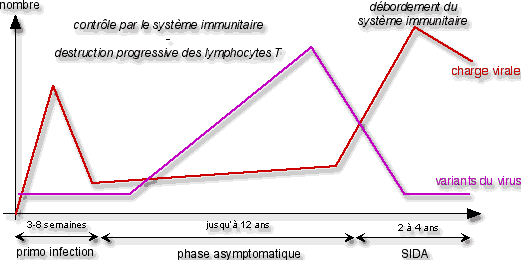
On distingue 3 phases lors d’une infection par le virus du sida :
- La primo-infection : juste après la contamination par le VIH, le nombre de virus présents (= charge virale) augmente fortement, puis diminue rapidement, du fait de la réponse du système immunitaire ;
- La phase asymptomatique : l’individu atteint ne présente aucun symptôme de la maladie, et le nombre de virus n’augmente que très légèrement ; mais le nombre de variants augmente fortement…
Malgré le contrôle de la maladie par le système immunitaire, les lymphocytes T sont progressivement détruits par le virus ; - Le sida : le système immunitaire est débordé ; le nombre de virus augmente fortement (mais le nombre de variants se limite aux plus efficaces) ; les symptômes apparaissent.
Diagnostic
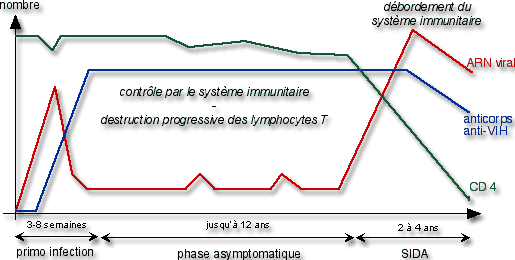
Parallèlement à l’évolution de l’infection, un certain nombre de paramètres varie : la quantité de CD4 (correspondant au nombre de lymphocytes – elle diminue donc pendant la phase asymptomatique), la quantité d’ARN viral (correspondant au nombre de virus), et les anticorps anti-VIH. Ces derniers montrent la réaction du système immunitaire face à l’infection par le VIH. Ils apparaissent lors de la primo-infection (qui dure de 3 à 8 semaines).
Chez les adultes, cette apparition d’anticorps anti-VIH est utilisée pour diagnostiquer une infection par le virus du sida. On recherche ainsi leur présence, par deux tests de dépistage ELISA (fixation des anticorps), puis par un test de confirmation par Western blot (séparation de protéines sur gel).
En cas de résultat positif, on dit que l’individu est séropositif : il possède des anticorps anti-VIH dans son sérum.
Il est à noter que l’infection n’est pas décelable par cette méthode lors de la primo-infection (pas d’anticorps…).
On propose donc de réaliser généralement 2 tests à deux mois d’intervalle (sauf s’il n’y a pas eu de pratique à risque depuis deux mois). Toutefois, on peut déceler une primo-infection en recherchant la présence d’antigène p24 (capside interne) dans le sérum.
Chez le nouveau-né, on réalise un diagnostic direct : coculture de cellules sanguines prélevées chez l’enfant avec des lymphocytes, puis détection de l’ARN viral par PCR. En effet, les anticorps franchissant la barrière hémato-placentaire, une séropositivité à la naissance n’est que le reflet de celle de la mère du nouveau-né…
Suivi sérologique d’un patient VIH+
Un patient séropositif est suivi, pour observer l’évolution de la maladie. Pour cela, on recherche l’ARN viral dans le plasma et on le quantifie. Ceci donne la quantité de virus présent, ou charge virale.
Thérapeuthique
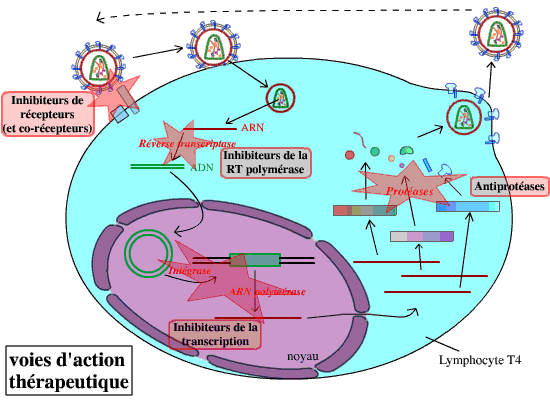
Les recherches de traitement contre le virus du sida sont multiples. Elles font appel aux connaissances actuelles sur le cycle du virus : ses moyens pour s’accrocher et pénétrer dans ses cellules cibles, son expression dans ces cellules, etc. Il existe de nombreuses voies de traitement, visant donc à bloquer le développement du VIH en différents points de son cycle :
Des traitements visant à prévenir l’infection (blocage de l’attachement et de la pénétration du virus dans la cellule), qui étaient encore inefficaces il y a peu, sont en cours de développement. Les traitements actuels utilisent un mélange d’inhibiteurs de la transcriptase inverse et d’antiprotéases : ces traitements sont efficaces, mais ils n’éliminent pas le virus de l’organisme infecté. Leur action consiste essentiellement à bloquer l’expansion du virus : ceci nécessite donc un traitement à vie.
On attend beaucoup également de la thérapie génique, mais pour l’instant ce type de traitement n’est pas encore appliqué.
En conclusion, le meilleur traitement reste encore la prévention…