Depuis les années 90, la vision du monde des ARN a été bouleversée par la découverte de nombreuses sortes de petits ARN aux multiples fonctions. Cet article détaille en particulier le cas des micro-ARN et des ARN interférents, montrant leur importance dans le domaine de la recherche scientifique mais aussi médicale, avec de nombreuses applications thérapeutiques envisageables.
Introduction
Longtemps, les ARN ont paru être de simples intermédiaires entre ADN et protéines : ARN codants, correspondant aux ARN messagers (ARNm) transmettant le message du gène dans le cytoplasme, ARN non-codants, correspondant aux ARN ribosomiques et ARN de transfert œuvrant au déchiffrement et à la traduction de l’ARNm en protéine, et ARN catalytiques participant à l’épissage des introns.
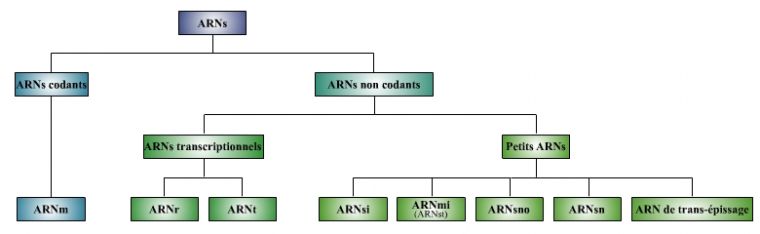
Mais tout un nouveau monde de petits ARN non codant (ARNnc) a été découvert depuis la fin des années 90 (voir figure ci-dessous). Il comprend notamment deux nouvelles classes de petits ARN : les micro-ARN (ARNmi) et les petits ARN interférents (ARNsi : small interfering RNA) qui remplissent de nombreuses fonctions, en particulier celle de l’inhibition post-transcriptionnelle de l'expression des gènes.
ARN : différents types d’ARN, ARNm : ARN messager, ARNr : ARN ribosomique, ARNt : ARN de transfert, ARNsi : small interfering RNA ou petit ARN interférent, ARNmi : micro ARN (qui comprennent les ARNst (small temporal RNA ou petit ARN temporaire), ARNsno : small nucleolar RNA ou petit ARN nucléolaire, ARNsn : small nuclear RNA ou petit ARN nucléaire.
Quel est ce mécanisme, comment a-t-il été découvert, et quelles sont ses applications ? (référence 1)
Le mécanisme de l’inhibition traductionnelle
Les petits ARNmi et ARNsi ne sont pas codés par la même partie du génome. Les premiers (ARNmi) proviennent de gènes qui leur sont propres et dont ils sont les uniques produits. Les seconds (ARNsi) dérivent de deux sources, exogène ou endogène. La source exogène correspond soit à l’apport extérieur d’un ARN double brin par injection expérimentale, par exemple dans le nématode C. elegans, soit à un apport en provenance de génomes à ARN double brin comme ceux de certains virus à ARN des plantes. La source endogène correspond à une production naturelle par utilisation des parties exoniques (codantes ou non codantes) d’un gène plus étendu.
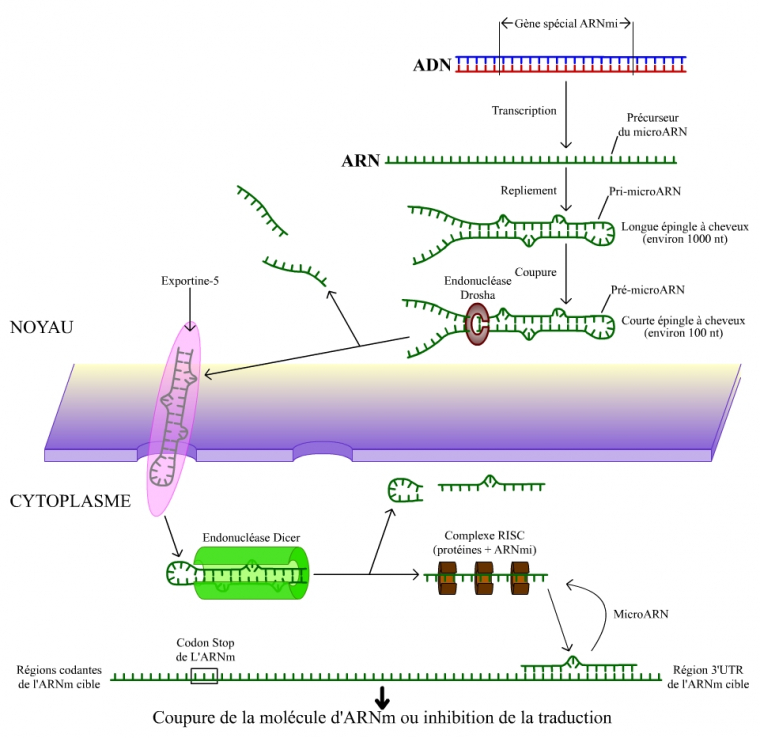
Concernant les ARNmi, leur transcrit est d’abord, pour chacun, une molécule d’ARN simple brin d’un millier de nucléotides. Chacune de ces molécules présente, le long de sa séquence, des motifs nucléotidiques intrachaînes partiellement complémentaires, qui les conduisent à adopter une structure secondaire en forme d’une longue épingle à cheveux. Cette structure peut être divisée en trois parties : le « corps » qui est formé de séquences plus ou moins complémentaires présentes sur le simple brin, se disposant en vis-à-vis par appariement, la « tête » (en forme de boucle) et les « jambes », simple brin de l’épingle qui portent les séquences n’ayant pas trouvé de complémentaires. Se produit alors la série de transformations suivante.
L’enzyme Drosha (ribonucléase de type III) y effectue une première série de coupures qui réduit cette structure en une courte molécule d’une centaine de nucléotides, toujours en épingle à cheveux (short hairpin RNA : shRNA), mais amputée de ses « jambes ». L’exportine-5 la transporte alors dans le cytoplasme.
Là, une seconde ribonucléase de type III, appelée Dicer, achève le travail commencé par l’enzyme Drosha : par une deuxième série de coupures, elle élimine la « tête » de l’épingle à cheveux tandis que d’autres protéines qui lui sont associées (de type hélicase) dissocient le petit ARNdb (double brin) subsistant, d’une vingtaine de nucléotides, en deux ARN simple brin. L’enzyme Dicer clive et sépare également les longs ARN double brin des ARNsi en morceaux d’environ 21 nucléotides.
L’un des simples brins obtenus est le microARN (ARNmi) ou le petit ARN interférent (ARNsi). Il s’associe à un complexe protéique en formant un nouveau complexe appelé RISC (RNA Induced Silencing Complex). C’est en cet équipage qu’il se porte sur sa cible : l' ARNm auquel il s’apparie.
En cas d’appariement parfait (ARNsi), l’ARNm est détruit et il n’y pas traduction. Les RISC qui sont à l’origine de cette destruction restent ensuite parfaitement fonctionnels, ce qui leur permet d’opérer de nouveau sur d’autres ARNm de même spécificité. C’est cette réutilisation qui les rend particulièrement offensifs. Mais même lorsque l’appariement est imparfait (ARNmi), il y a tout de même barrage à la traduction de l’ARNm.
À travers l’exemple des ARNmi, la figure ci-dessous résume le mode d’action de ces petits ARN.
Pour une présentation en 3D, accéder à une animation Flash sur le site de la revue Nature (commentaires en anglais).
Les ARNmi comme les ARNsi réduisent donc les gènes au silence en agissant au stade post-transcriptionnel.
Quelques grandes étapes de leur découverte
La mise en évidence de petits ARN double brin capables de réduire spécifiquement un ARNm au silence résulte de travaux effectués chez un modeste ver rond nématode, grand habitué des paillasses, Caenorhabditis elegans (C. elegans).
En 1995, Guo et Kemphues, de l’université Cornell à New York, étudiaient, chez ce ver, le gène par-1 indispensable à l’établissement de la polarité antéro-postérieure lors de la première division de la cellule-œuf (référence 2). Au cours de l’étude de la fonction de ce gène, ils ont tenté d’éteindre son expression en injectant, dans la gonade, l’ARN complémentaire du messager de ce gène, c’est-à-dire l’ARN-antisens. Il était attendu par les auteurs que cette injection conduise, dans les embryons produits par l’animal injecté, à la production d’un long ARN double brin résultant de l’appariement de l’ARNm avec l’ARN-antisens injecté. Un tel appariement devait empêcher l’ARNm de par-1 d’être traduit. Cette expérience devait donc permettre de phénocopier le résultat d’une mutation nulle dans le gène par-1 et d’obtenir un défaut de polarisation de l’embryon. Tel fut bien le résultat obtenu. Mais curieusement – pour l’époque – l’injection témoin d’ARN-sens eut le même effet. Et pourtant, il ne pouvait pas s’apparier à l’ARNm !
En 1998, Fire et collaborateurs, du département d’embryologie de Baltimore (USA), se trouvèrent confrontés au même phénomène déroutant en étudiant le gène unc-22, indispensable au bon fonctionnement des muscles de C. elegans (référence 3).
Ils se demandèrent si les préparations d’ARN-sens injectées n’étaient pas en réalité contaminées par des ARN-antisens du fait d’une propriété particulière de l’enzyme (l’ARN polymérase ADN dépendante de phage) utilisée pour réaliser la synthèse in vitro des brins sens et antisens d’ARN.
Ils testèrent cette idée en injectant, d’une part des solutions purifiées d’ARN-sens ou d’ARN-antisens (qui n’eurent que peu d’effet sur les muscles des vers), et d’autre part une solution contenant un mélange de ces deux molécules. Celui-ci agit tellement sur la musculature des vers qu’on les vit entrer en convulsion dans leur boîte de Petri. Et ce phénomène se produisait même avec une très petite quantité du mélange, ce qui laissait présager un processus catalytique.
L’injection d’un mélange de molécules d’ARN-sens et d’ARN-antisens susceptibles de s’apparier entre elles en de longs ARNdb apparaissait donc comme un moyen extrêmement efficace d’empêcher l’expression d’un ARNm cible, du moins chez C. elegans. C’est d’ailleurs la présence d’ARN double brin à l’état de trace dans les expériences de Guo et Kemphues qui expliquent leurs résultats. Hélas, une étude de ce type ne pouvait être menée sur les cellules de mammifères, car la présence de ces longs ARNdb, à la suite de leur injection, déclenche chez elles une réponse générale non spécifique de la séquence de l’ARNdb injecté. Cette réaction cellulaire fait intervenir la production d'interférons qui provoquent un blocage généralisé de la synthèse des protéines entraînant la mort cellulaire.
En 2000, Pasquinelli et collaborateurs, de l’école médicale de Boston (USA), qui travaillaient aussi sur C. elegans, mirent en évidence le rôle d’un petit ARN codé par le gène let-7 indispensable au passage du dernier stade larvaire au stade adulte (référence 4). Ce petit ARN partage des traits communs (fabrication à partir d’un ARN en épingle à cheveux, capacité à se fixer sur un ARNm cible) avec un autre petit ARN, l’ARN lin-4, découvert sept ans plus tôt, qui gouverne le passage du stade larvaire 1 au stade larvaire 2.
Mais, cette fois-ci, contrairement à lin-4 détecté chez le seul C. elegans, les homologues de let-7 sont retrouvés chez tous les eucaryotes testés : protozoaires, champignons, plantes et animaux.
La conservation de let-7 au cours de l’évolution était donc l’indice que ce qui avait pu paraître anecdotique avec le gène lin-4 du seul C. elegans devait être, en réalité, un mode de régulation majeur de l’expression génique des eucaryotes.
Il était donc opportun de partir à la recherche des petits ARN passés inaperçus jusque-là, tant par manque de savoir-faire technique que par habitude de ne concevoir les ARN que sous le seul angle de la triade ARN messager, ARN ribosomal et ARN de transfert. Plus de cent petits ARN allaient être découverts : un nouveau monde ARN s’ouvrait devant les chercheurs, tandis que l’énigmatique mécanisme de l’inhibition des ARNm commençait à être élucidé.
La percée finale eut lieu un an plus tard. Elle fut l’œuvre d’Elbashir et collaborateurs, de Göttingen en Allemagne, qui apportèrent la preuve qu’en administrant aux cellules de mammifères ces petits ARN (dans leur état double brin, avant dissociation par les protéines associées à l’enzyme Dicer) la réponse interféron n’avait plus lieu, et surtout que les ARNm cibles étaient réduits au silence (référence 5). Cette découverte fut saluée comme l’avancée majeure de l’année 2002 par la revue Science.
Les premières applications
Ces petits ARN (ARNsi ou ARNmi), susceptibles de détruire spécifiquement un ARNm cible, n’ont pas été longs à entrer dans la panoplie des nouveaux outils de la biologie moléculaire. Ils présentent en effet un double intérêt :
- de révélateur de la fonction des gènes, puisqu’une fonction qui n’est plus accomplie dit, par défaut, celle que tenait le gène lorsque son ARNm pouvait être traduit en protéine ;
- d’outil thérapeutique, puisque le message nocif de tel ou tel gène peut être interdit d’expression.
Chez les organismes dont le génome a été séquencé, des comparaisons fines ont permis de retrouver, sur les gènes codant des protéines, des séquences correspondant à celles qui donnent naissance aux petits ARN, raison pour laquelle ceux-ci peuvent ensuite s’apparier aux ARNm de ces gènes.
Elles sont de plus en plus engrangées dans des banques ARNi mises à la disposition des chercheurs du monde entier ; et l’on sait leur associer les promoteurs qui peuvent les faire s’exprimer dans les cellules où elles sont introduites.
La thérapeutique par petits ARN soulève de grands espoirs, mais les obstacles restent nombreux lorsqu’il s’agit de passer de simples cultures cellulaires à des êtres vivants, et notamment de :
- leur faire gagner les cellules cibles et de leur faire franchir les membranes cellulaires ;
- vérifier leur absence de toxicité ;
- estimer leur stabilité et donc les doses à administrer ;
- s’assurer de leur spécificité.
Trois exemples rendront compte des succès obtenus et des difficultés rencontrées.
Tumeurs cérébrales
Si les tumeurs cérébrales peuvent grossir c’est qu’à l’instar de toutes les tumeurs solides leurs récepteurs (EGFR) captent activement le facteur de croissance épidermique (EGF pour epidermal growth factor).
Entraver par interférence ARN la construction de ce récepteur, empêcherait l’entrée de Ca2+ dans ces cellules, lequel stimule la réplication de leur ADN et donc la prolifération.
Encore faut-il que l’ARNi délivré parvienne à franchir la barrière hémato-encéphalique puis la membrane plasmique des cellules cancéreuses.
Mission accomplie en février 2004 par l’équipe de William Pardridge (Université de Californie, Los Angeles, USA) chez un modèle souris dont le cerveau avait été injecté de cellules cancéreuses de névroglie humaine (référence 6).
Les petites sphères lipidiques (liposomes), qui étaient prodiguées chaque semaine dans la circulation sanguine des souris, contenaient des plasmides codant pour le petit ARN en épingle à cheveux (shRNA, voir figure sur le mécanisme de l’inhibition) qui allait être à l’origine de la reconnaissance, puis de la destruction des ARNm EGFR.
Ces sphérules contenaient aussi des anticorps qui, en se liant à des récepteurs spécifiques de la barrière hémato-encéphalique murine (mouse transferrin receptor) et des cellules cancéreuses humaines (human insulin receptor) leur permettaient de franchir ces deux obstacles.
Les souris ainsi traitées survivaient deux fois plus longtemps que leurs congénères témoins ; leurs cellules tumorales mises en culture n’absorbaient presque plus de Ca2+, de même qu’elles n’incorporaient pratiquement plus la thymidine indispensable à la réplication de leur ADN.
Le petit ARN en épingle à cheveux avait donc bien été transformé en petit ARNi actif, et cela par l’endonucléase Dicer des cellules cancéreuses humaines ; et l’ARNm codant pour l’EGFR avait été détruit. Un beau succès obtenu in vivo chez la souris et, techniquement, une magnifique expérience !
Le sida
L’interférence ARN peut-elle être utilisée dans la lutte contre le virus du sida ? On peut l’envisager, d’autant que certains succès ont été obtenus. Par exemple, dans des lymphocytes et macrophages en culture, infectés par le virus, l’injection d’ARNi est parvenue à détruire les ARNm codant pour des protéines (Tat, Gag ou Rev) indispensables à la réplication du virus, bloquant celle-ci. Hélas, lorsque les cultures se prolongent, le virus du sida, connu pour son énorme variabilité génétique, finit par échapper aux ARNi, qui ne reconnaissent plus leur cible complémentaire sur les ARNm viraux. C’est donc sur toute une gamme d’ARNi et non sur un seul qu’il s’agit de jouer pour contourner cette résistance.
La mise au point d’une stratégie par interférence ARN contre le virus du sida est d’autant plus difficile que macrophages et lymphocytes ne sont pas les seules cibles touchées par le virus. Mais les recherches foisonnent et sans cesse paraissent de nouveaux résultats.
La dégénérescence maculaire
Pour la première fois, et avec l’accord de la Food and Drug Administration, depuis novembre 2004, la thérapie par ARNi est en test clinique chez l’Homme aux États-Unis.
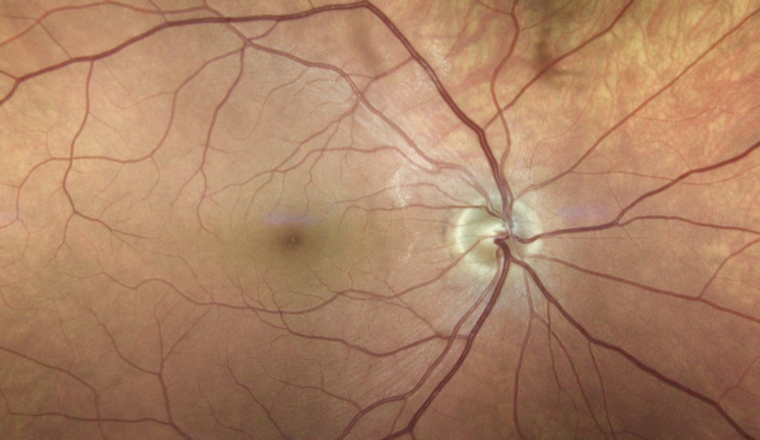
L’objectif est de combattre une maladie de la rétine, liée à l’âge : la dégénérescence maculaire, sous sa variante forme humide (wet-AMD). La maladie peut se déclarer dès l’âge de 50 ans. Elle affecte la macula, région centrale de la rétine, de couleur jaune, englobant la fovéa (zone assurant une vision précise, nécessaire à la lecture, et colorée), voir figure ci-dessous. Cette zone de la rétine ne comporte pas de vaisseaux sanguins et est irriguée, en périphérie, par les vaisseaux de la rétine, et en profondeur, par ceux de la choroïde contiguë. La wet-AMD est provoquée par la croissance anormale des vaisseaux sanguins situés en arrière de celle-ci, qui finissent par la recouvrir et par la léser, en laissant fuir leur contenu.
Ce détail d'un fond d'œil montre la tache aveugle (blanche, zone de convergence des neurones en nerf optique) et la macula, centrale, de couleur jaune, de 5 mm de diamètre environ, dépourvu de vaisseaux et renfermant, en son centre, la fovéa.
Les patients commencent par ne plus pouvoir lire, ni conduire, et la cécité survient lorsque la prolifération des vaisseaux gagne toute la rétine. Les moyens de traitement actuels se révèlent souvent impuissants. Or, c’est le facteur de croissance endothélial vasculaire (VEGF) qui fait proliférer les vaisseaux de la rétine et c’est bien sûr son ARNm, ou celui de son récepteur, qui pourraient être ciblés par des ARNi.
Des entreprises de biotechnologie les ont mis au point et des essais préliminaires ont été conduits chez des primates, notamment par l’équipe de Reich (Université de Pennsylvanie, Philadelphie, USA), au début de l’année 2004. L’expérience a consisté à injecter l’ARNi dans le corps vitré de l’œil, à raison d’une fois toutes les six semaines. Chez les primates traités, les fuites provenant des vaisseaux lésés se sont arrêtées au 21e jour, tandis que la construction de nouveaux vaisseaux cessait au 35e. Et cela, sans effet nocif, même aux plus fortes doses (référence 7).
Des équipes médicales et universitaires sont en train de tester ces ARNi sur quelques patients, en procédant à des injections dans le corps vitré ou dans le blanc de l’œil. Les premiers résultats seront publiés vers la fin de l’année 2005.
L’état actuel de la recherche clinique sur l’utilisation de l’interférence ARN à des fins thérapeutiques est à retrouver dans la thèse citée à la fin de cet article.
Conclusion
Il est aujourd’hui établi que les petits ARN ; ARNsi ou ARNmi, découverts dans les années 90 à partir d’organismes aussi humbles que le petit ver rond C. elegans, régulent, et de façon très semblable, l’expression post-transcriptionelle des gènes chez les eucaryotes.
Nouveaux outils de la biologie, ils contribuent à identifier la fonction des gènes, chez les organismes dont le génome a été séquencé, et ils suscitent le grand espoir, qui reste encore à confirmer au niveau clinique, de disposer à terme d’une nouvelle classe de médicaments.
Mais il apparaît que leur action ne s’arrête pas à la seule régulation de l’expression génique post-transcriptionnelle. Ils interviennent aussi au stade de la transcription et sont partie prenante dans la lutte contre les virus ; ils concourent à contenir les mutations induites par le déplacement des petits éléments mobiles que sont les transposons ; ils interviennent également dans la condensation de l’euchromatine en hétérochromatine…
Le chapitre de leur histoire commence tout juste à s’écrire.
Références
-
Dossier Pour la Science « Génome humain et médecine » (2005) 46.
Lau N. et Bartel D. La police du génome. 45-51.
Bachellerie J.P. et Cavaillé J. Les ARN sur tous les fronts. 52-57
Seitz H. et Cavaillé J. Des gènes furtifs. 58-63 -
Guo S. et Kemphues K.J. Par-1, a gene required for establishing polarity in C. elegans embryos, encode a pupative Ser/Thr kinase that is asymmetrically distributed. Cell. (1995) 81(4) :611-20.
-
Fire A., Xu S., Montgomery M.K., Kostas S.A., Driver S.E. et Mello C.C. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature. (1998) 391(6669) :806-11.
-
Pasquinelli A.E. et coll . Conservation of the sequence and temporal expression of let-7 heterochronic regulatory RNA. Nature. (2000) 408(6808) :86-9.
-
Elbashir S.M., Harborth J., Lendeckel W., Yalcin A., Weber K. et Tuschl T. Duplexes of 21-nucleotide RNAs mediate RNA interference in cultured mammalian cells. Nature. (2001) 411(6836) :494-8.
-
Zhang Y., Zhang Y.F., Bryant J., Charles A., Boado R.J. et Pardridge W.M . Intravenous RNA Interference Gene Therapy Targeting the Human Epidermal Growth Factor Receptor Prolongs Survival in Intracranial Brain Cancer. Clin Cancer Res. (2004) 10(11) :3667-77.
-
Tolentino M.J., Brucker A.J., Fosnot J., Ying G.S., Wu I.H., Malik G., Wan S. et Reich S.J. Intravitreal injection of vascular endothelial growth factor small interfering RNA inhibits growth and leakage in a nonhuman primate, laser-induced model of choroidal neovascularization. Retina. (2004) 24(1) :132-8.
Pour aller plus loin
- RNA interference : animation sur le site Nature Reviews
- Cours de biochimie, Université d’Angers : « L’interférence ARN »
- « Interférence ARN : utilisation thérapeutique et vectorisation », thèse de pharmacie, Boudaud David, 2018. Voir en particulier la partie 3 : « Médicaments utilisant l’interférence ARN, qui sont-ils et quels essais cliniques pour le marché pharmaceutique en 2018 ?». Cette partie de la thèse présente l’état actuel des études cliniques concernant des médicaments ciblant la mort des cellules rénales, la croissance tumorale, différents troubles ophtalmiques et l’ATTR (amylose héréditaire).