Une équipe de chercheurs vient de découvrir un système d’acheminement efficace permettant d’intégrer une ou plusieurs molécules d’ARN messager dans les cellules β des îlots de Langerhans du pancréas. Ils ont également montré que les macrophages sont essentiels à ce transfert.
Depuis quelques années, les recherches sur les thérapies fondées sur l’utilisation d’ARN messager s’accélèrent et les applications se multiplient. Le transfert de ces molécules fragiles et immunogènes dans des cellules cibles nécessite de trouver un système d’acheminement capable à la fois de protéger les molécules d’ARN messager, de les transporter et d’assurer leur libération dans le cytoplasme afin qu’elles y soient traduites en protéines. Actuellement, les recherches portent sur l’utilisation de nanoparticules lipidiques contenant, entre autres, des lipides ionisables (capables d’acquérir une charge positive lorsque le pH du milieu diminue) et des lipides auxiliaires (pouvant être neutres ou chargés positivement ou négativement). Ces molécules sont indispensables pour que les ARN messagers puissent s’échapper des endosomes et pénétrer dans le cytoplasme. Cependant, l’une des difficultés est de trouver une voie d’administration et une composition chimique qui permettent d’adresser ces vecteurs à un type cellulaire défini.
Le pancréas représente un organe vital de par ses fonctions endocrines et exocrines. Jusqu’à présent, le traitement des maladies d’origine pancréatique reposait principalement sur l’injection de vecteurs viraux à travers le conduit pancréatique. Outre les effets indésirables liés à leur utilisation (immunogénicité, matériel génétique viral susceptible de s’intégrer dans celui de la cellule hôte), le caractère invasif de cette méthode rendait aussi l’opération risquée.
En s’appuyant sur les connaissances actuelles, une équipe de chercheurs s’est fixée comme objectif de mettre au point un système d’adressage efficace et spécifique au pancréas 1. Pour cela, ils ont comparé l’efficacité des voies d’administration intrapéritonéale et intraveineuse et ont étudié l’influence de la composition en lipides ionisables et auxiliaires des nanoparticules. Dans chacune des expériences, des nanoparticules lipidiques contenant des molécules d’ARN messager codant la luciférase de luciole ont été injectées à des souris. L’observation de la luminescence permettait alors de visualiser les cellules ciblées par ces vecteurs lipidiques.
Les résultats ont montré que la luminescence est plus importante dans le pancréas lorsque les nanoparticules sont injectées par voie intrapéritonéale. Ils ont également permis de cibler un lipide ionisable favorisant l’adressage au pancréas. Enfin, après avoir testé l’effet de lipides auxiliaires présentant des charges différentes (lipides zwitterioniques, anioniques ou cationiques), il s’est avéré que les lipides cationiques favorisent le transfert des nanoparticules aux cellules du pancréas en réduisant leur adressage aux autres organes comme le foie, la rate ou les poumons.
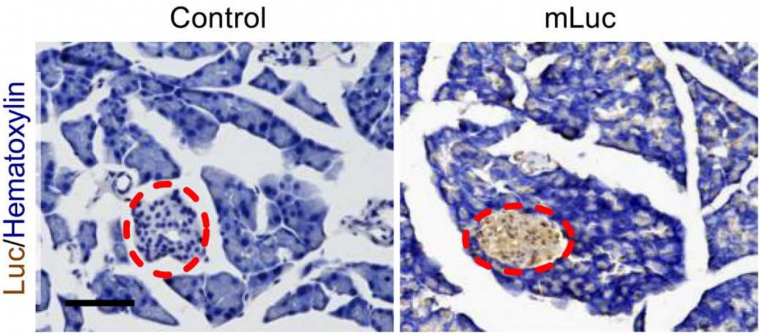
En complément de ces expérimentations, des analyses immunohistochimiques réalisées sur des coupes de pancréas ont révélé que les protéines codées par les ARN messagers des nanoparticules s’expriment très majoritairement dans les cellules β des îlots de Langerhans (Figure 1). Pour comprendre les mécanismes permettant le transfert de l’ARN messager aux cellules cibles, les chercheurs se sont intéressés à l’influence des cellules immunitaires abondantes dans la cavité péritonéale. Ils ont montré que les macrophages, par l’intermédiaire des vésicules d’exocytose qu’ils sécrètent, sont responsables du transfert des ARN messagers contenus dans les vecteurs lipidiques aux cellules β des îlots de Langerhans.
Des nanoparticules lipidiques contenant de l'ARNm codant la luciférase (mLuc) ont été injectés par voie intrapéritonéale à des souris. Les souris témoins ont été injectées avec une solution saline. Six heures plus tard, les souris ont été euthanasiées, et leurs pancréas fixés et congelés. Les lames minces ont été colorées à l'hématoxyline tandis que la luciférase est révélée par immunohistochimie. Les ovales rouges indiquent les îlots de Langerhans. Barre d'échelle : 100 µm.
Cette découverte offre de nombreux espoirs de traitements face à des maladies incurables comme certains cancers du pancréas ou encore les diabètes. En effet, les cellules β ne représentent qu’une très faible partie de la totalité des cellules pancréatiques mais jouent un rôle primordial dans le fonctionnement de l’organisme.