Des complexes protéiques qui permettent aux insectes de détecter une grande variété de composés volatils.
Notre capacité à comprendre le monde qui nous entoure dépend de protéines sensorielles spécialisées dans la détection de stimuli comme la lumière, la température et le toucher. Le plus grand groupe de protéines sensorielles est, de loin, constitué par les chimiorécepteurs, qui nous permettent de percevoir les saveurs et les odeurs. Chez les mammifères, le sens de l’odorat commence dans le nez, où les molécules en suspension dans l’air rencontrent des cellules spécialisées appelées neurones olfactifs. Chacun de ces neurones exprime un seul type de récepteur olfactif (sur un total estimé d’environ 400 récepteurs dans l’espèce humaine). Tous les récepteurs olfactifs des mammifères appartiennent à la superfamille des récepteurs couplés aux protéines G (RCPG). Une molécule odorante donnée se lie à un ensemble spécifique de récepteurs, entraînant l’activation d’un sous-ensemble de neurones olfactifs, ce qui aboutit finalement à la sensation d’une odeur particulière.
Comment les insectes sentent
Les insectes dépendent eux aussi fortement de l’odorat pour s’orienter au sein de leur environnement. Cependant, les insectes utilisent un mécanisme très différent de détection des molécules en suspension dans l’air. Le principal organe olfactif de nombreux insectes est constitué par leurs antennes, qui sont recouvertes de minuscules structures semblables à des poils, appelées sensilles. Les molécules odorantes pénètrent dans les sensilles olfactives par des pores, où elles interagissent ensuite avec des récepteurs olfactifs présents sur les neurones olfactifs.
Contrairement aux récepteurs olfactifs des mammifères, les récepteurs des insectes ne sont pas des récepteurs couplés aux protéines G (RCPG). Les récepteurs olfactifs des insectes font partie de la catégorie des canaux ioniques activés par les ligands, et sont constitués de quatre sous-unités. La liaison d’une molécule odorante ouvre le canal et permet l’entrée d’ions dans la cellule, conduisant à l’activation du neurone olfactif. Chez la plupart des insectes, les récepteurs olfactifs sont des complexes tétramériques composés de deux types de sous-unités : une sous-unité variable de liaison à la molécule odorante (appelée OR) et un corécepteur conservé connu sous le nom de Orco. Les gènes codant les sous-unités OR se sont rapidement multipliés et diversifiés au cours de l’évolution dans les différentes espèces d’insectes, au point de représenter l’une des familles de canaux ioniques les plus vastes et les plus divergentes dans la nature, avec potentiellement des millions de variants différents. Cette évolution rapide contribuerait à la capacité des insectes à s’adapter à des écosystèmes très divers.
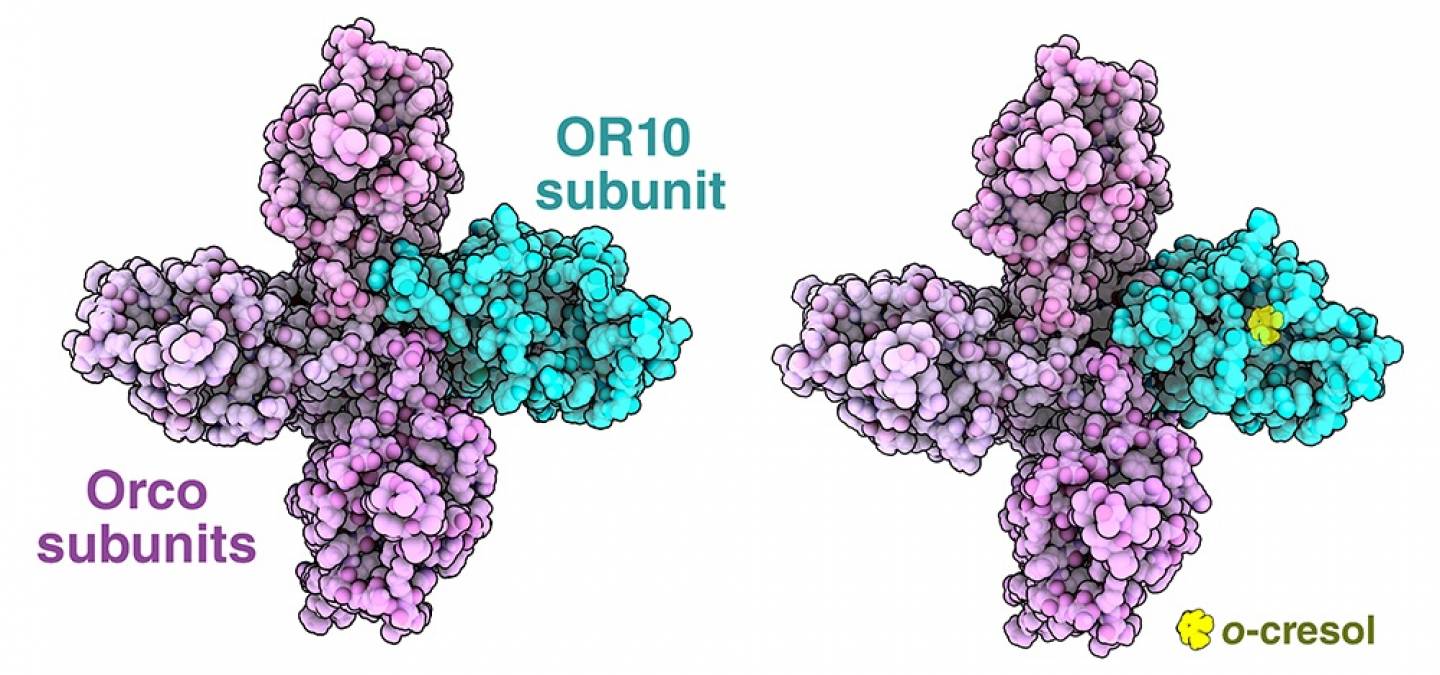
Bien qu’il ait été initialement supposé que les récepteurs olfactifs seraient construits sous forme de tétramères symétriques comprenant deux sous-unités OR et deux corécepteurs Orco, des études structurales récentes ont révélé des récepteurs asymétriques, constitués d’une sous-unité OR associée à trois sous-unités Orco 1 (comme le montrent les structures visibles sur la figure 1, construite à partir des entrées de la base de données des protéines (PDB) 8V00 et 8V02 ; des structures asymétriques similaires peuvent également être observées avec les entrées PDB 8Z9A, 8Z9Z, 8V3C et 8V3D).
Lorsqu’une molécule odorante se lie, elle s’insère dans une poche profonde et hydrophobe située dans la région transmembranaire de la sous-unité OR. Cette fixation provoque un changement de conformation de la sous-unité OR, qui ouvre le pore du canal et permet le passage d’ions. Il est intéressant de noter que les sous-unités Orco restent en grande partie immobiles au cours de ce processus, ce qui souligne le rôle central de la sous-unité OR dans la détection de molécules odorantes spécifiques.
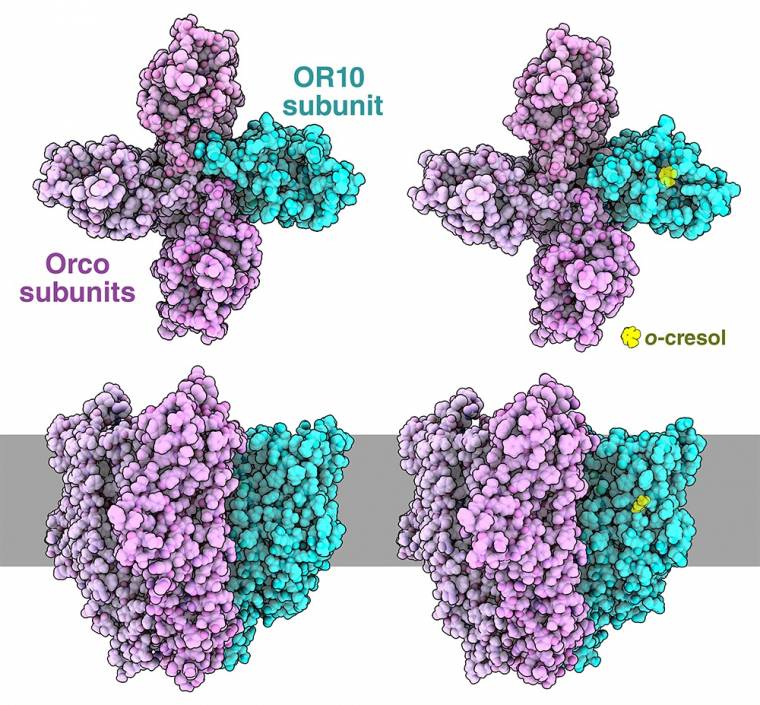
Les récepteurs olfactifs des insectes sont des canaux ioniques constitués de quatre sous-unités. Sur le canal représenté ici (entrées PDB 8V00 et 8V02), les sous-unités Orco sont représentées en rose, tandis que la sous-unité OR est en turquoise. Sur la droite, le récepteur est représenté en configuration ouverte après fixation d’un ligand, l’o-crésol (en jaune). En haut : vue du dessus ; en bas : vue de profil, avec le récepteur inséré dans la membrane plasmique (en gris)
Détecter une diversité d’odeurs
Alors que de nombreux insectes familiers, comme les mouches et les abeilles, expriment le corécepteur Orco et assemblent leurs récepteurs olfactifs sous la forme d’hétérotétramères, certaines lignées basales d’insectes sont totalement dépourvues de gènes Orco. Une espèce de machile, Machilis hrabei, un arthropode semblable au poisson d’argent et considéré comme appartenant à une branche ayant divergé précocement du reste des insectes, ne possède que cinq gènes codant des sous-unités OR et aucun gène Orco. Comparé à des organismes modèles d’insectes, comme la mouche du vinaigre Drosophila melanogaster, dont le génome code plus de 60 gènes OR, Machilis hrabei offre un système simplifié pour comprendre comment différentes substances odorantes peuvent être reconnues par les récepteurs.
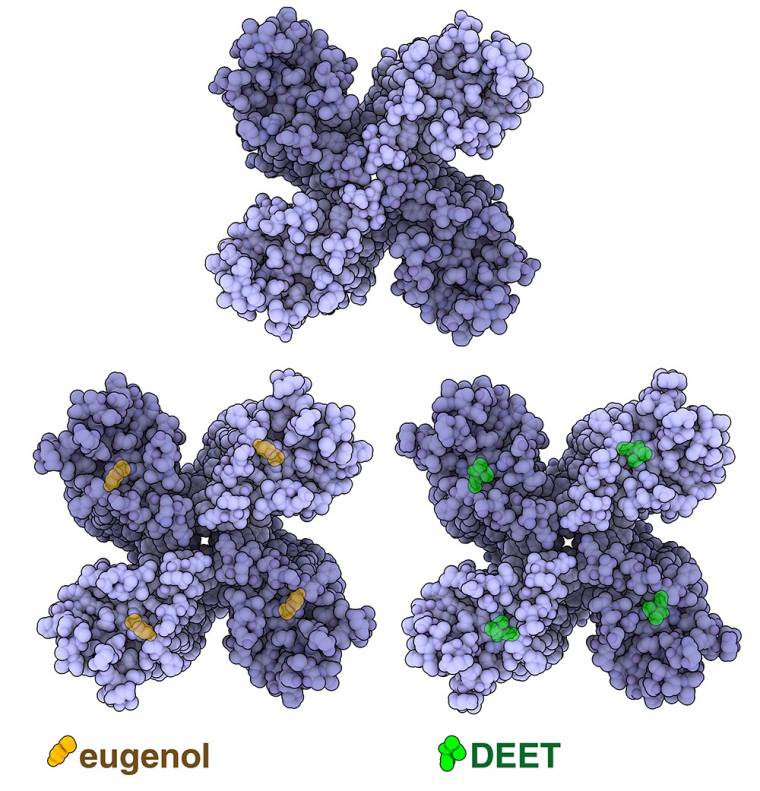
Les chercheurs ont constaté que les récepteurs olfactifs chez M. hrabei pouvaient être constitués de quatre sous-unités identiques, et que différents canaux variaient fortement dans leur sensibilité aux molécules odorantes 1. Alors qu’un récepteur constitué de quatre sous-unités OR5 (représentée sur la figure 2 à partir des entrées PDB 7LIC, 7LID et 7LIG) était activé en réponse à plus de la moitié des 54 molécules odorantes testées, y compris l’eugénol (le principal composant de l’huile de clou de girofle) et le DEET (un répulsif anti-insectes efficace), des canaux homomériques assemblés à partir d’autres sous-unités OR répondaient à un ensemble beaucoup plus restreint de substances odorantes 2. Les analyses structurales suggèrent que cette capacité à reconnaître des molécules diverses provient de la nature de la poche de liaison aux molécules odorantes. Plutôt que de reposer sur une interaction unique hautement spécifique, cette poche peut accueillir des molécules chimiquement distinctes grâce à de nombreuses interactions faibles hydrophobes.
Ces études mettent en évidence la flexibilité du système Orco/OR à former des complexes contenant un nombre variable de sous-unités OR au sein du clade des insectes. La question de savoir si les récepteurs olfactifs des insectes existent in vivo avec d’autres rapports de sous-unités Orco/OR constitue un domaine de recherche actif.
Comprendre comment les insectes détectent une diversité de signaux chimiques a des implications pratiques importantes. Les connaissances acquises sur ces mécanismes peuvent guider le développement de répulsifs plus sûrs et plus efficaces afin de réduire la propagation des maladies transmises par les insectes, ainsi que l’élaboration de stratégies visant à protéger les cultures contre les insectes ravageurs.
Certains récepteurs olfactifs d’insectes peuvent être activés par des molécules odorantes diverses
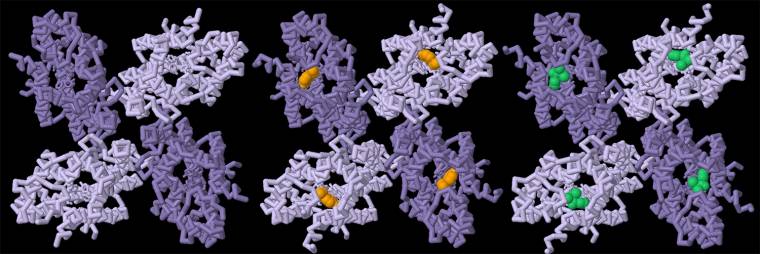
Vous pouvez examiner de plus près comment un seul récepteur olfactif d’insecte (un tétramère de OR5 provenant de Machilis hrabei) est capable de reconnaître deux molécules odorantes différentes dans la même poche de liaison en vous rendant sur la page de l’article d’origine (en anglais), et en cliquant sur l’onglet JSmol de la section Exploring the structure.
Une comparaison du récepteur homotétramérique OR5 seul ou ayant fixé l’eugénol (en jaune) ou le DEET (en vert). Les sous-unités OR5 sont représentés en violet.
Pour aller plus loin
- Vous pouvez en apprendre davantage sur les récepteurs olfactifs d’autres animaux, notamment chez les mammifères, dans un ancien article de la molécule du mois.
- Vous pouvez découvrir d’autres canaux ioniques, notamment le canal mécanosensible Piezo1, le récepteur à la capsaïcine TRPV1, les canaux potassiques et les canaux sodiques dépendants du voltage.
Ce texte correspond à la traduction par Cédric Bordi de l’article Molecule of the Month : Insect Odorant Receptors 1 écrit par Janet Iwasa en avril 2026 sur le site PDB-101, le portail éducatif de la base de données sur les protéines (PDB).