Présentation des modalités d'élevage du xénope, ainsi que des protocoles de réalisation d'une fécondation naturelle et d'une fécondation in vitro.
Introduction
Xenopus laevis, le crapaud à griffe ou dactylère du Cap, originaire d’Afrique australe, est un amphibien anoure de la famille des Pipidae. Il possède un mode de vie essentiellement aquatique, ne remontant à la surface de l’eau que pour respirer. Les femelles adultes mesurent une dizaine de centimètres du museau à l’anus (Fig.1).
 |
Les mâles sont toujours plus petits que les femelles. Parmi les caractéristiques de ces animaux, on note des pattes postérieures très musculeuses et garnies d’une large palmure. Cette disposition anatomique en fait d’excellents et puissants nageurs. De plus, les trois doigts internes des pattes postérieures portent des griffes cornées (Fig.2).
| Pour voir une animation cliquez sur l'image. |
La coloration de la peau est extrêmement variable d’un individu à un autre (Fig.3 et 4) et peut être modulée par l’éclairement de l’environnement et du substrat. Des souches albinos existent également (Fig.5).
 |
 |
 |
Élevage en laboratoire
Les adultes
Le mode de vie aquatique de ces animaux favorise leur élevage en laboratoire. À l’inverse de la plupart des autres amphibiens qui nécessitent l’aménagement d’un aquaterrarium, le xénope se satisfait d’un simple aquarium ou d’un bac dans lequel il vit en pleine eau. La contenance minimum d’un bac pour maintenir une quinzaine de femelles doit être de l’ordre de 50 litres (Fig.6).
 |
Chaque bac doit être recouvert d’un couvercle grillagé pour empêcher la fuite des animaux (leurs pattes musculeuses leur permettent de sauter hors des bacs) (Fig.7).
 |
L’eau d’élevage doit être dépourvue de chlore et la température maintenue à 22 °C. Il est préférable de consacrer à l’élevage, une pièce thermostatée à 24 °C de façon à corriger la déperdition de chaleur de l’eau des bacs. Cette pièce sera éclairée par un plafonnier en tubes fluorescents type Néon blanc Mazda Fluor SF36W/AZU965. L’alternance nycthémérale de l’éclairage sera assurée par une horloge avec une périodicité de 12h/12h.
On peut concevoir un planning hebdomadaire pour le maintien des adultes en élevage au laboratoire :
- Lundi
- Matin : alimentation : saupoudrage d’aliments complets pour poisson sous forme de granulés « Aqualife » N°6.
- Après-midi : nettoyage : les animaux de chaque bac sont tour à tour retirés et stockés temporairement à part. Les bacs sont vidés, nettoyés, grattés sans détergent à l’aide d’une éponge type « scotch brite », rincés abondamment et remplis avec une eau à 22 °C. L’eau est délivrée à la bonne température grâce à un ballon chauffe-eau thermostaté. Les animaux sont replacés dans leur bac d’origine.
- Mardi
- Matin et après-midi : repos des animaux, pas de renouvellement d’eau.
- Soir : distribution de granulés.
- Mercredi
- Matin : nettoyage, même protocole que pour le lundi après-midi.
- Après-midi : repos des animaux, pas de renouvellement d’eau.
- Jeudi
- Matin et après-midi : repos des animaux, pas de renouvellement d’eau.
- Soir : distribution de granulés.
- Vendredi
- Matin : nettoyage, même protocole que pour le lundi après-midi.
- Après-midi : repos des animaux, pas de renouvellement d’eau.
- Samedi et dimanche : repos des animaux, pas de renouvellement d’eau.
Les têtards
Dès que les larves sont capables de se nourrir, elles sont placées dans des aquariums à raison de 10 têtards par litre d’eau déchlorée (ou mieux, de l’eau de source) aérée par un bulleur. Les têtards sont microphages. Ils filtrent les boues déposées sur le fond de l’aquarium. Ces boues sont constituées par des décoctions d’orties séchées ou des poudres de potage du commerce (Knorr). On peut également ajouter un peu de levure de boulanger. Pendant leur activité de filtrage, les têtards adoptent une position stationnaire, le corps oblique, la tête tournée vers le fond de l’aquarium (Fig.8). Seule l’extrémité de la queue est animée d’un battement rapide pour maintenir l’inclinaison du têtard (voir Fig. 8).
| Pour voir l'animation cliquez sur l'image. |
Bien que le filtrage assuré par les têtards contribue à éclaircir l’eau de l’aquarium, il faut changer l’eau et nettoyer l’aquarium dès que les boues commencent à proliférer. Cette prolifération est le signe d’une fermentation préjudiciable à l’oxygénation des têtards.
Ces derniers atteignent la métamorphose deux mois et demie après la ponte. Pendant cette période les animaux ne se nourrissent plus. La métamorphose achevée, les jeunes grenouilles se nourrissent de proies vivantes adaptées à leur taille qui est de l’ordre du centimètre. Ce sont principalement des larves de chironomes couramment vendues dans les boutiques spécialisées en aquariophilie. L’élevage en laboratoire peut conduire à l’obtention d’animaux adultes. La maturité sexuelle apparaît environ un an après la fécondation pour une femelle et six mois pour un mâle. Cependant, il est préférable d’attendre un an et demie pour une femelle, et un an pour un mâle pour des raisons de dimension des animaux et de quantités d’œufs utilisables.
Pathologies
Elles sont peu nombreuses. Le xénope est plutôt résistant aux agents infectieux connus chez les amphibiens. Les atteintes bactériennes, fongiques ou parasitaires sont les plus communes.
L’infection la plus répandue est la « red leg septicemia » qui se manifeste par des lésions cutanées, des œdèmes sous-cutanés et une inflammation du réticule veineux peaucier notamment au niveau des pattes. Les agents infectieux sont bactériens tels que Aeromonas et Pseudomonas. Les animaux atteints doivent être isolés rapidement à cause du caractère contagieux de l’infection. Le traitement consiste en l’addition de tétracycline dans l’eau d’élevage à raison de 100 mg.mL-1 pendant une semaine.
Les atteintes fongiques peuvent survenir sur d’éventuelles plaies cutanées. Le traitement consiste en l’adjonction de produits antifongiques (vendus en aquariophilie) dans l’eau d’élevage.
D’une manière générale, la moindre plaie externe peut être traitée par un bain antiseptique à base d’éosine (Fig.9).
 |
Marquage
L’une des méthodes les plus simples est de couper des griffes aux trois doigts internes des pattes postérieures et de convenir d’un code tenant compte des différentes combinaisons, comme de lire les dizaines sur la patte de gauche et les unités sur celle de droite. L’inconvénient est que les griffes repoussent en quelques mois, ce qui nécessite d’entretenir le marquage. La méthode la plus sure est d’effectuer des autogreffes de la peau ventrale sur le dos de l’animal. Bien qu’un peu lourde à mettre en œuvre, cette méthode présente l’avantage de réaliser un marquage permanent et de varier les combinaisons en fonction de la forme des greffons et de leur lieu d’implantation.
Reproduction
Préparation des géniteurs
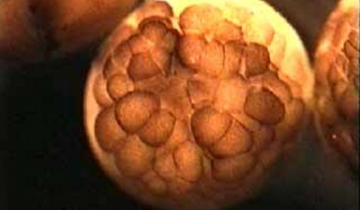
Le succès des amphibiens pour l’étude du développement embryonnaire tient aux dimensions importantes des œufs (entre 1 et 2 mm de diamètre), à leur développement externe qui le rend aisément accessible à l’observateur et au grand nombre d’œufs pondus comme chez le xénope (plusieurs centaines).
De plus, les embryons peuvent être obtenus artificiellement en induisant l’ovulation puis en pratiquant la fécondation in vitro.
Ovulation
L’ovulation peut être obtenue artificiellement avec des hormones gonadotropes du commerce. Afin de garantir le succès de cette opération, il est préférable de préparer plusieurs femelles. Celles-ci peuvent être stimulées tous les 3 mois dans des conditions d’élevage et d’alimentation optimales. L’ovulation est induite par l’injection d’hormone gonadotrope chorionique (Chorionic Gonadotropin, Sigma, 10.000 I.U. per vial, code CG-10) dans les sacs lymphatiques dorsaux. Selon le poids de l’animal, 500 à 700 unités d’hCG diluée dans un soluté de type sérum physiologique, sont injectées.
 |
L’injection est effectuée dans les sacs lymphatiques dorsaux (Fig.10). Le xénope comme tous les amphibiens, possède un espace entre la peau et le plan musculaire sous-jacent. Cet espace est divisé en compartiments séparés par des parois conjonctives ou septa. Il est rempli de liquide lymphatique et en communication avec le système circulatoire lymphatique. Cette disposition anatomique favorise l’injection et la diffusion des hormones dans l’ensemble du corps de l’animal. Afin d’éviter le reflux il est conseillé de piquer l’aiguille dans le haut de la cuisse à travers un septum et de serrer le lieu d’injection pendant quelques secondes au moment de retirer l’aiguille. Des glandes cutanées secrètent un mucus abondant qui enduit la peau et rend les animaux extrêmement glissants. Pendant toute cette manipulation, il est donc recommandé de tenir l’animal avec un chiffon sec pour éviter qu’il ne s’échappe (Fig.11).
 |
Les femelles en stimulation sont ensuite remises séparément dans un aquarium situé à l’écart et recouvert d’un couvercle faisant écran, dans une pièce isolée du passage des personnels afin d’éviter toute forme de stress qui risquerait de compromettre le succès de la ponte. Dans ces conditions, les animaux commencent à pondre une douzaine d’heures après la piqûre, à la température ambiante de 22 °C. Des œufs peuvent ainsi être obtenus tout au long de la journée, soit entre 6 et 10 heures.
Spermatogenèse
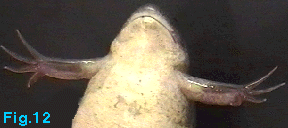
Elle est naturellement productive chez les mâles pourvus de caractères sexuels secondaires bien visibles tels que les callosités noirâtres des membres antérieurs (voir Fig. 12). Dans le cas contraire la spermatogenèse peut être stimulée chez le mâle par stimulation hormonale (deux injections d’hormone gonadotrope 50 I.U. à 24 heures d’intervalle).
Fécondation naturelle
Dans leur nature d’origine, les xénopes se reproduisent pendant le printemps austral. Dans nos régions ils peuvent s’accoupler naturellement en été et en automne à condition qu’ils trouvent des conditions d’élevage pseudo-naturelles dans des aquariums extérieurs (substrat graveleux, plantes aquatiques, nourriture abondante…). La reproduction peut être stimulée par un traitement hormonal approprié (voir ci-dessus).
Une fois stimulés, les animaux présentent des caractères sexuels secondaires. Les mâles à maturité portent des épaississements épidermiques pigmentés, kératinisés et rugueux sur la surface interne des membres antérieurs. Ce sont les callosités qui servent au mâle pour s’accrocher à la femelle au moment de l’accouplement (Fig.12).
 |
Les femelles possèdent deux papilles turgescentes qui encadrent le cloaque (Fig.13).
 |
L’amplexus est lombaire et la ponte peut durer plusieurs heures (Fig.14).
 |
La femelle expulse périodiquement des grappes de plusieurs dizaines d’ovocytes que le mâle arrose de sa semence simultanément. Les œufs fécondés peuvent être ainsi récoltés aisément sur le fond du bac à l’aide d’une pipette en verre avec une embouchure supérieure à 2 mm de diamètre. Cette méthode présente l’avantage d’être naturelle et ne nécessite pas de prélèvement chirurgical. Elle est conseillée pour une simple observation à usage éducatif.
Fécondation in vitro
À mesure que les ovocytes transitent par les voies génitales femelles, ils sont transitoirement accumulés dans la région distale de l’oviducte renflée. Il est alors possible de les récolter environ toutes les heures par lots de quelques dizaines voire une centaine. Pour ce faire, il faut saisir la femelle à pleine main de façon à la maintenir en contention tout en dirigeant le cloaque vers la coupelle où les œufs doivent être déposés (voir Fig. 15).
Cette manipulation, plutôt délicate, nécessite de la dextérité et un peu d’habitude. Les œufs sont entourés d’une gangue mucilagineuse qui colle au fond de la coupelle (Fig.16).
 |
La fécondation peut être effectuée selon deux protocoles différents :
-
En effectuant un broyat à partir de biopsies testiculaires dans un milieu de culture pour amphibien (MBS: Modified Barth’s Saline). Quelques gouttes de ce milieu de culture sont déposées sur les œufs (Fig.17). Le milieu peut être conservé au réfrigérateur pendant quelques heures.
 |
-
En appliquant sur la surface des oeufs, des fragments de biopsie testiculaire. La section du testicule libère des spermatozoïdes fécondants. Cette dernière méthode permet de conserver les fragments testiculaires plusieurs jours au réfrigérateur dans le milieu de culture. Les spermatozoïdes restant dans les tubes séminifères se conservent plus longtemps que dans la première méthode. Dès que les spermatozoïdes sont en contact avec les œufs, la coupelle est agitée énergiquement dans le plan horizontal (Fig.18) afin d’étaler les œufs en une monocouche sur le fond de la coupelle (Fig.19).
 |
 |
Environ 10 minutes après l’application des spermatozoïdes, la coupelle est remplie de MBS 0.1X. Les premiers signes de la fécondation s’observent dans les 20 minutes qui suivent l’entrée du spermatozoïde (voir De l’oeuf à la grenouille).
L’avantage de cette technique réside dans le fait que l’on peut obtenir des lots d’œufs fécondés au même moment et qui se développent de manière synchrone. Ceci est nécessaire dans le cadre de recherches fondamentales effectuées en laboratoire.
Gestion des femelles : Les femelles ayant pondu sont stockées dans un aquarium, à part des femelles prêtes à pondre. Il est recommandé de les marquer et d’enregistrer sur un répertoire d’élevage, la date de ponte, la quantité d’œufs produits, les pourcentages de fécondation et de développement. Ces données assurent la traçabilité des animaux. Une femelle ayant fourni des pontes en quantité et en qualité peut ainsi être suivie et remise à pondre tous les trois mois. Il est également conseillé de ne pas réutiliser les femelles dont la médiocrité des résultats est répétitive.
Attention !
La fécondation in vitro nécessite une biopsie du mâle. Bien qu’aisément réalisable sur un amphibien, une biopsie est cependant un acte chirurgical qui requiert légalement une habilitation. Celle-ci est accordée pour des laboratoires de recherche. Par contre, dans le cadre d’un établissement d’enseignement secondaire (lycées et collèges), la réalisation de la fécondation et l’observation du développement embryonnaire ne peuvent se concevoir qu’après accouplement des géniteurs stimulés ou pas, par des hormones gonadotropes.
Appendices
MBS (Modified Barth’s Medium)
On prépare deux solutions :
- 0,1 M CaCl2
- MBS 10X (NaCl / KCl / MgSO4)
A. 0.1 mol.L-1 CaCl2
- 11,1g/litre de CaCl2
- Stériliser et stocker en aliquots à – 20 °C
B. MBS 10X
- NaCl 880 mmol.L-1
- KCl 10 mmol.L-1
- MgSO410 mmol.L-1
- HEPES 50 mmol.L-1
- NaHCO3 25 mmol.L-1
- Ajuster le pH à 7,8 avec de la soude 1 mol. L-1
- Stériliser
La solution de MBS normale s’effectue en mélangeant 7 mL de la solution A avec 100 mL de la solution B. Ajuster à 1 litre avec de l’eau distillée. Pour éviter tout risque d’infection, il est conseillé d’ajouter un antibiotique (gentamycine) à raison de 50 mg.mL-1.
Commande
Pour des commandes, vous pouvez vous adresser au Centre de Ressources Biologiques "Xénope".
Crédits
Les images ont été réalisées à partir de prises de vues vidéo personnelles au service de Biologie du Développement de l’Université Pierre et Marie Curie (Fig 1 à 5 et 8 à 19), ainsi qu’à l’UMR 7622-Laboratoire de Biologie du Développement de l’Université Pierre et Marie Curie (Fig. 6 et 7).