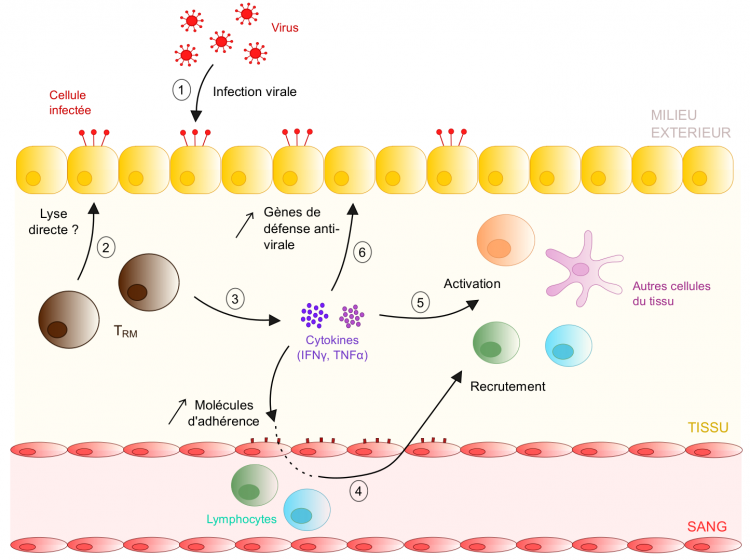
En cas de ré-infection du tissu (1), les TRM sont probablement capables de tuer directement les cellules infectées via leur forte expression d’enzymes lytiques comme le granzyme B - cela reste néanmoins à démontrer in vivo (2). En parallèle, suite à leur activation, les TRM sécrètent des cytokines comme l'IFNγ ou le TNFα (3). Ces molécules induisent différents mécanismes favorisant la mise en place de réponses immunitaires anti-virales efficaces. Premièrement, elles augmentent l’expression de molécules d’adhésion par l’endothélium vasculaire (e. g. VCAM-1), ce qui favorise le recrutement de lymphocytes circulants au sein du tissu infecté (4). Ensuite, elles induisent l’activation d’autres cellules immunes résidentes du tissu ( e. g. cellules dendritiques) ou des lymphocytes nouvellement recrutés (5). Enfin, la sécrétion cytokinique par les TRM favorise également l’expression de gènes anti-viraux par les cellules épithéliales (e. g. gènes codant pour des chimiokines et cytokines impliquées dans les réponses immunitaires innées), ce qui augmente leur résistance à l’infection virale (6).
Ainsi, les TRM déclenchent des cascades de réactions immuno-stimulatrices et anti-virales lors d’une ré-infection du tissu, favorisant une protection rapide et efficace contre le pathogène.