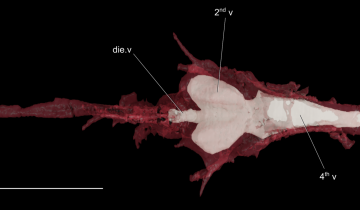
Protocole d'enregistrement de l'activité électrique d'un nerf de crabe.
Principe
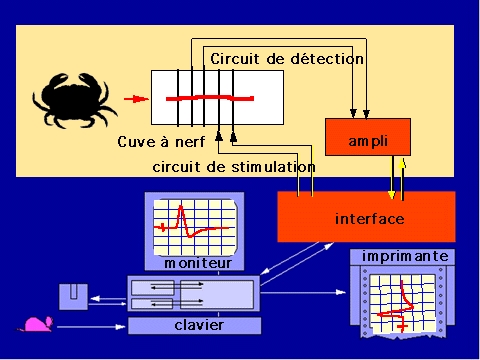
Lorsqu’un nerf est en activité, il est parcouru par des messages nerveux se traduisant par une activité électrique globale qu’il est possible d’enregistrer après l’avoir amplifiée. L’utilisation des animaux vertébrés étant prohibée dans l’enseignement, il est nécessaire d’utiliser des invertébrés pour étudier de façon pratique les réponses d’un nerf à des stimulations. Les crabes constituent un matériel approprié pour ce type de travaux en raison de la facilité à se procurer ces animaux à un faible coût et du peu de difficulté à isoler les nerfs sensorimoteurs des pattes locomotrices. Une fois le nerf disséqué et placé sur les électrodes d’une cuve à nerf, les réponses à divers types de stimulations électriques peuvent être visualisées sur un écran d’oscilloscope ou avec un système d’ExAO. Il est ainsi possible de déterminer le seuil d’excitabilité du nerf et de ses différents groupes de fibres, leur vitesse de conduction, les périodes réfractaires relatives et absolues, les réactions du nerf à des modifications de la composition du milieu de survie, etc. Le schéma ci-dessous montre les principes du montage expérimental.
 |
|
Plusieurs espèces de crabes peuvent être utilisées : crabe enragé, tourteau, étrille. Il est possible de se procurer des crabes vivants chez les marchands de poissons, sur les marchés et dans certains supermarchés. Il est également possible, quoique plus coûteux, de les commander auprès d’une station biologique. |
Dissection du nerf
-
Amputer l’animal de l’une de ses pattes locomotrices au niveau de l’articulation avec le thorax.
 |
 |
| Patte N° 5 de C. maenas | Patte N° 4 de C. maenas |
-
Saisir le troisième segment de la patte en partant de l’extrémité distale (carpopodite) dans la main gauche et le deuxième article (propodite) entre le pouce et l’index de la main droite.
 |
- Désarticuler soigneusement la patte entre les segments 2 et 3 par des mouvements de va-et-vient d’avant en arrière et de haut en bas.
 |
- Tirer lentement, régulièrement mais fermement en maintenant la base de la patte en position rectiligne. Le nerf sensorimoteur de la patte reste attaché aux segments 2 et 1.
 |
- Transférer le nerf attaché aux segments 2 et 1 dans du liquide physiologique pour nerf de crabe oxygéné (bullage d’air avec une pompe d’aquarium) et le laisser reposer au minimum une quinzaine de minutes.
 |
| Segments terminaux de la patte du crabe Carcinus maenas avec le nerf attaché. Noter la séparation du nerf en deux groupes de fibres (elle se produit spontanément dans le liquide physiologique et peut être prévenue par une ligature). |
- Au cours des manipulations, remettre le nerf dans ce milieu s’il cesse de répondre aux stimulations.
Remarques, trucs & astuces :
- Veiller à la bonne oxygénation du milieu de survie en y laissant buller de l’air.
- Vérifier le pH du milieu et l’ajuster à 7,2 – 7,4 le cas échéant.
- Veiller à maintenir une atmosphère humide dans la cuve en plaçant quelques gouttes de liquide physiologique au fond de la cuve qui doit être maintenue fermée.
- Si l’on désire empêcher la séparation des groupes de fibres dans le liquide physiologique, placer une ligature à l’extrémité distale du nerf.
Montage
- Installer le nerf sur les électrodes d’une cuve à nerf au fond de laquelle auront été placées quelques gouttes de liquide physiologique. Veiller à placer la partie du nerf encore raccordée au propodite du côté des électrodes excitatrices.
- Déposer une goutte de liquide physiologique au niveau des contacts entre nerf et électrodes.
- Fermer la cuve.
 |
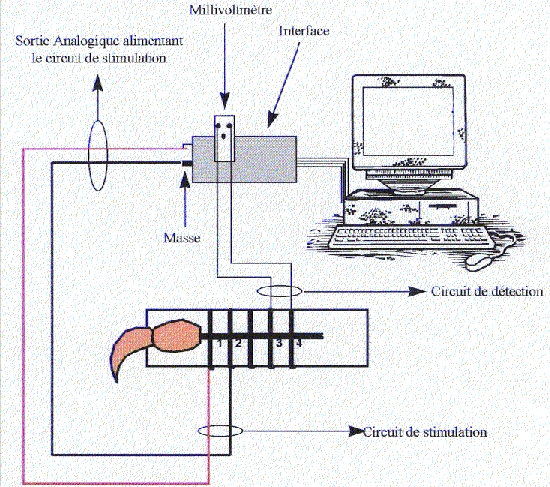
Remarque : Selon le type de matériel d’ExAO utilisé, les détails du montage peuvent varier. Toutefois, quel que soit le matériel, on placera les électrodes stimulatrices en « cathode descendante », c’est-à-dire avec l’électrode négative (cathode) placée entre l’électrode stimulatrice positive (anode) et la première électrode réceptrice.
 |
Résultats
Stimulation simple : superposition des réponses pour 3 stimulations d’intensité croissante.
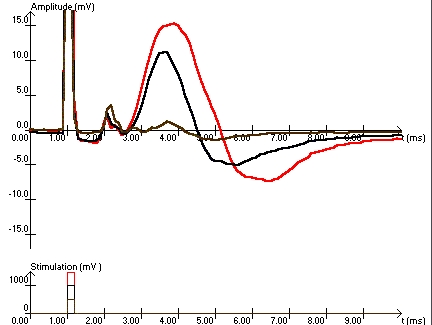 |
| Superposition des réponses pour 3 stimulations d'intensité croissante. |
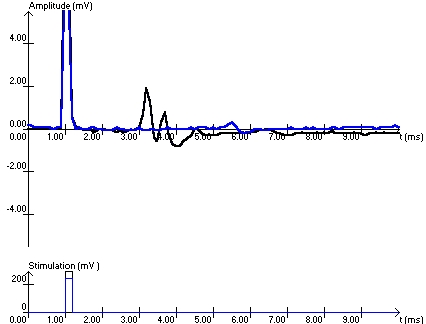 |
| Superposition des réponses pour une stimulation infraliminaire et une stimulation liminaire (noter la différence d'échelle avec les tracés précédents). |
Liquide physiologique
Tableau 1 : Composition du liquide physiologique
|
NaCl |
30 g |
|
KCl |
0,9 g |
|
CaCl2 2 H2O |
1,9 g |
|
MgSO4 7 H2O |
4,19 g |
|
Eau distillée |
Compléter à 1 litre |
|
pH à 7,2 – 7,4 |
Ajuster avec HCl ou NaOH dilués selon le pH obtenu |