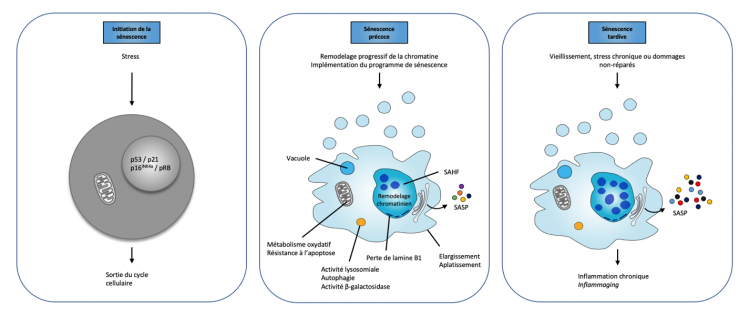
La sénescence est un état cellulaire initié par un stress et dont l’étape première est l’arrêt du cycle cellulaire en phase G1. S’ensuit alors une modification progressive de l’architecture chromatinienne initiée par une diminution de l’expression de la lamine B – permettant en temps normal la fixation de l’ADN au niveau de la membrane nucléaire – qui se matérialise par l’émergence des foyers d’hétérochromatine associés à la sénescence (SAHF, senescence-associated heterochromatin foci). Ces derniers sont caractérisés par les marqueurs d’hétérochromatine transcriptionnellement réprimée (e.g. di- et tri- méthylation sur la lysine 9 de l’histone H3 : H3K9me2/3).
La sénescence est un état cellulaire initié par un stress et dont l’étape première est l’arrêt du cycle cellulaire en phase G1. S’ensuit alors une modification progressive de l’architecture chromatinienne initiée par une diminution de l’expression de la lamine B – permettant en temps normal la fixation de l’ADN au niveau de la membrane nucléaire – qui se matérialise par l’émergence des foyers d’hétérochromatine associés à la sénescence (SAHF, senescence-associated heterochromatin foci). Ces derniers sont caractérisés par les marqueurs d’hétérochromatine transcriptionnellement réprimée (e.g. di- et tri- méthylation sur la lysine 9 de l’histone H3 : H3K9me2/3).
La sénescence est un état cellulaire initié par un stress et dont l’étape première est l’arrêt du cycle cellulaire en phase G1. S’ensuit alors une modification progressive de l’architecture chromatinienne initiée par une diminution de l’expression de la lamine B – permettant en temps normal la fixation de l’ADN au niveau de la membrane nucléaire – qui se matérialise par l’émergence des foyers d’hétérochromatine associés à la sénescence (SAHF, senescence-associated heterochromatin foci). Ces derniers sont caractérisés par les marqueurs d’hétérochromatine transcriptionnellement réprimée (e.g. di- et tri- méthylation sur la lysine 9 de l’histone H3 : H3K9me2/3).