Auteurs : Gérald Zabulon, Chantal Guidi-Rontani
Laboratoire "Organisme photosynthétiques et environnement" FRE2433 du CNRS, Ecole Normale Supérieure de Paris
Adaptation et mise en ligne : Gilles Furelaud, Gilles Camus
Table des matières
- Introduction
- Bacillus anthracis, un pathogène
- La lutte contre B. anthracis par antibiothérapie
- L'internalisation des toxines : une cible pour de nouvelles thérapies
- Autres stratégies thérapeutiques
- Bilan
- Références et liens
1. Introduction
Lors de tout cycle de pathogénicité microbienne, les micro-organismes se voient confrontés aux mécanismes de défense de l’hôte. Pour survivre, il leur est impératif de modifier les fonctions des cellules de ce dernier. Cette “modification” peut prendre deux aspects : soit les micro-organismes parviennent à créer un environnement cellulaire favorable à leur établissement et peuvent dès lors se multiplier et persister dans l’hôte, soit ils bloquent les fonctions vitales de la cellule, entraînent la "maladie", voire la mort de l’hôte et sont ainsi transmis d’hôte en hôte.
La virulence d'un pathogène est sous la dépendance de trois facteurs :
- le pouvoir infectieux (la capacité à établir un foyer infectieux localisé) ;
- le pouvoir invasif (la capacité à se répandre dans les tissus voisins du foyer d'infection) ;
- et le pouvoir toxinogène (la capacité à produire des toxines, armes essentielles du pathogène capables d'empoisonner l'hôte).
Le présent document a pour objectif de présenter quelques approches thérapeutiques permettant de lutter contre un micro-organisme pathogène en contrant en particulier son pouvoir toxinogène. Nous utiliserons pour cela l'exemple d'une bactérie du genre Bacillus (bactérie en forme de bâtonnet) : Bacillus anthracis.
" ... at postquam cecidit Paridis Phoebique sagittis,
nunc certe, dixi, non est metuendus Achilles. "
OVIDE, Metamorphoses, XIII, v. 501-502.
" ... mais puisqu'il est tombé sous les flêches de Paris et de Phoebus,
Surement, je dis maintenant qu'Achille n'est plus à craindre. "
" ... but when he fell by Paris' and Phoebus' arrows,
Surely, I said now is Achilles to be feared no more. "
2. Bacillus anthracis, un pathogène
2.1. Le bacille de l'anthrax et la définition d'agent infectieux par Koch.
C'est en utilisant Bacillus anthracis comme modèle biologique que Robert Koch a pu définir, en 1876, "l'agent infectieux d'une maladie".
Pour cela, Koch a émis quatre postulats :
- L'agent infectieux est présent chez tous les individus présentant la pathologie.
- L'agent infectieux peut être cultivé.
- L'agent, lorsqu'il est introduit chez l'hôte ou dans un modèle s'en rapprochant, induit le développement de la pathologie.
- Il est possible d'isoler à nouveau l'agent infectieux à partir d'un animal présentant la pathologie.
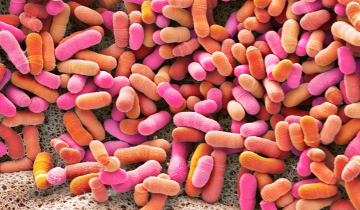
Bacillus anthracis est un bacille immobile, toxinogène, sporulant en aérobiose, à Gram-positif. Il est l'agent étiologique de la maladie du charbon ou anthrax. L'anthrax est une zoonose (maladie animale contagieuse) touchant principalement les mammifères. Bien que rare et sporadique dans la plupart des pays industrialisés, elle représente un problème de santé publique mais aussi un problème économique dans les pays en voie de développement. Enfin, B. anthracis constitue une menace sérieuse, étant potentiellement utilisable comme arme biologique.
 |
|
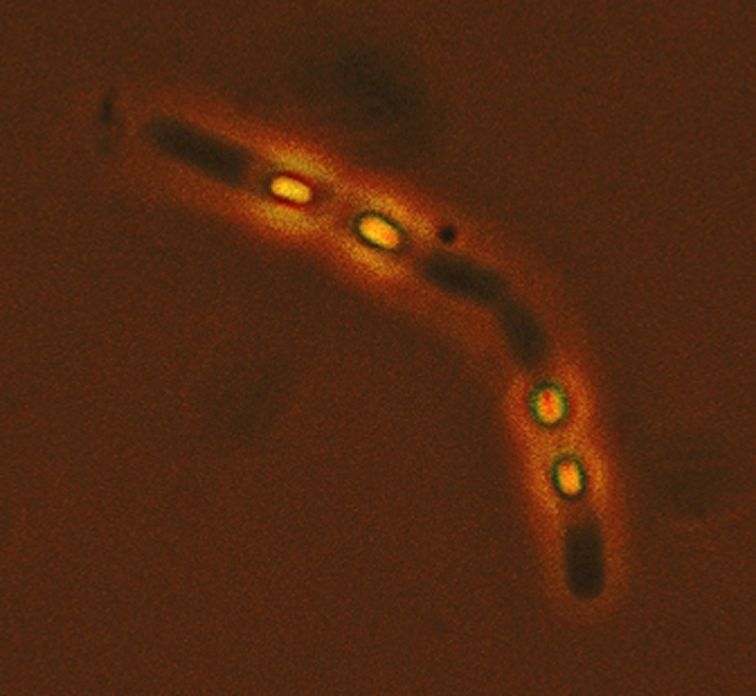
Analyse temporelle de la formation de pré-spores ovoïdes (de l'ordre de 500 nm) de Bacillus anthracis incluses dans le cytoplasme de leur cellule mère. Le suivi de l'expression de gènes impliqués lors du processus de sporulation est réalisé par microscopie à épifluorescence à l'aide d'un gène rapporteur (ici gène codant pour la β-galactosidase). Les bactéries Bacillus anthracis sont reconnaissables à leur forme en batonnet. Photo : Chantal Guidi-Rontani |
2.2. B. anthracis, une bactérie dangereuse pour l'Homme
La découverte de la formation de spores (taille de 1 à 5 μm) par le bacille du charbon, formation résultant de conditions hostiles de l'environnement pour la bactérie, a été une découverte clé en microbiologie. Les spores peuvent persister dans le sol infecté pendant de longues périodes (les spores du genre Bacillus ont une demie-vie de l'ordre de 100 ans) assurant de fait la perpétuité de l'espèce. D'autre part, celles-ci sont hautement résistantes à une exposition prolongée à de nombreux stress : température, ultraviolet, dessiccation, présence de solvants, pH et radiation. La spore de B. anthracis est toujours la forme infectante et peut infecter l'hôte par voie cutanée, digestive ou respiratoire. De ce fait, il n'y a pas de transmission inter humaine. Parmi les différentes voies d'infection de B. anthracis, l'inhalation de spores est l'infection la plus sévère : celle-ci s'accompagne en effet d'une rapide évolution et présente toujours un caractère funeste (avec une période d'incubation estimée de 1 à 14 jours, et un maximum de 43 jours).
La pathogénicité de B. anthracis est en particulier due à la production par cette bactérie de deux toxines : la toxine oedématogène, et la toxine létale.
- La toxine oedématogène est ainsi nommée car induisant des oedèmes chez le cobaye. Elle possède une activité de type adénylate cyclase (formation d'AMPcyclique).
- La toxine létale est nommée ainsi car directement responsable des symptômes du choc septique conduisant à la mort de l'individu infecté.
Ces deux toxines sont formées chacune de deux protéines secrétées. Une de ces deux protéines est commune aux deux toxines.
| Protéine | Structure | Fonction | Toxine | Fichiers | |
|
EF Facteur oedématogène (767 acides aminés) |
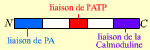 |
Activité adénylate cyclase : hausse de l'AMPc intracellulaire, d'où une activation incontrôlée des kinases AMPc-dépendantes cellulaires. (cette activité est dépendante du calcium, via la Calmoduline) |
EF+PA Toxine oedématogène |
Structure 3D : 1K8T.pdb |
 |
|
PA Antigène Protecteur (735 acides aminés) |
 |
Permet l'internalisation du facteur (EF ou LF) avec lequelle elle est associée |
Structure 3D : 1ACC.pdb |
 |
|
|
LF+PA Toxine létale |
|||||
|
LF Facteur létal (776 acides aminés) |
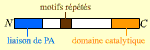 |
Métalloprotéase à Zinc qui conduit à la surexpression de cytokines par les macrophages |
Structure 3D : 1JKY.pdb |
 |
2.3. B. anthracis, une arme biologique potentielle
Aussi, le caractère extrêmement résistant des spores suggère une possible utilisation de B. anthracis comme arme biologique. Le Département de la Défense des Etats-Unis estime que la dose de spores suffisante pour provoquer le décès de 50% des malades (LD50) est de 8 000 à 10 000 spores inhalées. Une politique de vaccination animale existe depuis 1939, le premier vaccin humain n'ayant été développé qu'en 1954. Toutefois, il est clair qu'une politique de protection efficace à une menace bio terroriste ne peut être construite sur un plan de lutte basée sur la vaccination. En effet :
- la vaccination ne répond pas à une prophylaxie de type post-exposition ;
- il est impossible d'évaluer les risques d'exposition humaine dans le cas d'une menace d'origine criminelle ou bio terroriste ;
- la vaccination massive des populations est irréalisable.
Aussi, face au défi émergent du bio terrorisme, il est d'importance de définir des stratégies de lutte contre B. anthracis, prophylaxie de type post-exposition. Afin d'élaborer de nouvelles molécules effectrices pharmacologiques, les chercheurs doivent tirer avantage de l'élucidation des mécanismes moléculaires et cellulaires impliqués lors des étapes précoces de l'infection et ainsi entreprendre la quête du "Talon d'Achille" de B. anthracis. Nous allons voir comment la compréhension des mécanismes moléculaires et cellulaires de la virulence impliqués lors du processus d’invasion et de dissémination de B. anthracis permet l'identification de cibles moléculaires pour des thérapies de la maladie du charbon ou "anthrax".
3. La lutte contre B. anthracis par antibiothérapie
La pénicilline G, la doxycycline (les cyclines), et la ciprofloxacine (les fluoroquinolones) restent les antibiotiques de choix du traitement de toutes les formes de l'anthrax. B. anthracis colonise l'hôte en associant une septicémie (forme d'infection caractérisée par la présence d'un micro-organisme dans le sang) à une toxémie (intoxication généralisée causée par des toxines ou d'autres substances créées par un agent infectieux), les deux composants de l'anthrax systémique.
La germination des spores, à savoir l'émergence rapide de la forme végétative est une étape clé lors de la phase précoce de l'infection. La forme végétative survit comme pathogène extracellulaire (dans le flux sanguin), et évite l'ingestion par les macrophages de l'hôte. Les composants qui contribuent à l'inhibition de la phagocytose sont, d'une part un constituant externe de la bactérie (la capsule) constituée d'un polymère d'acide γ-D-glutamique, et d'autre part l'activité adénylate cyclase de la toxine oedématogène. B. anthracis est sensible à la pénicilline et autre β-lactamines composants. Aussi, une antibiothérapie précoce est efficace pour prévenir la maladie du charbon chez les personnes exposées (Fig. 2, bulle I). La ciprofloxacine, la doxycycline et la pénicilline G ont été approuvées par la "Food and Drug Administration" (FDA) pour la prophylaxie antibiotique contre la maladie du charbon sur la base de données pharmacocinétiques et pharmacodynamiques menées sur des animaux (efficacité du médicament, sensibilité de l'organisme, effets secondaires...). "US public health guidelines" préconise une durée optimale de traitement de soixante jours pour toute personne potentiellement exposée.
Malheureusement, les antibiotiques présentent un champ d'activité de courte durée au cours de l'infection : efficaces contre les formes végétatives de B. anthracis, ils n'ont aucune action contre les spores. De plus, depuis quelques années, les suppositions de Alexander Fleming datant de 1945 deviennent réalité : "Cela aboutirait à ce qu'au lieu d'éliminer l'infection, on apprenne aux microbes à résister à la pénicilline et à ce que ces microbes soient transmis d'un individu à l'autre jusqu'à ce qu'ils en atteignent un chez qui ils provoquent une pneumonie ou une septicémie que la pénicilline ne pourra pas guérir". En effet, nous observons l'émergence de souches de B. anthracis résistantes aux antibiotiques (souches pénicilline-résistantes). Cette évolution constitue une grave menace.
Les effets pernicieux de ce germe sont la conséquence de la production de deux exotoxines (toxines secrétées) : la toxine oedématogène et la toxine létale. Il est donc crucial de définir de nouvelles stratégies afin de bloquer spécifiquement les activités de ces toxines, déterminants majeurs de l'infection, et ainsi parvenir à une prophylaxie adéquate et efficace de l'anthrax.
4. L'internalisation des toxines : une cible pour de nouvelles thérapies
4.1. Les toxines de B. anthracis
Les toxines de B. anthracis, la toxine oedématogène (EdTx) et la toxine létale (LeTx) sont composées chacune de deux protéines sécrétées dont l'une est commune aux deux toxines. Les trois protéines sont appelées antigène protecteur (PA, 83 kDa de masse molaire), facteur létal (LF, 83 kDa) et facteur oedématogène (EF, 89 kDa). Séparément chacun des trois composants est totalement inactif in vivo et in vitro. Deux de ces protéines (EF et LF) ont une activité toxique qui ne peut s'exercer que par l'intermédiaire de la troisième protéine, l'antigène protecteur (PA).
Les combinaisons PA-EF et PA-LF constituent respectivement :
- la toxine oedématogène, une adénylate cyclase dont l'activité nécessite la présence d'une protéine exclusivement eucaryote, la calmoduline ;
- la toxine létale, une métalloprotéase à zinc capable de couper les MAP kinases kinases (MAPKK1, 2, 3, 4, 6 et 7) qui constituent un des trois modules de la chaîne d'activation MAPK responsable du transfert d'informations extérieures à la cellule vers le noyau au niveau transcriptionel.
Afin d'exercer leur activité enzymatique, LF et EF doivent être transportés au sein du cytosol via PA.
4.2. Processus d'intoxication par les toxines
 |
|
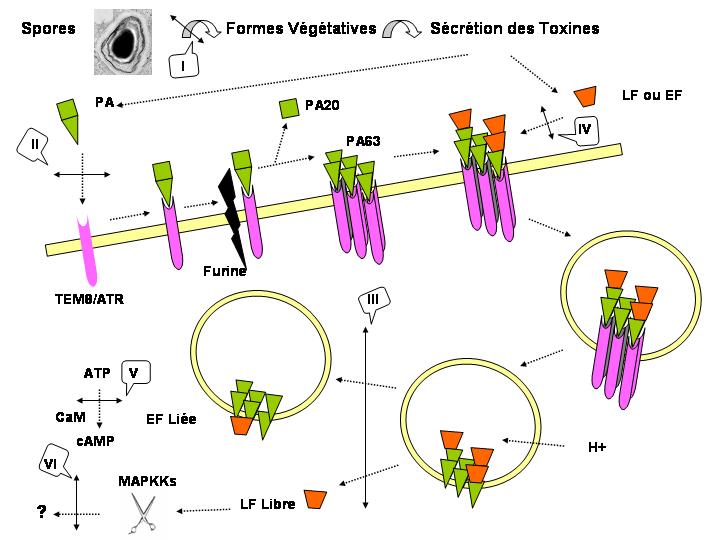
Après fixation sur le récepteur "tumor endothelium marker 8" (TEM8)/ATR (en violet) de la membrane cellulaire (en jaune), la molécule native PA (en vert) subit une protéolyse limitée par la furine, au site consensus R164KKR, en deux polypeptides de 20 kDa (PA20) et 63 kDa (PA63). Les fragments PA63 peuvent alors s'associer spontanément pour former un heptamère et interagir avec EF ou LF (en orange). Trois molécules de LF et/ou EF peuvent se fixer par heptamère de PA63. L'internalisation de ces complexes, permettant de délivrer le facteur létal LF et le facteur oedématogène EF au sein du cytosol des macrophages à partir des vésicules de l'endosome précoce, est réalisée via un processus "clathrin-dependent". LF et EF adoptent des stratégies différentes afin d'exposer leur site catalytique au sein du cytosol : LF est totalement libéré dans le cytosol; EF reste associé à la membrane endosomiale. Les flèches numérotées avec les bulles de I à VI indiquent les étapes moléculaires correspondant à une cible thérapeutique potentielle (explications dans la suite du document). |
4.3. Les cibles thérapeutiques potentielles
Une approche thérapeutique attractive est de bloquer spécifiquement la translocation de LF et de EF au sein du cytosol. En effet, nous savons combien le secret de l'extraordinaire létalité de la plupart des toxines ne réside pas autant dans l'efficacité enzymatique de leur domaine catalytique que dans les mécanismes de reconnaissance et d'internalisation au sein des cellules cibles. Afin d'atteindre ce but, différentes stratégies sont proposées.
4.3.1. Mutations de l'antigène protecteur
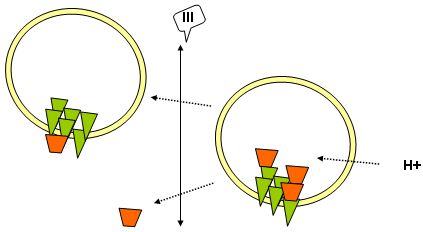 |
L'inhibition spécifique de la translocation de LF et EF peut être réalisée en créant des mutations de PA telles que des mutants dominants négatifs (Fig. 2, bulle III).
De tels mutants de PA sont capables de co-oligomériser avec les molécules de PA natives mais ne permettent plus l'association avec LF ou EF et de ce fait bloquent toute entrée de LF ou de EF au sein du cytosol.
4.3.2. Inhibition de la fixation de l'antigène protecteur sur son récepteur
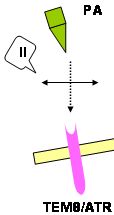 |
Une seconde approche intéressante est d'inhiber spécifiquement la fixation de PA sur son récepteur cellulaire via des techniques d'ingéniérie d'anticorps monoclonal anti-PA (Fig. 2, bulle II).Une immunothérapie basée sur ces anticorps, possédant une haute spécificité, a été proposée pour une prophylaxie à moyen terme de l'infection
4.3.3. Inhibition de l'interaction facteur protecteur - facteurs létal et oedématogène
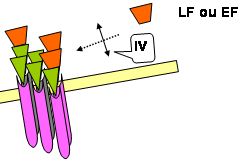 |
Enfin, le groupe de John Collier (Harvard Medical School, Department of Microbiology and Molecular Genetics) a démontré que l'interaction entre la protéine PA et les protéines LF/EF peut être inhibée par un inhibiteur synthétique polymérique polyvalent. La sélection de peptides, à partir d'une librairie, a permis d'identifier des candidats capables de se fixer sur la sous unité de l'heptamère, formé par PA63, responsable de la fixation de LF ou de EF et ainsi prévenir l'interaction de PA63 avec LF ou EF (Fig. 2, bulle IV).
Ces découvertes fournissent des outils moléculaires afin de perfectionner notre compréhension de la pathogénèse de l'anthrax et donnent de nouvelles clés pour la définition de nouvelles thérapies.
5. Autres stratégies thérapeutiques
5.1. Inhiber les activités enzymatiques des toxines
La structure tridimensionnelle de chacune des protéines composant les toxines, obtenues récemment, fournit un excellent point de départ afin de développer des inhibiteurs spécifiques des activités enzymatiques des toxines.
La découverte de l'activité enzymatique de la toxine létale, une métalloprotéase à zinc, est une piste à suivre lors de la recherche de nouvelles approches pharmacologiques.Toutefois, malgré la mise au point de méthodes sensibles testant la sensibilité aux inhibiteurs des protéases, l'identification d'inhibiteurs spécifiques de LF n'a pu aboutir.
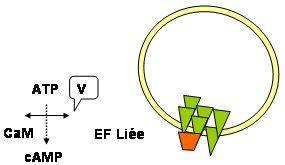 |
Par l'étude de la structure tridimensionnelle du site catalytique de EF, Soelaiman et collaborateurs (Université de Chicago, Ban-May Institute for Cancer Research) ont pu identifier des inhibiteurs spécifiques de l'activité adenylate cyclase de EF : dérivés appartenant à la classe chimique de la quinazoline, ethyl 5-aminopyrazolo[1, 5-a]quinazoline-3-carboxylate (Fig. 2, bulle V).
Il est à noter que lorsqu'elle est injectée en sous-cutanée, la toxine oedématogène native provoque chez l'animal un important oedème. L'aspect des lésions cutanées, recouvertes d'une croute noirâtre, et l'exsudation par les orifices naturels d'un sang noir, poisseux et incoagulable à la mort de l'animal, expliquent le nom de la maladie. Des souches déficientes pour l'adenylate cyclase ont une virulence atténuée (de 10 fois).
5.2. Cibler les cytokines pro-inflammatoires
Le facteur létal LF, essentiel dans la maladie du charbon, est le facteur responsable de la létalité. Malgré de nombreux progrès concernant, d'une part la relation entre la structure et les fonctions de la protéine LF, et d'autre part l'indentification de cibles cellulaires potentielles, le mécanisme intime de la cytotoxicité due à la toxine létale reste non résolu. LF, une métalloprotéase à zinc, déclanche une cascade de remaniements physiologiques et biochimiques. Comme décrit précédemment, la cascade des MAP kinase (MAPK) est la première cible. Hanna et collaborateurs ont démontré la surproduction des cytokines pro-inflammatoires : interleukine 1 (IL1), le "tumor necrosis factor" (TNFα), et l'interleukine 6 (IL6) par les macrophages in vitro. Il est à noter que la voie de signalisation impliquant les MAP kinase kinases (MAPKKs) est directement responsable de la production des cytokines (par exemple la biosynthèse du TNFα, de l'IL1 et de l'IL6 par le macrophage). Hanna et collaborateurs ont reporté la protection des souris de la toxicité létale par (1) une immunisation passive contre IL-1 et TNFα ou (2) une injection d'un antagoniste du récepteur de l'IL-1.
Ces résultats impliquent que le choc septique, observé dans la maladie et responsable de la mort de l'hôte, pourrait résulter essentiellement de la stimulation des cellules de l'inflammation par la toxine létale via la libération des cytokines (IL-1 et TNFα...)
 |
Hanna et collaborateurs proposent d'améliorer l'issue de l'infection via des traitements anti-médiateurs tels que des anti-TNF ou des anticorps monoclonaux (Fig. 2, bulle VI).
5.3. Antioxydante, une voie à suivre
Lors d'une seconde étude, Hanna et collaborateurs ont proposé que le stress oxydant (mécanisme de défense cellulaire) pourrait représenter une composante essentielle dans la maladie du charbon. Les résultats obtenus dévoilent une augmentation du métabolisme oxydant, à savoir des radicaux libres, par le macrophage après intoxication par la toxine létale :
- en présence d'agents anti-oxydants exogènes tels que le β-mercaptoethanol (BME) ou le dithiothreitol (DTT), de solvants organiques qui piègent les radicaux libres (éthanol, DMSO) ou des "dévoreurs d'oxygène" (mépacrine), la cytotoxicité résultant de l'action de la toxine létale est antagonisée ;
- les macrophages issus de patients atteints de granulomatose septique chronique ou CGD, macrophages dont l'activité du complexe de la NADH oxydase est abolie et donc incapable de produire des anions superoxydes (O2-) sont complètement résistants à la toxine létale.
Il est à noter que les radicaux libres, "reactive oxygen intermediate" (ROIs) et "reactive nitres intermediates" (RNIs), sont toxiques pour la cellule qui les produit si ceux-ci atteignent le cytosol de la cellule. Leur production doit donc être, d'une part restreinte aux compartiments oxydants tel que le phagosome, et d'autre part finement régulée afin d'éviter une surproduction et une diffusion vers le cytosol de la cellule. Les antioxydants sont donc de sérieux candidats pour une thérapeutique de l'anthrax due à leur capacité à antagoniser LF (Fig. 2 bulleVI).
6. Bilan
Une meilleure compréhension des mécanismes moléculaires et cellulaires qui composent le scénario de la toxicité de B. anthracis a permis d'identifier de nouvelles cibles moléculaires. Ces découvertes devraient permettre d'optimiser une thérapeutique de l'anthrax.
L'issue finale sera de comprendre comment B. anthracis interagit avec les cellules sentinelles, telles que les cellules dendritiques, afin de briser les défenses de l'hôte et mener à terme son scénario de toxicité.
7. Références et liens
P.C. Hanna et collaborateurs sont à University of Michigan Medical School, 5641 Med Sci II, Ann Arbor, MI 48109-0620.
- C. Guidi-Rontani "The alveolar macrophage : The Trojan horse of Bacillus anthracis". Trends in Microbiology (2002) 10:405-409.
- C. Guidi-Rontani and M. Mock "Macrophage Interactions". Current Topics in Microbiology and Immunology "Anthrax" Edit. T.M. Koehler, Springer-Vertag, Heidelberg, New York, (2002) 271.
- S. Soelaiman, B.Q. Wei, P. Bergson, Y-S. Lee, Y. Shen, M. Mrksich, B.K. Shoichet and W-J. Tang "Structure-based inhibitor discovery against adenylyl cyclase toxins from pathogenic bacteria that cause anthrax and whooping cough". J. Biol. Chem. (2003) 278(28):25990-25997.
- P.C. Hanna, D. Acosta and R.J. Collier "On the Role of Macrophages in Anthrax". PNAS (1993) 90(21):10198-10201.
- P.C. Hanna, B.A. Kruskal, R.A. Ezekowitz, B.R. Bloom and R.J. Collier "Role of macrophage oxidative burst in the action of anthrax lethal toxin" Mol. Med. (1994) 1(1):7-18.
- Bacillus anthracis and anthrax (En anglais. Site de Kenneth Todar University of Wisconsin-Madison Department of Bacteriology).
- Bacillus anthracis (Dictionnaire de Bactériologie Vétérinaire).
- Bacillus anthracis, agent causal de l'anthrax (Site web techmicrobio)