Article présentant les différentes étapes de la photosynthèse et des expériences réalisables en classe permettant de montrer le déroulement de celle-ci.
Analyse de résultats expérimentaux et de démonstrations célèbres : expériences d'Emerson, d'Engelman, de Ruben et Kamen...
Introduction
Les végétaux, organismes photoautotrophes, sont capables d’utiliser l’énergie lumineuse pour réaliser la synthèse de molécules organiques, à partir de composés minéraux. L’ensemble de ces réactions est regroupé sous le terme de photosynthèse.
La photosynthèse est réalisée par des organismes autotrophes au carbone, grâce à des pigments particuliers, et peut être découpée en deux groupes de réactions.
Le dossier aborde de manière succincte ces généralités sur la photosynthèse. Il s’agit essentiellement d’une version « abrégée » de l’ensemble de documents présents sur le site Biologie et Multimédia qui reprennent l’essentiel du module « Biologie et Physiologie végétales » de 2e année de l’Université Paris VI. Ce dossier « abrégé » reste donc bien évidemment incomplet. À tout moment, il est possible d’accéder aux documents complets, par les liens signalés.
Les organismes autotrophes au carbone
Autotrophie et hétérotrophie
Les êtres vivants sont composés d’eau et de sels minéraux, ainsi que de substances organiques. Ces dernières comportent glucides, lipides, protéines, acides nucléiques, etc. Or les composés organiques sont continuellement renouvelés (par dégradation et synthèse). Ce fonctionnement des êtres vivants nécessite des échanges constants de matière et d’énergie avec le milieu extérieur.
On peut ainsi distinguer différents types d’organismes en fonction de leurs besoins et de la source d’énergie utilisée.
- Les organismes hétérotrophes : ils sont incapables d’effectuer eux-mêmes les synthèses de leurs constituants à partir d’élément minéraux. Ils sont en général chimiotrophes, c’est-à-dire utilisant comme source d’énergie l’énergie chimique récupérée au cours de l’oxydation des composés organiques réduits présents dans leur alimentation.
- Les organismes autotrophes : ils sont capables d’utiliser des éléments inorganiques pour synthétiser leurs propres constituants organiques. Ils sont en général phototrophes, c’est-à-dire capables d’utiliser l’énergie lumineuse et de convertir cette énergie en étapes chimiques.
Voir sur le site BMédia : Chez les procaryotes, on peut trouver en fait des types trophiques bien plus complexes…
Organismes hétérotrophes et chimiotrophes
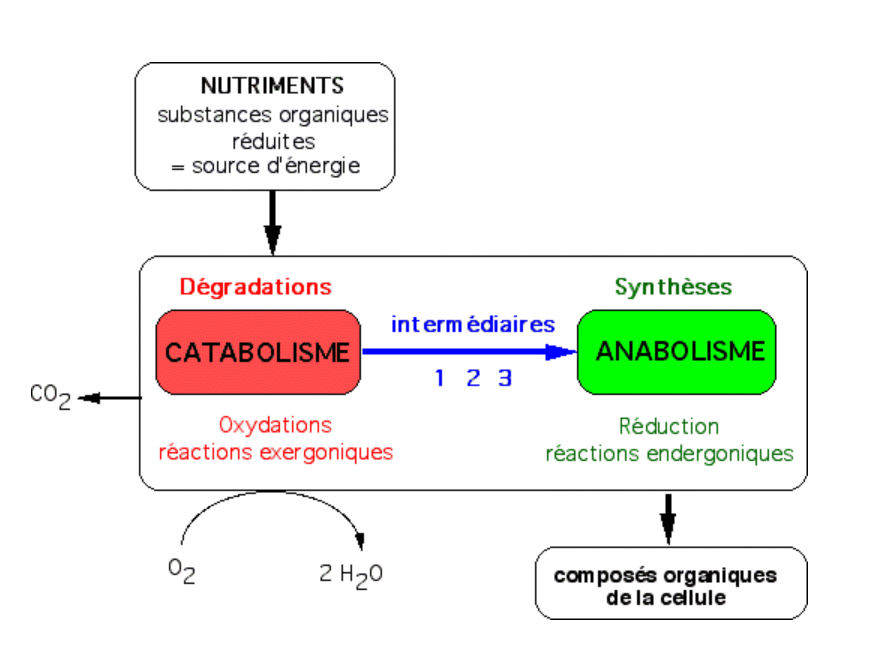
Il s’agit des animaux, des champignons, et de certains procaryotes (la bactérie E. coli par exemple). Ces organismes utilisent des substances organiques à la fois comme source d’énergie et comme source de pouvoir réducteur.
Les intermédiaires sont : 1 = ATP, intermédiaire énergétique ; 2 = NADH ou NADPH, coenzymes d’oxydo-réduction ; 3 = molécules du métabolisme intermédiaire (pyruvate, malate, acétylCoA, etc.).
Voir sur le site BMédia : Exemples d’organismes hétérotrophes / chimiotrophes.
Organismes autotrophes et phototrophes
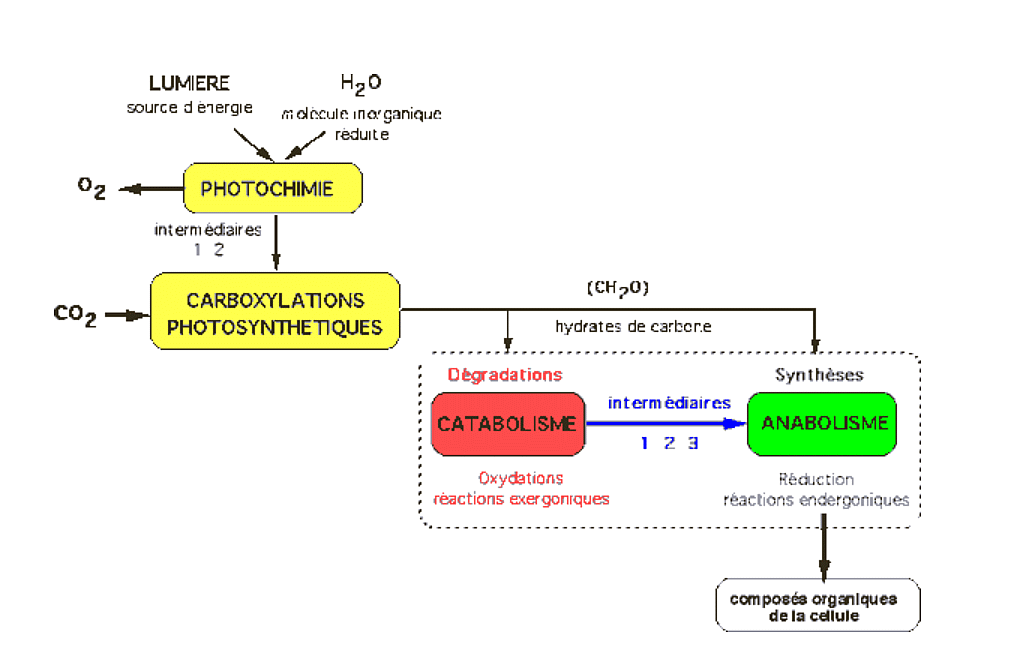
Il s’agit des végétaux chlorophylliens et de certains procaryotes. Ces organismes utilisent la lumière comme source d’énergie et l’eau comme pouvoir réducteur.
Les intermédiaires sont : 1 = ATP, intermédiaire énergétique ; 2 = NADH ou NADPH, coenzymes d’oxydo-réduction ; 3 = molécules du métabolisme intermédiaire (pyruvate, malate, acétylCoA, etc.).
Toutefois, le fait qu’un organisme est autotrophe n’implique pas que toutes ses cellules soient autotrophes. Ainsi, si l’on prend l’exemple des trachéophytes (plantes vascularisées, ce qui inclus les plantes à fleurs), on peut noter que dans leur cas l’appareil aérien est autotrophe, mais que l’appareil racinaire est lui hétérotrophe (de même que l’embryon et la plantule).
Voir sur le site BMédia : Exemples d’organismes autotrophes / phototrophes et classification sommaire
Cycles de l’oxygène et du carbone
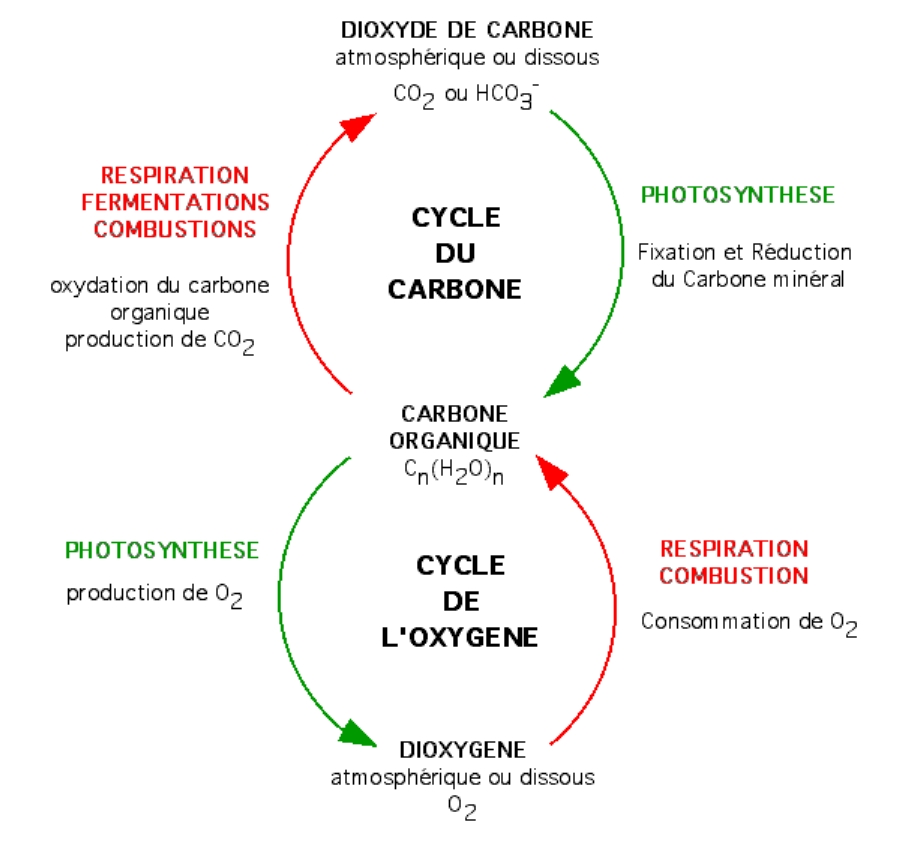
La photosynthèse des végétaux chlorophylliens est responsable de la fixation et de la réduction de CO2, ainsi que de la libération d’O2.
À l’inverse, la fonction respiratoire des organes et organismes non chlorophylliens est responsable de l’oxydation des composés organiques (consommation d’O2, libération de CO2).
Il en résulte un cycle pour le carbone et un cycle pour l’oxygène qui sont antiparallèles.
Voir sur le site BMédia : Le fonctionnement de ces cycles est lié à des flux d’énergie entre les organismes
Localisation de la photosynthèse
Chez les plantes terrestres (Embryophytes, anciennement appelées cormophytes), la photosynthèse se réalise dans les chloroplastes des parenchymes chlorophylliens des organes chlorophylliens. Ces organes sont les feuilles, plus rarement les tiges. Chez les algues, les cellules chlorophylliennes sont localisées dans l’ensemble du thalle.
Nous nous limitons ici à l’exemple des Angiospermes. Une étude expérimentale (par exemple basée sur la présence d’amidon, stocké temporairement lors de la photosynthèse) permet de mettre en évidence la localisation de la photosynthèse, aussi bien au niveau de l’organisme dans son entier qu’au sein de la cellule elle-même (voir à ce sujet le document sur cette mise en évidence expérimentale)
Localisation au sein des feuilles
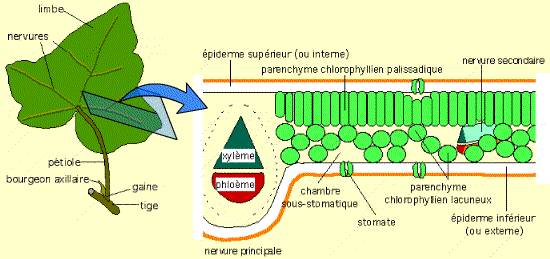
Chez les Angiospermes, la photosynthèse est essentiellement localisée au niveau de la feuille. Cet organe aplati, en relation étroite avec la tige, possède une morphologie lui permettant de présenter une grande surface vis-à-vis de l’environnement.
Voir sur le site BMédia : Exemple d’une feuille : le lierre
La nervure médiane, très en relief comme chez beaucoup de dicotylédones, contient principalement des tissus conducteurs de la sève brute (xylème) et de la sève élaborée (phloème). Ces tissus sont protégés par des tissus de soutien.
De part et d’autre de cette nervure, le limbe est formé par du parenchyme palissadique (face supérieure) et du parenchyme lacuneux (face inférieure).
La feuille est protégée des pertes d’eau par deux épidermes, recouverts d’une cuticule imperméable.
Les échanges de gaz sont assurés par les stomates.
La plupart des feuilles d’Angiospermes dicotylédones présente un parenchyme chlorophyllien palissadique à la face supérieure : c’est à son niveau que se déroule la photosynthèse. Ce tissu est en relation aussi bien avec l’extérieur (par les stomates) qu’avec l’intérieur de la plante (par les tissus conducteurs des nervures).
Voir sur le site BMédia : La feuille des Angiospermes Monocotylédone ne présente souvent qu’un seul type de parenchyme et Présentation plus complète de la structure de la feuille.
Localisation au sein des cellules
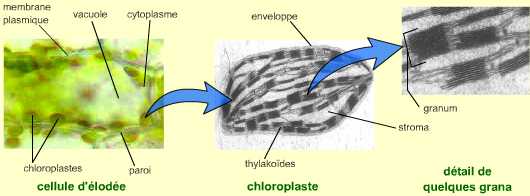
Au sein des cellules chlorophylliennes, la photosynthèse se déroule dans les chloroplastes. Ces organites de grande taille (environ 10 micromètres de long) possèdent une enveloppe composée d’une double membrane, et un système endomembranaire formant des saccules : les thylakoïdes. La conversion de l’énergie lumineuse en énergie de liaison chimique et en pouvoir réducteur se réalise au niveau des membranes des thylakoïdes. La réduction du carbone inorganique (CO2) en carbone organique a lieu dans le stroma du chloroplaste. Cette matière organique synthétisée peut être stockée temporairement sous la forme de grains d’amidon.
Dans la cellule végétale, les chloroplastes sont disposés dans le cytoplasme périphérique de la vacuole. Voir le document complet pour un schéma explicatif.
Le chloroplaste est observé au microscope électronique à transmission. On note deux types de thylakoïdes : les thylakoïdes granaires qui s’assemblent en « piles » de saccules (les grana), et les thylakoïdes intergranaires.
Voir sur le site BMédia : Schéma du chloroplaste, et voir aussi le document sur le chloroplaste
Isolement de chloroplastes
Les chloroplastes peuvent être observés dans les conditions naturelles (« in situ »). Mais il est parfois nécessaire de les isoler, afin de réaliser une étude plus précise de leur nature et de leur fonctionnement. Pour cela, on procède à l’éclatement des cellules végétales, puis à l’isolement et à la purification des chloroplastes intacts par plusieurs centrifugations successives.
Voir sur le site BMédia : Isolement des chloroplastes : protocoles de laboratoire et photographies
Équation globale de la photosynthèse
Diverses expériences permettent d’aboutir à une équation globale, résumant les mécanismes de la photosynthèse. Nous revenons ici sur quelques expériences permettant d’en démontrer les différents éléments, et donc de construire progressivement cette équation.
Plus de propositions d’expériences sont disponibles dans le dossier Expériences sur la photosynthèse.
Production de dioxygène, utilisation de dioxyde de carbone
On peut tout d’abord chercher si certains échanges gazeux se réalisent chez les plantes chlorophylliennes, en présence de lumière. On utilisera pour cela une plante aquatique, l’élodée du Canada, et comme source de CO2, de l’hydrogénocarbonate de sodium. Celui-ci, soluble dans l’eau est absorbé par la plante et converti en CO2 grâce à une anhydrase carbonique selon la réaction :
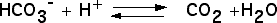 |
Les trois expériences sont réalisées dans : (a) de l’eau distillée ; (b) de l’eau du robinet ; (c) de l’eau additionnée d’hydrogénocarbonate à 1 %.
C’est en (c) que la production d’oxygène est la plus importante.
L'expérience précédente montre qu’à la lumière, une plante verte produit de l’O2 si du CO2 lui est fourni.
Cette constatation n’implique aucune relation chimique entre le CO2 et l’O2.
Voir sur le site BMédia : On peut obtenir des conclusions plus quantitatives en utilisant une électrode à oxygène (ExAO)
Ces expériences permettent donc de démontrer qu’en présence de lumière, les végétaux chlorophylliens consomment du CO2 et libèrent du O2. Toutefois, ces expériences seules ne nous permettent pas d’expliquer ce que permettent ces échanges gazeux pour la plante.
Production de glucides
Dans un deuxième temps, on recherche si l’exposition à la lumière a des conséquences sur la matière organique (et plus particulièrement glucidique) présente au sein du végétal. Des expériences utilisant des isotopes radioactifs démontrent ainsi que l’énergie lumineuse permet, indirectement, la synthèse de glucides simples.
Toutefois, il est difficile de caractériser ces glucides simples produits par la photosynthèse dans des expériences utilisant du matériel simple. Il est possible par contre de caractériser l’amidon (un polymère de glucose mis en réserve lorsque la photosynthèse est très active). Cette caractérisation se réalise avec le lugol, un réactif spécifique de l’amidon.
On peut ainsi observer la présence d’amidon au sein des chloroplastes de cellules de feuille d’élodée mises à la lumière.
Une feuille d’élodée est placée dans une eau enrichie en hydrogénocarbonate et éclairée plusieurs heures.
A gauche : cellules observées sans coloration, chloroplastes naturellement verts.
A droite : après traitement par le lugol, des grains d’amidon de couleur sombre sont visibles dans les chloroplastes.
Voir sur le site BMédia : On peut réaliser une expérience similaire à l’échelle de la feuille du pélargonium
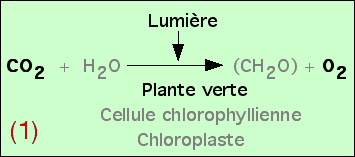
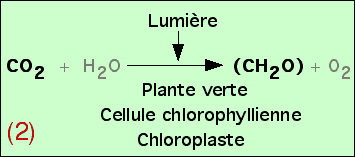
On peut donc déduire de ces expériences qu’une plante éclairée fabrique des glucides (CH2O)n dans ses chloroplastes à partir du CO2 du milieu.
On obtient ainsi l’équation bilan de la photosynthèse. Afin d’obtenir un équilibre chimique de cette réaction, on rajoute H2O, mais sans que les expériences présentées ici aient permis de démontrer son utilisation réelle.
Remarque : origine de l’O2
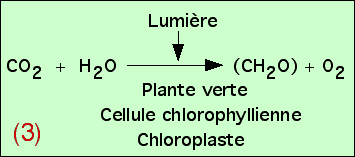
Des études plus précises peuvent être réalisées, afin de mieux comprendre les relations entre les atomes des molécules figurées dans cette équation bilan. Si le devenir du carbone du CO2 ne pose pas de problème (il est incorporé dans les glucides synthétisés), l’origine de l’oxygène de l’O2 pourrait se trouver soit au niveau du CO2, soit au niveau de l’eau H2O. En réalité, il apparaît que c’est l’oxygène de l’eau qui est libéré, au cours d’une réaction d’oxydo-réduction. Ceci permet de préciser alors l’équation bilan de la photosynthèse.
Voir sur le site BMédia : Origine de l’O2 et implications pour l’équation bilan de la photosynthèse
Les pigments photosynthétiques
La réalisation de la photosynthèse par les chloroplastes des végétaux met en jeu un ensemble de molécules particulières, nommées pigments photosynthétiques. Le terme de « pigment » correspond au fait que ces molécules sont colorées, de part leur capacité à capter certaines radiations lumineuses. Ces pigments sont de trois types :
- les chlorophylles, présentes chez tous les végétaux autotrophes au carbone ;
- les caroténoïdes, présents chez tous les végétaux autotrophes au carbone ;
- les phycobilines, présentes exclusivement chez les algues et les cyanobactéries.
On peut assez facilement extraire et séparer ces différents pigments.
Voir sur le site BMédia : Extraction et séparation des pigments photosynthétiques
Structure des pigments
Les chlorophylles sont constituées d’un noyau tétrapyrrolique avec un magnésium en son centre, et estérifié avec un alcool à très longue chaîne en C20 (le phytol). Dans la membrane des thylakoïdes, les chlorophylles sont associées à des protéines et forment des complexes protéines – pigments.
Les chlorophylles diffèrent par les substituants des groupements pyrroles. Le phytol n’est pas détaillé ici.
Légende : I, II, III, IV = groupements pyrroles et V = cycle supplémentaire.
Télécharger le fichier PDB de la chlorophylle a pour une visualisation avec rasmol / rastop : chloa.pdb
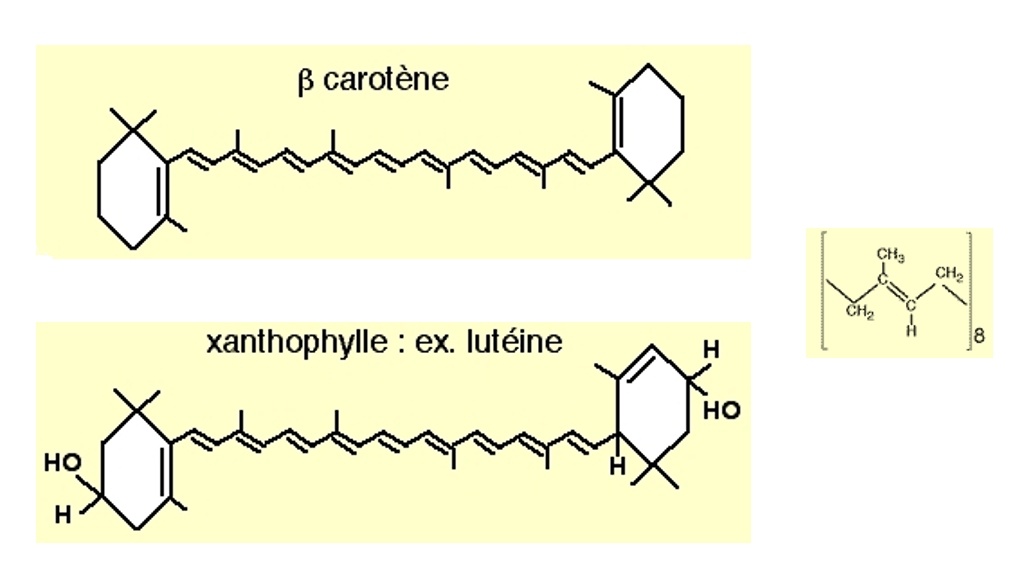
Les caroténoïdes sont des molécules constituées de 40 carbones, avec deux extrémités cyclisées reliées par une longue chaîne de 8 unités isoprènes.
Le β-carotène est un exemple de carotène, et la lutéine un exemple de xanthophylle. À droite est représentée une unité isoprène.
Télécharger le fichier PDB du βcarotène pour une visualisation avec rasmol / rastop : bcarotene.pdb
Les phycobilines sont composées d’un noyau tétrapyrrolique ouvert, associé à une protéine. On les trouve au sein des photosystèmes de certaines algues, et de bactéries photosynthétiques telles que les cyanobactéries.
L’exemple présenté ici est la phycocyanobiline, représentée sans la protéine qui l’accompagne normalement.
Télécharger le fichier PDB de la phycocyanobiline pour une visualisation avec rasmol / rastop : phycocyanobiline.pdb
Spectres d’absorption
Les chlorophylles et les caroténoïdes absorbent certaines radiations dites actives pour la photosynthèse, dans la gamme de longueurs d’onde visibles comprises entre 500 et 700 nm.
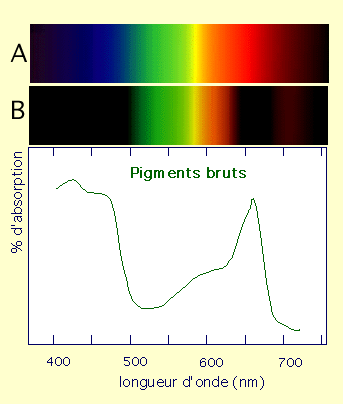
À partir d’une solution de pigments, on peut donc mesurer les caractéristiques d’absorption de la lumière en réalisant un spectre d’absorption à l’aide d’un spectrophotomètre UV-visible classique, qui permet de mesurer l’absorption (A) en fonction de la longueur d’onde (l).
A : spectre lumineux en absence de pigments.
B : spectre lumineux en présence de pigments.
On note que l’absorption maximale se réalise dans le bleu et dans le rouge.
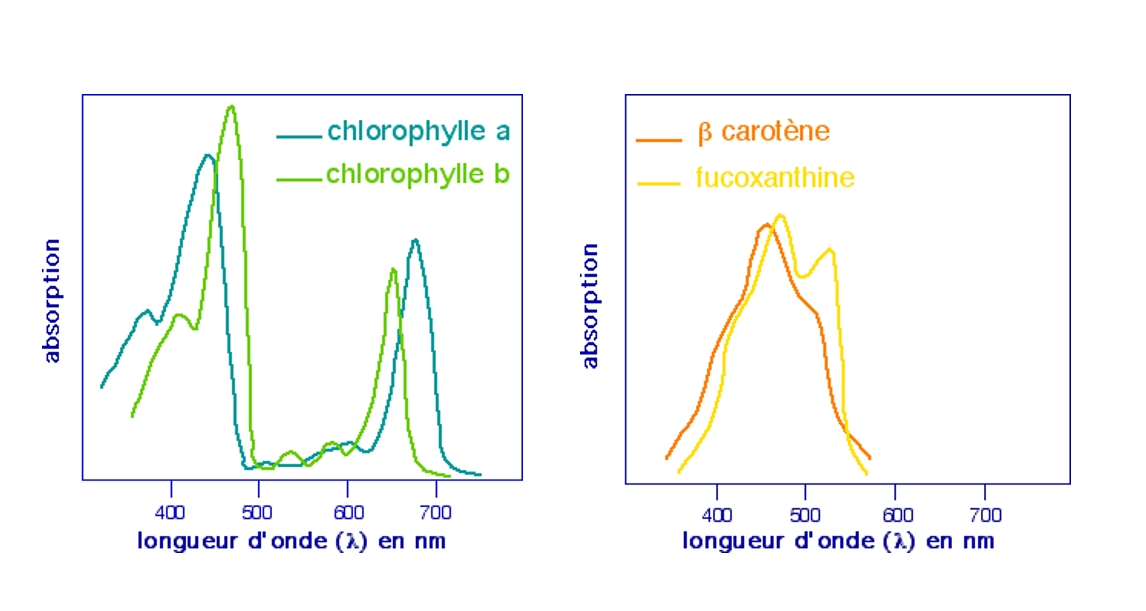
Un tel spectre global ne permet pas de reconnaître la part qui revient à chaque pigment. Pour cela, il faut travailler sur des solutions de pigments séparés et purifiés.
A gauche : spectres d'absorption des chlorophylles a et b.
A droite : spectres d'absorption du bêta-carotène et de la fucoxanthine
Voir sur le site BMédia : distribution spectrale de l’énergie lumineuse
Comportement des chlorophylles à la lumière
Les chlorophylles sont des pigments. De ce fait, ces molécules (comme les autres pigments photosynthétiques) peuvent être excitées par les radiations lumineuses. Cette excitation est due à la présence de liaisons conjuguées (et donc d’électrons délocalisés) : l’arrivée d’un photon fait passer un électron délocalisé d’un état fondamental (non excité) à un état excité. Chez la chlorophylle, il existe deux états excités : un état supérieur (Sa) et un état inférieur (Sb), selon l’énergie du photon excitateur.
La chlorophylle, une fois excitée, retourne à son état fondamental, plus stable thermodynamiquement. Ceci peut se faire de plusieurs manières, et en particulier en :
- émettant de la lumière (c’est la fluorescence constatée dans une solution de chlorophylle) ;
- transférant son énergie à une molécule très proche (c’est la résonance, qui permet aux pigments de l’antenne collectrice des photosystèmes de transférer l’énergie lumineuse de molécule en molécule jusqu’à une chlorophylle piège) ;
- perdant un électron (c’est la photochimie, qui permet à la molécule de chlorophylle piège du photosystème de réduire un accepteur d’électron, et ainsi de permettre la réalisation de la chaîne photosynthétique).
Voir sur le site BMédia : Précisions et importance des deux états d’excitation
Spectre d’action – expérience d’Engelman
Les spectres d’absorption des pigments sont uniquement liés à leur capacité à capter des photons de certaines longueurs d’onde. Le spectre d’action consiste à quantifier l’activité que l’on cherche à corréler à ces pigments (ici l’activité photosynthétique), en fonction des longueurs d’onde incidentes. Les spectres d’action ainsi réalisés suivent globalement les spectres d’absorption des végétaux chlorophylliens, ce qui confirme que c’est bien cette capacité à capter les photons qui permet la réalisation de la photosynthèse.
Voir sur le site BMédia : Spectres d’action et d’absoprtion, rendement quantique
Plusieurs approches expérimentales permettent de déterminer ce spectre d’action. Une expérience simple et bien connue est celle réalisée par Engelman.
Influence des conditions du milieu
La photosynthèse est influencée par les facteurs de l’environnement : la lumière (source d’énergie), le CO2 (source de carbone) et la température (qui affecte l’ensemble des réactions biochimiques).
La photosynthèse est un processus complexe qui fait intervenir de nombreuses étapes qui sont affectées de manière différente par les facteurs de l’environnement. De ce fait, les facteurs externes agissent indépendamment les uns des autres et le phénomène global obéit à la loi dite des « facteurs limitants » que l’on peut énoncer de la façon suivante : lorsqu’un processus est contrôlé par plusieurs facteurs agissant indépendamment, son intensité est limitée par le facteur qui présente la valeur minimum. Le facteur est alors limitant et la vitesse du processus est proportionnelle à la valeur de ce facteur.
Mesure de la photosynthèse
Pour pouvoir étudier les facteurs externes influant sur la photosynthèse, encore faut-il être capable de mesurer celle-ci. Dans cette optique, un certain nombre de paramètres peuvent être pris en compte, et en particulier l’incorporation du carbone dans les molécules organiques, l’évolution de la concentration en CO2, ou encore l’évolution de la concentration en oxygène.
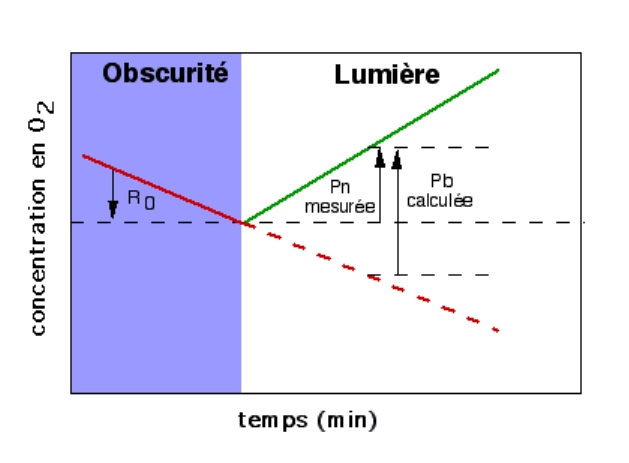
Une solution simple et quantitative est l’utilisation d’une électrode à oxygène pour mesurer l’évolution de la concentration en oxygène. Ainsi, on observe à la lumière un dégagement d’oxygène. La mesure de ce dégagement correspond à la photosynthèse nette (Pn). En effet, la plante, dans le même temps, réalise la respiration cellulaire, et consomme ainsi de l’oxygène, ce qui fausse cette mesure… La solution est alors de mesurer la consommation d’oxygène à l’obscurité, qui correspond à la respiration (Ro). On obtient alors la valeur de la photosynthèse brute (Pb) par la formule suivante : Pb = Pn - Ro
Pb = Pn - Ro
Pb = photosynthèse brute ; Pn = photosynthèse nette ; Ro = respiration
Voir sur le site BMédia : explication des paramètres de mesure ; les différentes techniques de mesure ; détails sur l’électrode à oxygène…
Influence de la lumière
La photosynthèse se réalise en présence de lumière. Il est possible de quantifier ce phénomène, en éclairant des plantes avec une source lumineuse permettant de réaliser une gamme d’intensités (flux de photons) déterminées.
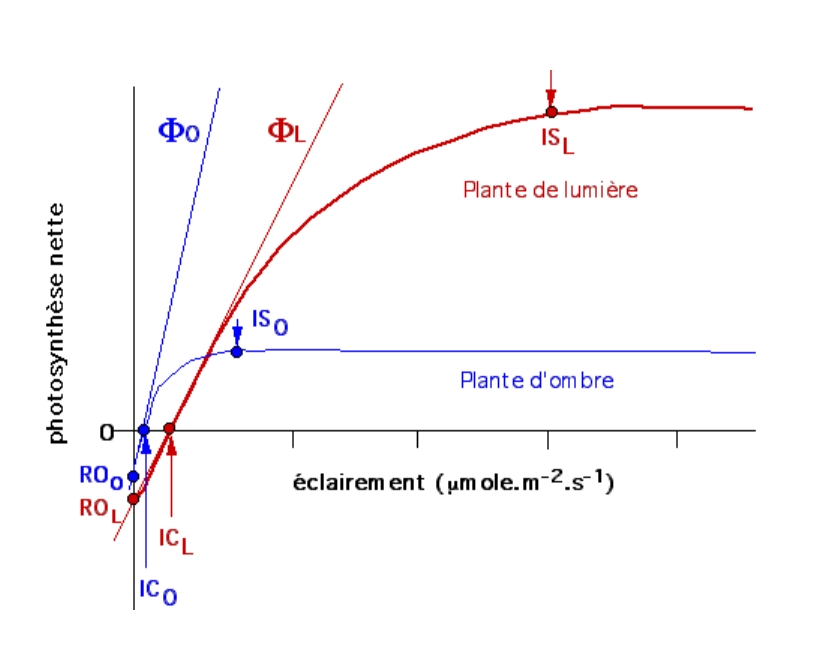
On obtient ainsi des courbes biphasiques, permettant de déterminer plusieurs paramètres :
- L’éclairement saturant ou optimal (IS) : c’est l’éclairement pour lequel la courbe atteint un plateau. Au-delà, la capacité d’absorption des photons dépasse la capacité de leur utilisation. Les réactions d’assimilation du CO2 deviennent limitantes et la photosynthèse présente une intensité maximale.
- Le point de compensation pour la lumière (IC) : c’est la valeur de l’éclairement pour laquelle la photosynthèse nette est nulle ; la photosynthèse compense juste la respiration.
- Le rendement de l’absorption des photons (ou rendement quantique foliaire Phi Ф) c’est la pente (coefficient directeur) de la partie linéaire initiale de la courbe. Dans cette gamme d’éclairement, la lumière est limitante.
Il est aussi possible d’étudier l’influence qualitative de la lumière, en réalisant le spectre d’action de la lumière sur le végétal étudié. On peut ainsi s’apercevoir que toutes les radiations lumineuses ne sont pas aussi efficaces pour la photosynthèse.
Voir sur le site BMédia : Étude du spectre d’action, détermination du rendement quantique en fonction de la longueur d’onde
Comparaison de la photosynthèse de plantes de lumière et de plantes d’ombre
Les autres facteurs (concentration en CO2 atmosphérique, température 25 °C) sont maintenus constants.
IC : intensité de compensation ; IS : intensité saturante ; Ф : rendement quantique foliaire.
En bleu : plantes d’ombre ; en rouge : plantes de lumière.
Quand on compare le comportement de ces deux types de plantes on constate que :
- ICO (ombre) est inférieure à ICL (lumière) ;
- ФO (ombre) est supérieur à ФL (lumière) ;
- ISO (ombre) est inférieure à ISL (lumière).
En d’autres termes, les plantes d’ombre présentent une intensité photosynthétique optimale et une intensité de compensation plus faible, mais une efficacité dans l’absorption des photons plus élevée (plantes des sous-bois). Inversement, les plantes de lumière sont moins efficaces dans la capture des photons, mais elles fixent davantage de CO2 (ex : plantes cultivées).
Influence de la concentration en CO2
Les plantes aériennes assimilent le CO2 atmosphérique (0,035 % de CO2) tandis que les plantes aquatiques absorbent soit le CO2 dissous (concentration faible : environ 10 µM à pH 7), soit les ions bicarbonate HCO3- (concentrations élevées : de l’ordre du mM, mais variable en fonction du pH), qui sont ensuite convertis en CO2 grâce à la réaction catalysée par l’anhydrase carbonique.
La quantité de CO2 disponible est limitante dans des conditions d’éclairement moyen. Par conséquent, une augmentation de la photosynthèse est observée lorsqu’on augmente la concentration de CO2.
La courbe présente une première partie pseudo-linéaire pour laquelle le CO2 est limitant, et une seconde partie qui correspond à un plateau pour lequel l’éclairement est devenu limitant et la photosynthèse maximale, dans ces conditions.
Voir sur le site BMédia : Effets conjugués de la teneur en CO2 et de l’éclairement
Influence de la température
L’optimum de température des plantes varie en fonction de leur origine. Ainsi, les plantes des régions tempérées ont un maximum qui se situe entre 15 °C et 25 °C, avec une limite de tolérance au froid vers – 2 °C à 0 °C et de tolérance au chaud vers 40 °C à 50 °C.
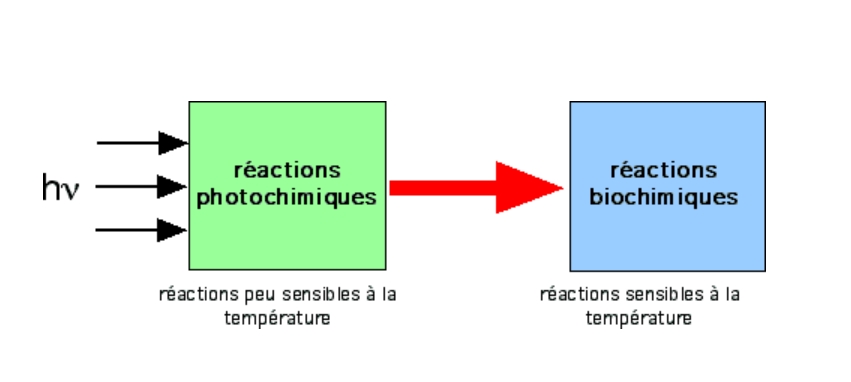
Pour une plante donnée, on observe des modifications du point de compensation (IC) et du point de début de saturation (IS), mais sans modification du rendement Ф. Ceci montre que les réactions photochimiques sont peu ou pas sensibles à la température, au contraire des réactions biochimiques.
Voir sur le site BMédia : L’influence de la température. Courbes de photosynthèse nette d’une plante à 15 °C et à 25 °C
Deux groupes de réactions
Plusieurs types d’expériences ont montré que la photosynthèse pouvait être découpée en deux groupes de réactions de significations différentes, mais couplées entre elles et nécessitant des intermédiaires.
Origine de l’oxygène (Ruben et Kamen, 1938)
L’équation bilan de la photosynthèse montre un dégagement de dioxygène.
La question se pose de savoir d’où provient ce dioxygène. On peut en effet émettre deux hypothèses : soit cet oxygène provient du CO2, soit il provient de l’eau H2O. Afin de trancher entre ces deux possibilités, Ruben et Kamen ont utilisé un isotope lourd de l’oxygène (18O) à la place de l’oxygène habituel (16O) et ils ont marqué ainsi diverses molécules (H2O, CO2). Lorsque de l’eau est marquée par le 18O (H218O), le dioxygène produit par la photosynthèse devient marqué ; ce n’est pas le cas lorsque le CO2 est marqué par le 18O. Ils en déduisent que c’est l’eau (H2O) qui est à l’origine du dioxygène produit. Pour former une molécule de dioxygène, il faut donc 2 molécules d’eau.
Ces résultats montrent que l’on peut décomposer la réaction photosynthétique en deux groupes de réactions :
Ces deux réactions (oxydation de l’eau et réduction du dioxyde de carbone) sont couplées dans un ensemble complexe de réactions d’oxydoréduction faisant intervenir des transporteurs de protons (H+) et d’électrons (e-).
Voir sur le site BMédia : Réactions d’oxydoréductions entre les couples H2O/O2 et CO2/(CH2O)
Existence de deux types de réactions (Emerson et Arnold, 1932)
Diverses expériences d’incorporation de CO2 par des chlorelles (algues unicellulaires) ont permis de mettre en évidence que l’ensemble des réactions composant la photosynthèse peut être décomposé en deux groupes :
- des réactions mettant directement en jeu la lumière – on parle de phase photochimique de la photosynthèse ;
- des réactions plus lentes, sans utilisation directe de la lumière – on parle de phase biochimique de la photosynthèse.
Voir sur le site BMédia : Démonstration de l’existence de deux types de réactions
La libération d’O2 nécessite un accepteur d’électron (Hill, 1937)
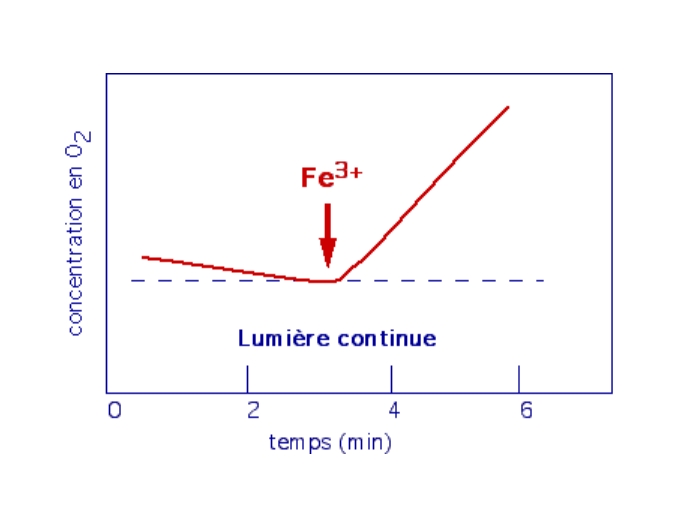
Hill utilise une suspension de chloroplastes isolés dans un tampon sans CO2. Il mesure les variations de dioxygène à l’aide d’une électrode à oxygène. Il ajoute à la préparation un accepteur artificiel d’électrons, le ferricyanure de potassium, Fe3+(CN–)6K3 (réactif de Hill) et travaille en lumière continue.
En absence de CO2, les chloroplastes sont capables de libérer du dioxygène, à condition qu’un accepteur d’électron (Fe3+) soit présent dans le milieu.
Le réactif de Hill se comporte comme un accepteur d’électron :
Fe3+ + e – → Fe2+
Dans les conditions naturelles de la photosynthèse, ce rôle d’accepteur d’électron est rempli par le couple NADP+/NADPH :
NADP+ + 2e – + 2H+ → NADPH + H+
Le couple NADP+/NADPH joue ainsi le rôle d’intermédiaire entre l’oxydation de l’eau et la réduction du CO2.
De plus, l’ATP sert aussi d’intermédiaire énergétique : de l’ATP est formé en conséquence du fonctionnement de la chaîne photosynthétique, et est ensuite utilisé lors de la formation des composés carbonés.