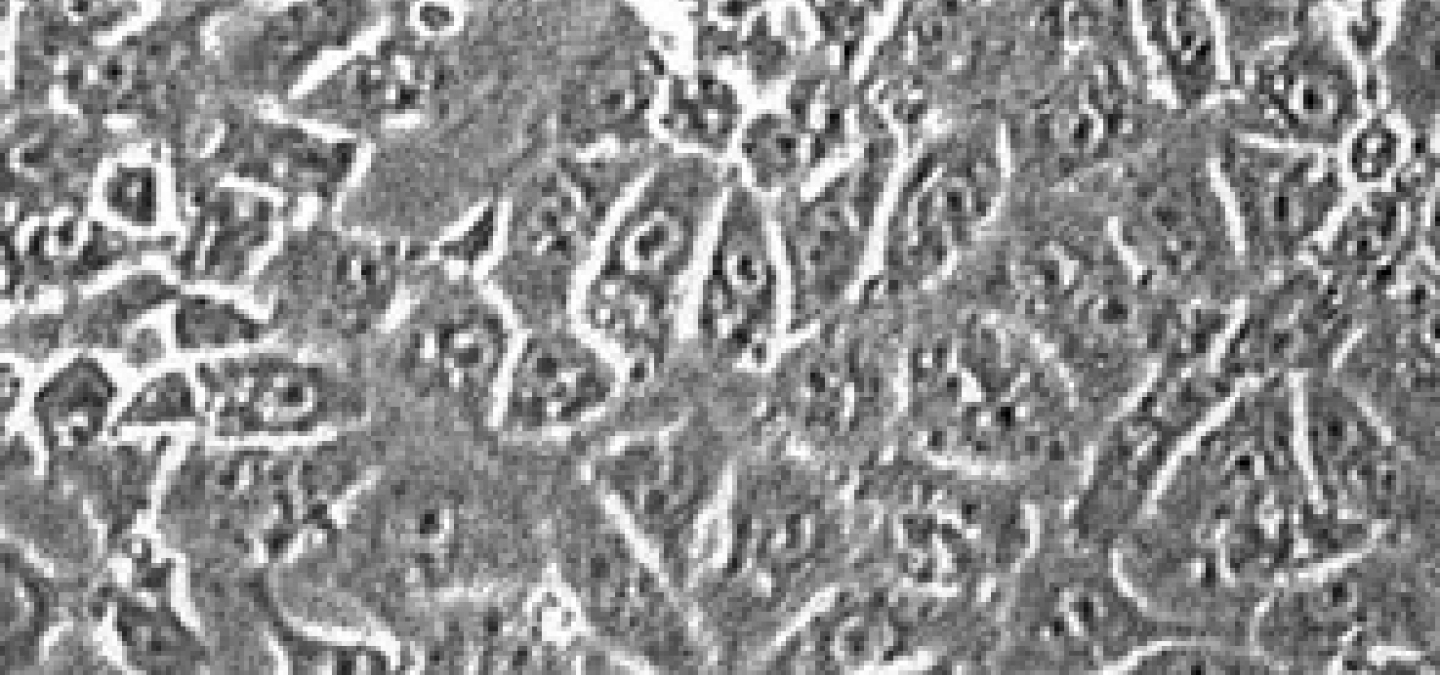
Le protocole présenté ici explique comment mettre en place une culture de cellules d’embryons de caille, à partir d’œufs.
Introduction
Le protocole présenté ici explique comment mettre en place une culture de cellules d’embryons de caille, à partir d’œufs.
But méthodologique
Travailler dans des conditions strictes d’asepsie.
Résultats attendus
- Pas de contamination.
- Multiplication des cellules de l’explant.
- Migration de cellules.
- Différenciation de cellules.
Matériel
Par groupe de 4 élèves :
- œufs de caille (commande à : Société « La caille de Chanteloup », Le Petit Vélobert, 35180 Corps-Nuds).
- 1 loupe binoculaire (nettoyée à l’alcool)
- 2 champs stériles
- 2 paires de petits ciseaux stériles
- 2 petits récipients stériles (pour recevoir l’œuf)
- 1 petite cuillère stérile (cuillère à moka)
- 1 pince stérile
- 1 boîte de Pétri paraffinée, à fond noir stérile
- 6 épingles entomologiques stériles
- 2 microscalpels stériles
- 2 pipettes Pasteur
- 1 tube à centrifuger
- 4 pipettes de 1 mL stériles
- 1 pipette de 2 mL stérile
- 1 flacon de culture contenant quelques mL de Tyrode (milieu physiologique, sels inorganiques et D-glucose) stérile
- 1 tube à centrifuger contenant 1 mL de trypsine EDTA
- 1 tube de 10 mL de milieu de culture (milieu de Leibovitz avec sérum à 10 %). Milieu de Leibovitz = milieu de culture constitué de sels inorganiques, galactose, 18 acides aminés, 8 vitamines : ce milieu s’utilise additionné juste avant emploi de sérum de veau et d’antibiotiques.
- une centrifugeuse
- 2 petits incubateurs Jeulin à 37 °C
Protocole expérimental
1re semaine : présentation du protocole et du matériel
Explications (environ 45 min). Présentation et explications terminées, les élèves se partagent la réalisation du protocole. Un des 4 élèves veillera à sa bonne exécution. Il serait impossible de donner en une seule séance de TP toutes les explications et de réaliser le protocole, d’autant qu’il n’est pas certain que le premier œuf ouvert soit embryonné.
2e semaine : réalisation du protocole
Œufs à l’étuve à 37 °C depuis 4 jours, coupelle d’eau dans l’étuve.
- Les élèves déposent leurs vêtements au fond de la salle, se lavent les mains au savon puis à l’alcool, se placent devant les paillasses qui ont été javellisées et à côté des becs Bunsen éclairés depuis 40 minutes. Aucun courant d’air, fenêtres fermées.
- Passer l’œuf à l’alcool à l’aide d’un coton.
- Découper une fenêtre au sommet de la coquille à l’aide des ciseaux.
- Verser le contenu de l’œuf dans un récipient stérile contenant du Tyrode stérile.
- Repérer l’embryon et découper l’aire extra-embryonnaire à l’aide de ciseaux.
- Transférer l’embryon dans un petit récipient stérile rempli de Tyrode à l’aide de la petite cuillère, éliminer le jaune résiduel en agitant.
- Transférer l’embryon dans la boîte de Pétri paraffinée à fond noir, remplie de milieu de Tyrode.
- Épingler l’aire extra-embryonnaire en inclinant les épingles.
- Observer l’embryon à la loupe binoculaire.
- Dégager l’embryon de ses enveloppes à l’aide des microscalpels.
- Prélever très doucement l’embryon à l’aide d’une pipette Pasteur et l’installer dans un tube à centrifuger contenant 1 mL de trypsine EDTA additionnée de 1 % d’antibiotiques.
- Placer le tube contenant l’embryon à l’étuve à 37 °C, de 10 à 15 minutes selon la taille de l’embryon.
- À l’aide d’une pipette Pasteur, aspirer et rejeter plusieurs fois l’embryon qui se désagrège alors ; bien mélanger.
- Centrifuger le tube 10 secondes à 1200 tours/minute.
- Jeter le surnageant.
- Ajouter 1 mL de milieu de culture pour faire une suspension cellulaire.
- Introduire stérilement dans le flacon de culture cellulaire 1 mL ou un peu plus de suspension cellulaire.
- Placer le flacon bien horizontalement dans l’étuve à 37 °C.
- Dans le fond de l’étuve sont placées 1 coupelle d’eau et 2 petites bougies précédemment allumées. On admet que lorsqu’elles s’éteignent, l’étuve contient suffisamment de CO2 pour la culture cellulaire (conseil donné par un laboratoire de recherches).
- Tous les 2 jours le professeur rajoute de l’eau dans la coupelle, rallume les 2 bougies (placer pendant la combustion les flacons dans une autre étuve), élimine une partie du milieu de culture et le remplace par du milieu neuf à 37 °C.
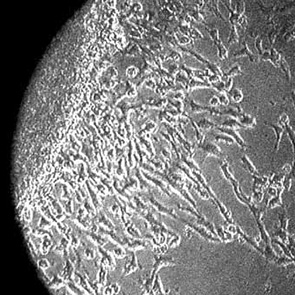
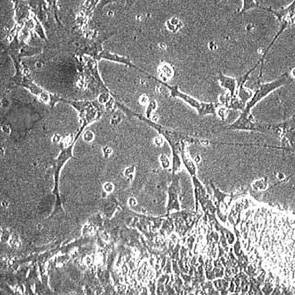
Résultats au bout de 7 jours
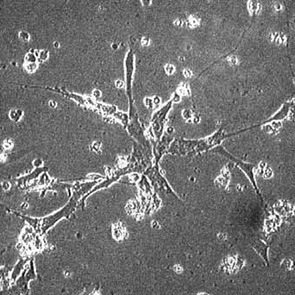
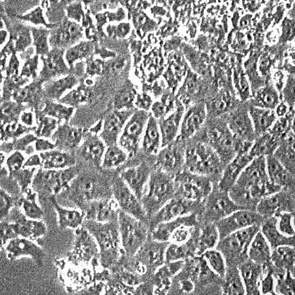
Au-delà les cultures s’abîment. Aucune pollution, dans aucun flacon. Présence dans les flacons de :
- cellules sphériques ;
- cellules allongées (forme de navette) ;
- très beaux fibroblastes ;
- superbes neurones.
Remarques
- Aucune réticence de la part des élèves.
- Séances qui ne sont pas de tout repos pour le professeur !
- Très grande satisfaction au vu des résultats.
- Résultats assurés si l’on suit toutes les rubriques et tous les conseils.
- Élément variable constaté : durée de l’incubation nécessaire à l’étuve, de 3 à 5 jours.
Illustrations
 |
 |
 |
 |
Référence
Marie-Jeanne Pellerin « Fenêtre sur… les cultures cellulaires animales ». CRDP Île-de-France.