L’Hermelle est un annélide, marin, polychète, sédentaire et tubicole, c’est-à-dire un ver formé d’une succession d’anneaux portant de nombreuses soies et qui vit dans un tube de sédiment sableux aggloméré par ses propres sécrétions. Les tubes de sable sont droits, accolés les uns aux autres, ressemblant à des gâteaux d’abeille et formant des pseudorécifs de masse souvent considérable.
Images : service de biologie du développement de l’Université Pierre et Marie Curie.
Généralités
L’Hermelle est un annélide, marin, polychète, sédentaire et tubicole, c’est-à-dire un ver formé d’une succession d’anneaux portant de nombreuses soies et qui vit dans un tube de sédiment sableux aggloméré par ses propres sécrétions. Les tubes de sable sont droits, accolés les uns aux autres, ressemblant à des gâteaux d’abeille et formant des pseudorécifs de masse souvent considérable.
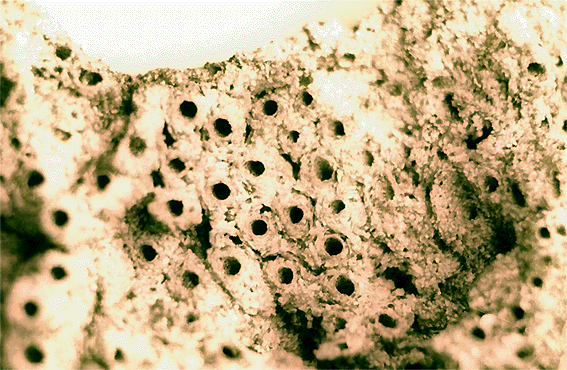 |
| Cliquez sur le photo pour obtenir une version légendée. |
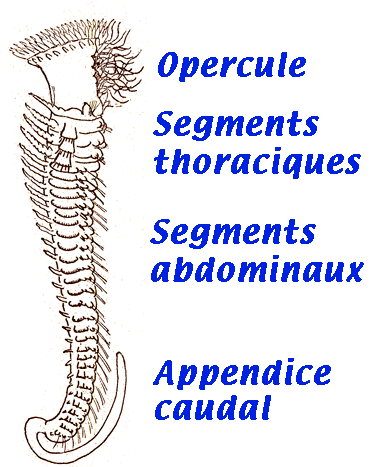
La sédentarité des polychètes va de pair avec une régionalisation accrue de leur anatomie. Ainsi l’hermelle présente des régions spécialisées très marquées. On distingue la région antérieure spécialisée en opercule destiné à fermer l’orifice du tube. Le reste du corps est divisé en régions parathoracique, abdominale et caudale.
 |
En laboratoire, les animaux peuvent être maintenus dans de l’eau de mer provenant de stations biologiques marines ou de l’eau de mer artificielle renouvelée, filtrée et aérée, en circuit fermé. Dans ces conditions, les hermelles restent matures pendant plusieurs jours, voire plusieurs semaines. La température optimale d’élevage est celle de l’eau de mer d’où elles proviennent. Cependant, pour maintenir les animaux en état de reproduction, il est préférable de les élever à une température comprise entre 5 et 10 °C.
Protocole expérimental
Pour réaliser la fécondation artificielle, le protocole est le suivant.
L’extraction des animaux de leur tube de sable s’effectue en émiettant les blocs de sable aggloméré en pleine eau. Les hermelles libérées sont récoltées et placées séparément dans des boîtes de Pétri remplies d’eau de mer.
L’observation est facilitée en plaçant les coupelles sur un fond noir ou de couleur foncée. De cette façon, on peut distinguer les mâles blanchâtres des femelles rouge-violacé. La ponte et l’émission des spermatozoïdes sont généralement provoquées par le stress de l’extraction, aussi, les animaux une fois placés dans les boîtes de Pétri émettent-ils spontanément leurs produits génitaux que l’on distingue nettement sur fond noir.
La mobilité des spermatozoïdes peut être vérifiée entre lame et lamelle au microscope à un fort grossissement au contraste de phase. Éventuellement, l’activation des spermatozoïdes peut être facilitée dans de l’eau de mer supplémentée en EDTA (Ethylène Diamine Tétra Acétate) à raison de 0,001 molaire, pH 8,2 (ajusté avec KOH mol.L-1).
Il ne reste plus qu’à prélever, avec une pipette Pasteur, les ovocytes et les spermatozoïdes émis sur le fond d’une coupelle contenant respectivement une femelle et un mâle.
Il est recommandé de diluer le prélèvement spermatique de telle manière qu’une goutte de prélèvement soit répartie dans un volume de 30 à 50 mL d’eau de mer. Cette précaution permet d’éviter une éventuelle polyspermie.
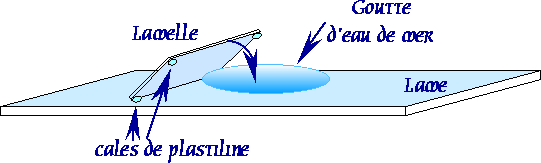
Les gamètes sont réunis dans une goutte d’eau de mer sur une lame histologique.
Une lamelle histologique est appliquée sur la goutte d’eau de mer après avoir pris la précaution de garnir chaque angle de la lamelle avec une cale de plastiline. Par son épaisseur et sa souplesse, la plastiline maintient un espace qui forme une chambre d’observation entre la lame et la lamelle. Cet espace évite l’aplatissement voire l’écrasement des ovocytes.
 |
On peut aussi utiliser des lames histologiques garnies d’une cupule creusée dans l’épaisseur du verre. Dans ce cas, les cales en plastiline de la lamelle ne sont pas nécessaires.
L’observation du développement s’effectue au microscope à lumière transmise sous un grossissement compris entre × 4 et × 16.
Stades de développement
Bien que les ovocytes puissent être fécondés à n’importe quel moment de la maturation, il est préférable d’attendre son achèvement car ainsi, les évènements de la fécondation peuvent être observés séparément. Dans ce cas, l’entrée du spermatozoïde s’effectue en une vingtaine de minutes.
La chronologie des événements qui suivent l’entrée du spermatozoïde dans l’ovocyte est alors la suivante :
- Émission du premier globule polaire.
- Émission du second globule polaire.
- Formation du premier lobe polaire.
- Apparition du premier plan de clivage et réintégration du premier lobe polaire (stade deux cellules).
- Formation du deuxième lobe polaire.
- Apparition du deuxième plan de clivage et réintégration du deuxième lobe polaire (stade quatre cellules).
- Poursuite du clivage (par ex : stade huit cellules).
- Stade gastrula.
- Larve trochophore.
- Une des particularités de certains développements embryonnaires des annélides et des mollusques consiste en la formation du lobe polaire. Il s’agit d’une protrusion cytoplasmique qui apparaît au pôle végétatif de l’œuf avant la formation du premier sillon de segmentation et qui est réintégrée dans l’un des blastomères (blastomère CD) au stade deux cellules. Ce phénomène se répète au stade suivant mais avec une moindre ampleur. Au stade 4 cellules, la réintégration du lobe polaire détermine le blastomère D impliqué dans la formation du mésoderme.
Il a été démontré chez d’autres espèces que Sabellaria, que le lobe polaire correspond à une région cytoplasmique liée au destin du blastomère D et qui contient des déterminants cytoplasmiques nécessaires au rythme du clivage, à la spécification de l’axe dorsoventral et à la différenciation du mésoderme. Ces déterminants seraient liés au cytosquelette cortical.
La succession des stades précoces du développement est résumée dans les spirales ci-dessous (la première donne accès aux images non-légendées, la seconde aux images légendées).
 |
| Pour voir les images non-légendées agrandies, cliquez sur les vignettes. |
 |
| Pour voir les images légendées agrandies, cliquez sur les vignettes. |