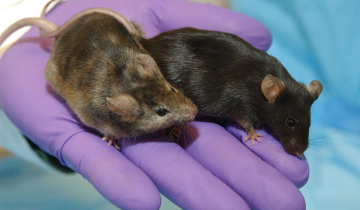
Trois études indépendantes publiées simultanément dans la revue Science du 31 décembre 2015 font état de la guérison de souris atteintes de myopathie par thérapie génique utilisant la technique CRISPR-Cas9.
Ces résultats, s'ils sont très loin d'être directement transposables à l'Homme, constituent un nouveau pas en avant important dans la recherche d'un moyen de guérir les malades atteints de myopathie.
Auteur, publication : Gilles Camus
Table des matières
- La myopathie de Duchène
- CRISPR-Cas9
- Guérison d'un modèle animal de myopathie par thérapie génique
- Perspectives
- Bibliographie
1. La myopathie de Duchène
La myopathie de Duchenne est une maladie génétique évolutive touchant les muscles. Elle est causée par l'absence (délétion) ou la mutation d'un gène, le gène DMD pour Duchenne Muscular Dystrophy, codant pour la protéine appelée dystrophine. Dans les deux cas l'erreur génétique entraîne une absence de dystrophine dans la cellule. Il existe également une forme moins grave de cette maladie, appelée myopathie de Becker, dans laquelle la nature de la mutation du gène DMD permet à la dystrophine d'être exprimée, même s'il s'agit d'une protéine tronquée. Cette protéine anormale conserve cependant en partie ses fonctionnalités ce qui limite l'étendue des désordres.
La dystrophine est une protéine présente à la face cytoplasmique de la membrane des cellules musculaires. C'est un élément du cytosquelette sous-membranaire et son absence désorganise ce cytosquelette, ce qui entraîne progressivement une dégénérescence des muscles. Si la prise en charge des effets de la maladie a progressé, il n'existe actuellement aucun traitement pour la soigner, et les malades ont une espérance de vie réduite (le décès intervient généralement avant l'âge de 30 ans en raisons de difficultés cardio-respiratoires).
La myopathie est l'une des maladies génétiques les plus fréquentes chez l'Homme (1 garçon sur 3 500 touchés à la naissance). Plusieurs raisons à cela. Tout d'abord le gène DMD est porté par le chromosome X. Comme pour toute maladie génétique liée à un gène porté par le chromosome X, les garçons sont beaucoup plus touchés que les filles. En effet la présence d'une anomalie portée par le gène DMD sur leur unique chromosome X ne peut pas être compensée puisqu'il n'y a pas de seconde copie. Par ailleurs la dystrophine est une protéine géante (427 kDa). Le gène DMD est donc également particulièrement grand (2,5 millions de pb) de sorte que la fréquence des erreurs de réplication de ce gène est importante.
Dans ce cadre, les résultats obtenus sont d'autant plus inattendus. En effet lorsque l'on parle d'une approche par thérapie génique, on pense généralement à l'apport d'une version saine d'un gène aux cellules qui en ont besoin. Mais dans le cas présent, outre la difficulté d'apporter un gène quel qu'il soit à des cellules qui ne sont pas isolées mais dans un organisme vivant complet, la grande taille du gène DMD constitue une difficulté supplémentaire.
2. CRISPR-Cas9
Les auteurs des trois études ont donc utilisé une technique différente. Plutôt que d'apporter une copie saine du gène DMD, ils ont réparé l'allèle défectueux présent dans les cellules en utilisant l'outil d'édition de génome CRISPR-Cas9. Cet outil a été mis au point très récemment par la française Emmanuelle Charpentier et l'américaine Jennifer Doudna (l'article qui décrit pour la première fois l'utilisation possible de la technique remonte à 2012, voir ref. 1). Pourtant, son utilisation se développe à toute vitesse dans les laboratoires. Il permet en effet de modifier précisément le patrimoine génétique des cellules avec une facilité, une rapidité et un coût sans commune mesure avec les techniques utilisées jusqu'à présent. Cet outil comporte deux choses :
- une endonucléase (Cas9). Cette enzyme bactérienne est capable de couper les deux brins d'une molécule d'ADN. Elle n'est pas apportée sous forme de protéine mais sous la forme de son gène qui doit alors être exprimé dans les cellules dans lequel il a pénétré.
- un ADN (CRISPR). Après transcription, cet ADN fourni un ARN qui va guider Cas9 vers l'ADN cible. Pour cela, cet ARN doit posséder une séquence complémentaire d'une séquence de l'ADN cible, et un domaine de recrutement de Cas9. En se positionnant au niveau de l'ADN cible par hybridation spécifique, et en liant Cas9, cet ARN permet une localisation précise de Cas9 et donc de son action.
3. Guérison d'un modèle animal de myopathie par thérapie génique
Trois équipes de recherches ont donc choisi d'utiliser l'outil CRISPR-Cas9 pour tenter de réparer le gène DMD des cellules musculaires d'un modèle murin de myopathie de Duchenne, les souris mdx (voir ref. 2, 3 et 4). Dans les trois cas l'approche s'est faite in vivo et en post-natal, ce qui correspond à des conditions parfaitement adaptées à une technique qui pourrait être utilisée chez l'Homme. Chez ces souris mdx, le gène DMD n'est pas absent mais une mutation a provoqué l'apparition d'un codon STOP précoce. La protéine ne peut donc pas être synthétisée. L'idée a été d'enlever l'exon contenant la mutation dans l'ADN des cellules musculaires de ces souris en utilisant CRISPR-Cas9, ceci afin de restaurer la synthèse d'une protéine presque complète. Pour cela il fallait choisir le lieu d'action de Cas9 sur le gène DMD et synthétiser l'ADN CRISPR portant une séquence complémentaire, et choisir le vecteur devant apporter l'ADN de CRISPR et de Cas9 aux cellules musculaires. Dans le cas présent il s'agit d'un virus.
Les trois équipes ont obtenu des résultats similaires : en apportant localement ou par voie systémique le virus contenant le système CRISPR adapté-Cas9, les souris traitées ont vu leur état s'améliorer dans les jours, semaines et mois qui ont suivi. Toutes les cellules musculaires ne se mettent pas à exprimer de la dystrophine, la protéine n'étant pas complète elle n'est pas fonctionnelle à 100 %, mais les souris ont montré une amélioration de leurs capacités musculaires. La maladie a donc été, au moins partiellement, guérie par cette approche de thérapie génique.
4. Perspectives
Ce résultat fait bien entendu naître l'espoir de la mise au point d'un traitement de la myopathie de Duchenne chez l'Homme. Et comme toujours en pareille situation il convient de rappeler que, si ces premiers résultats sont encourageants, il reste encore beaucoup à faire pour en arriver à un traitement utilisable chez l'Homme. Pour en arriver là il faut déjà faire en sorte que la technique fonctionne également chez l'Homme. Mais il faut en plus s'assurer de la spécificité de la modification. Le système utilisé est sensé modifier le génome de manière ciblée et contrôlée, mais il faut évidemment s'assurer que ce soit le cas chez l'Homme. Des modifications non contrôlées pourraient en effet provoquer d'autres désordres forcement imprévisibles et potentiellement inacceptables. Nul doute que beaucoup, à commencer par les auteurs de ces trois études, travaillent déjà ou vont travailler sur la méthode utilisée dans ces trois études pour la tester plus avant, pour l'améliorer, pour la développer, avec l'idée de pouvoir l'utiliser un jour chez l'Homme.
5. Bibliographie
- A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity. Martin Jinek, Krzysztof Chylinski, Ines Fonfara, Michael Hauer, Jennifer A. Doudna, Emmanuelle Charpentier. Science. 2012. 337:816-821.
- Postnatal genome editing partially restores dystrophin expression in a mouse model of muscular dystrophy. Chengzu Long1,2,3,*, Leonela Amoasii, Alex A. Mireault, John R. McAnally, Hui Li, Efrain Sanchez-Ortiz, Samadrita Bhattacharyya, John M. Shelton, Rhonda Bassel-Duby, Eric N. Olson. Science. 2015. 10.1126.
- In vivo genome editing improves muscle function in a mouse model of Duchenne muscular dystrophy. Christopher E. Nelson, Chady H. Hakim, David G. Ousterout, Pratiksha I. Thakore, Eirik A. Moreb, Ruth M. Castellanos Rivera, Sarina Madhavan, Xiufang Pan, F. Ann Ran, Winston X. Yan, Aravind Asokan, Feng Zhang, Dongsheng Duan, Charles A. Gersbach. Science. 2015. 10.1126.
- In vivo gene editing in dystrophic mouse muscle and muscle stem cells. Mohammadsharif Tabebordbar, Kexian Zhu, Jason K. W. Cheng, Wei Leong Chew, Jeffrey J. Widrick, Winston X. Yan, Claire Maesner, Elizabeth Y. Wu, Ru Xiao, F. Ann Ran, Le Cong, Feng Zhang, Luk H. Vandenberghe, George M. Church, Amy J. Wagers. Science. 2015. 10.1126